Уравнение связывающее термодинамические параметры и константу равновесия

webkonspect.com — сайт, с элементами социальной сети, создан в помощь студентам в их непростой учебной жизни.
Здесь вы сможете создать свой конспект который поможет вам в учёбе.
Чем может быть полезен webkonspect.com:
- простота создания и редактирования конспекта (200 вопросов в 3 клика).
- просмотр конспекта без выхода в интернет.
- удобный текстовый редактор позволит Вам форматировать текст, рисовать таблицы, вставлять математические формулы и фотографии.
- конструирование одного конспекта совместно с другом, одногрупником.
- webkonspect.com — надёжное место для хранения небольших файлов.
Химическое равновесие. Принцип Ле Шателье
Материалы портала onx.distant.ru
Понятие химического равновесия
Признаки химического равновесия
Принцип Ле Шателье
Влияние температуры на химическое равновесие
Влияние давления на химическое равновесие
Влияние концентрации на химическое равновесие
Константа химического равновесия
Примеры решения задач
Задачи для самостоятельного решения
Понятие химического равновесия
Равновесным считается состояние системы, которое остается неизменным, причем это состояние не обусловлено действием каких-либо внешних сил. Состояние системы реагирующих веществ, при котором скорость прямой реакции становится равной скорости обратной реакции, называется химическим равновесием. Такое равновесие называется еще подвижным или динамическим равновесием.
Признаки химического равновесия
- Состояние системы остается неизменным во времени при сохранении внешних условий.
- Равновесие является динамическим, то есть обусловлено протеканием прямой и обратной реакции с одинаковыми скоростями.
- Любое внешнее воздействие вызывает изменение в равновесии системы; если внешнее воздействие снимается, то система снова возвращается в исходное состояние.
- К состоянию равновесия можно подойти с двух сторон – как со стороны исходных веществ, так и со стороны продуктов реакции.
- В состоянии равновесия энергия Гиббса достигает своего минимального значения.
Принцип Ле Шателье
Влияние изменения внешних условий на положение равновесия определяется принципом Ле Шателье (принципом подвижного равновесия):
Если на систему, находящуюся в состоянии равновесия, производить какое–либо внешнее воздействие, то в системе усилится то из направлений процесса, которое ослабляет эффект этого воздействия, и положение равновесия сместится в том же направлении.
Принцип Ле Шателье применим не только к химическим процессам, но и к физическим, таким как кипение, кристаллизация, растворение и т. д.
Рассмотрим влияние различных факторов на химическое равновесие на примере реакции окисления NO:
Влияние температуры на химическое равновесие
При повышении температуры равновесие сдвигается в сторону эндотермической реакции, при понижении температуры – в сторону экзотермической реакции.
Степень смещения равновесия определяется абсолютной величиной теплового эффекта: чем больше по абсолютной величине энтальпия реакции ΔH, тем значительнее влияние температуры на состояние равновесия.
В рассматриваемой реакции синтеза оксида азота (IV) повышение температуры сместит равновесие в сторону исходных веществ.
Влияние давления на химическое равновесие
Сжатие смещает равновесие в направлении процесса, который сопровождается уменьшением объема газообразных веществ, а понижение давления сдвигает равновесие в противоположную сторону.
В рассматриваемом примере в левой части уравнения находится три объема, а в правой – два. Так как увеличение давления благоприятствует процессу, протекающему с уменьшением объема, то при повышении давления равновесие сместится вправо, т.е. в сторону продукта реакции – NO2. Уменьшение давления сместит равновесие в обратную сторону. Следует обратить внимание на то, что, если в уравнении обратимой реакции число молекул газообразных веществ в правой и левой частях равны, то изменение давления не оказывает влияния на положение равновесия.
Влияние концентрации на химическое равновесие
Для рассматриваемой реакции введение в равновесную систему дополнительных количеств NO или O2 вызывает смещение равновесия в том направлении, при котором концентрация этих веществ уменьшается, следовательно, происходит сдвиг равновесия в сторону образования NO2. Увеличение концентрации NO2 смещает равновесие в сторону исходных веществ.
Катализатор одинаково ускоряет как прямую, так и обратную реакции и поэтому не влияет на смещение химического равновесия.
При введении в равновесную систему (при Р = const) инертного газа концентрации реагентов (парциальные давления) уменьшаются. Поскольку рассматриваемый процесс окисления NO идет с уменьшением объема, то при добавлении инертного газа равновесие сместится в сторону исходных веществ.
Константа химического равновесия
Для химической реакции:
константа химической реакции Кс есть отношение:
В этом уравнении в квадратных скобках – концентрации реагирующих веществ, которые устанавливаются при химическом равновесии, т.е. равновесные концентрации веществ.
Константа химического равновесия связана с изменением энергии Гиббса уравнением:
ΔGT о = – RTlnK (2)
Примеры решения задач
Задача 1. При некоторой температуре равновесные концентрации в системе 2CO (г) + O2 (г)→2CO2 (г) составляли: [CO] = 0,2 моль/л, [O2] = 0,32 моль/л, [CO2] = 0,16 моль/л. Определите константу равновесия при этой температуре и исходные концентрации CO и O2, если исходная смесь не содержала СО2.
Решение.
Вещество
Во второй строке под Спрореагир понимается концентрация прореагировавших исходных веществ и концентрация образующегося CO2, причем, Сисходн= Спрореагир + Сравн.
Задача 2. Используя справочные данные, рассчитайте константу равновесия процесса
Решение.
ΔG298 о = 2·(- 16,71) кДж = -33,42·10 3 Дж.
lnK = 33,42·10 3 /(8,314× 298) = 13,489. K = 7,21× 10 5 .
Задача 3. Определите равновесную концентрацию HI в системе
если при некоторой температуре константа равновесия равна 4, а исходные концентрации H2 , I2 и HI равны, соответственно, 1, 2 и 0 моль/л.
Решение. Пусть к некоторому моменту времени прореагировало x моль/л H2.
| Вещество | H2 | I2 | HI |
| сисходн., моль/л | 1 | 2 | 0 |
| спрореагир., моль/л | x | x | 2x |
| cравн., моль/л | 1-x | 2-x | 2x |
Тогда, К = (2х) 2 /((1-х)(2-х))
Решая это уравнение, получаем x = 0,67.
Значит, равновесная концентрация HI равна 2× 0,67 = 1,34 моль/л.
Задача 4. Используя справочные данные, определите температуру, при которой константа равновесия процесса: H2(г) + HCOH(г) →CH3OH(г) становится равной 1. Принять, что ΔН о Т » ΔН о 298, а ΔS о T » ΔS о 298.
Решение.
Если К = 1, то ΔG о T = — RTlnK = 0;
ΔН о 298 = -202 – (- 115,9) = -86,1 кДж = — 86,1× 10 3 Дж;
ΔS о 298 = 239,7 – 218,7 – 130,52 = -109,52 Дж/К;
0 = — 86100 — Т·(-109,52)
Задача 5. Для реакции SO2(Г) + Cl2(Г) →SO2Cl2(Г) при некоторой температуре константа равновесия равна 4. Определите равновесную концентрацию SO2Cl2, если исходные концентрации SO2, Cl2 и SO2Cl2 равны 2, 2 и 1 моль/л соответственно.
Решение. Пусть к некоторому моменту времени прореагировало x моль/л SO2.
| Вещество | SO2 | Cl2 | SO2Cl2 |
| cисходн., моль/л | 2 | 2 | 1 |
| cпрореагир., моль/л | x | x | х |
| cравн., моль/л | 2-x | 2-x | x + 1 |
Решая это уравнение, находим: x1 = 3 и x2 = 1,25. Но x1 = 3 не удовлетворяет условию задачи.
Следовательно, [SO2Cl2] = 1,25 + 1 = 2,25 моль/л.
Задачи для самостоятельного решения
1. В какой из приведенных реакций повышение давления сместит равновесие вправо? Ответ обоснуйте.
Так как увеличение давления благоприятствует процессу, протекающему с уменьшением количества
газообразных веществ, то равновесие сместится вправо в реакции 3.
2. При некоторой температуре равновесные концентрации в системе:
составляли: [HBr] = 0,3 моль/л, [H2] = 0,6 моль/л, [Br2] = 0,6 моль/л. Определите константу равновесия и исходную концентрацию HBr.
К = 4; исходная концентрация HBr составляет 1,5 моль/л.
3. Для реакции H2(г) + S(г) →H2S(г) при некоторой температуре константа равновесия равна 2. Определите равновесные концентрации H2 и S, если исходные концентрации H2, S и H2S равны, соответственно, 2, 3 и 0 моль/л.
[H2] = 0,5 моль/л; [S] = 1,5 моль/л.
4. Используя справочные данные, вычислите температуру, при которой константа равновесия процесса
становится равной 1. Примите, что ΔН о Т≈ΔН о 298, а ΔS о T≈ΔS о 298
5. Используя справочные данные, рассчитайте константу равновесия процесса:
6. Для реакции 2С3Н8(г) → н-С5Н12(г)+СН4(г) при температуре 1000 К константа равновесия равна 4. Определите равновесную концентрацию н-пентана, если исходная концентрация пропана равна 5 моль/л.
7. При температуре 500 К константа равновесия процесса:
равна 3,4·10 -5 . Вычислите Δ G о 500.
8. При температуре 800 К константа равновесия процесса н-С6Н14(г)+ 2С3Н6(г)+Н2(г) равна 8,71. Определите ΔG о f,800(С3Н6(г)), если ΔG о f,800(н-С6Н14(г)) = 305,77 кДж/моль.
9. Для реакции СО(г) + Cl2(г) →СO2Cl2(г) при некоторой температуре равновесная концентрация СO2Cl2(г) равна 1,2 моль/л. Определите константу равновесия данного процесса, если исходные концентрации СО(г) и Cl2(г) равны соответственно 2,0 и 1,8 моль/л.
10. При некоторой температуре равновесные концентрации в системе 2SО2(г) + О2(г) →2SO3(г) составляли: [SО2 ]=0,10 моль/л, [О2]=0,16 моль/л, [SО3]=0,08 моль/л. Вычислите константу равновесия и исходные концентрации SО2 и О2.
К=4,0; исходная концентрация SО2 составляет 0,18 моль/л;
исходная концентрация О2 составляет 0,20 моль/л.
Связь константы равновесия с термодинамическими величинами.
Значение константы равновесия связано с основными термодинамическими функциями ( 

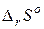

где 

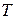

Уравнение (45) называется уравнением изотермы химической реакции для состояния равновесия.
Учитывая, что 


Соотношения (45) и (46) позволяют непосредственно выявить влияние как энтальпийного фактора, так и энтропии на константу равновесия обратимых химических реакций.
Смещение химического равновесия. Принцип Ле-Шателье
Изменение условий (температура, давление, концентрация), при которых система находится в состоянии химического равновесия, вызывает нарушение равновесия в результате неодинакового изменения скоростей прямой и обратной реакции. С течением времени в системе устанавливается новое химическое равновесие, соответствующее новым условиям. Переход из одного равновесного состояния в другое называется сдвигом или смещением положения равновесия.
Направление смещения положения химического равновесия в результате изменения внешних условиях определяется принципом Ле Шателье:
если на систему, находящуюся в состоянии равновесия, оказать внешнее воздействие (изменить температуру, давление, концентрацию), то равновесие смещается в сторону того процесса, который уменьшает это воздействие.
1. влияние температуры на состояние равновесия определяется знаком теплового эффекта:
при повышении температуры (нагревании) равновесие обратимой реакции смещается в сторону эндотермической реакции; при понижении температуры (охлаждении) равновесие обратимой реакции смещается в сторону экзотермической реакции.
Например, для реакции
при повышении температуры равновесие смещается в сторону обратной реакции – эндотермической, протекающей с поглощением теплоты.
2. влияние давления на состояние равновесия определяется изменением объема или количества моль газообразных веществ в ходе реакции:
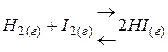 Þ Þ  , т.к. , т.к.  Таким образом, ни увеличение, ни уменьшение давления не смещают это равновесие. Таким образом, ни увеличение, ни уменьшение давления не смещают это равновесие. |  Þ Þ  , т.к. , т.к.  Таким образом, увеличение давления приведёт к смещению равновесия вправо, а уменьшение – влево. Таким образом, увеличение давления приведёт к смещению равновесия вправо, а уменьшение – влево. |
3. влияние концентрации реагирующих веществ на состояние равновесия:
при увеличении концентрации какого-либо вещества (путем его добавления) равновесие обратимой реакции смещается в сторону реакции, по которой это вещество реагирует, то есть расходуется. При уменьшении концентрации какого-либо вещества равновесие обратимой реакции смещается в сторону реакции, по которой это вещество образуется.
Например, для обратимой реакции 



Фазовое равновесие
Гетерогенные равновесия, связанные с переходом вещества из одной фазы в другую без изменения химического состава называются фазовыми.
Одним из наиболее общих законов гетерогенных равновесий (в том числе и фазовых) является правило фаз Гиббса (1876 г.):
в равновесной многофазной системе число степеней свободы (С) равно числу независимых компонентов системы (К) минус число фаз (Ф), плюс 2, где два – это число внешних факторов (p и T):

Компонент – химически однородное вещество, являющееся независимым составляющим веществом системы, может быть выделено из системы, и существовать изолировано любое время.
Например, для раствора хлорида калия (KCl) число компонентов равно 2.
В качестве независимых компонентов выбираются те вещества, наименьшее число которых достаточно для образования, как всей системы, так и любой её фазы.
Например, для образования равновесной системы из трех составляющих веществ 



Следовательно, число независимых компонентов в данном случае равно двум.
Фаза – часть системы, отделенная от других её частей поверхностью раздела, переходя через которую свойства меняются скачкообразно.
Например, в равновесной системе, описанной уравнением (49), число фаз равно 2.
Степень свободы – число условий ( Т, р, С), которые можно менять произвольно в известных пределах, не меняя этим числа или вида фаз.
Гетерогенные многофазные системы могут быть классифицированы:
| 1. по числу степеней свободы: | 2. по числу компонентов: |
| · инвариантные (С=0); · моновариантные (С=1); · бивариантные (С=2); · поливариантные (С›2); | · однокомпонентные (К=1); · двухкомпонентные (К=2); · трехкомпонентные (К=3). |
Рассмотрим равновесную гетерогенную систему:

Для геометрического изображения равновесного состояния гетерогенных систем используют диаграммы состояния.
Диаграмма состояния, описывающая систему (50) представлена на рисунке 3.
Рис. 3. Диаграмма состояния воды
Каждой фазе (жидкой, твердой, газообразной) отвечает определенное поле диаграммы, ограниченное от других фаз линией, характеризующей равновесие между данными двумя фазами ( 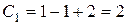
Кривая ОА – отвечает равновесию в системе лед-пар (кривая возгонки);
Кривая ОС – равновесию в системе вода-пар (кривая испарения);
Кривая ОВ – равновесию в системе лед-вода (кривая плавления).
Следовательно, каждая кривая относится к двухфазной системе. Такие системы являются моновариантными ( 
Например, кривая ОС является кривой давления насыщенного пара над жидкой водой. Эта кривая показывает, что каждой температуре соответствует одно определенное давление пара, и, наоборот, каждому давлению соответствует определенная температура, при которой вода и пар находятся в равновесие. Так, при температуре 100˚С (рис. 3) обе фазы находятся в равновесии между собой только когда давление водяного пара равно 101,3∙10 5 Па. Изменение давления пара при той же температуре приведет к однофазной системе.
В точке О пересекаются все три кривые, характеризующие равновесие в указанных двухфазных системах. Эта точка отвечает равновесию между всеми тремя фазами: лед-вода-пар и называется тройной точкой.
Согласно правилу фаз (48) число степеней свободы в тройной точке равно нулю ( 


Правило фаз помогает анализировать сложные химические процессы, протекающие в гетерогенных системах.
http://chemege.ru/ravnovesie/
http://megalektsii.ru/s48758t3.html


