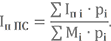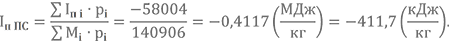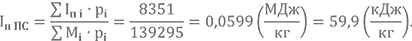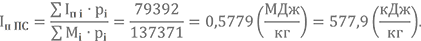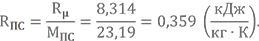Материальный и тепловой балансы камер сгорания
Основными физико-химическими характеристиками топлива являются его элементарный состав и теплота сгорания (теплотворная способность).
Стабильную часть любого топлива составляет его горючая масса – массовые процентные содержания углерода (Сг) водорода (Нг), горючей серы (Sг.л.), кислорода (Ог) и азота (Nг) [ 3] :
В состав рабочего топлива входит, кроме элементов горючей массы, так называемый, балласт топлива (А, W – процентные массовые содержания механических примесей и влаги):
Взаимосвязь массового состава рабочего топлива и его горючей массы осуществляется соотношениями:

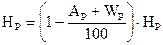
Горючая масса газообразного топлива обычно характеризуется мольным (объемным ) содержанием индивидуальных газов – водорода (Н2) различных углеводородов (СmHn), окиси углерода (СО), углекислого газа (СО2) азота (N2) и т.п.
Средняя мольная масса горючей массы газообразного топлива определяется следующим известным термодинамическим соотношением:
Элементарный массовый состав горючей массы газообразного топлива определяется соотношениями:
Нг =
Sгл =
Ог =
Nг =
где mi , ni, pi, qi, 

Теоретически необходимый расход кислорода для полного окисления горючих элементов единицы количества (1 кг) рабочего топлива:
= 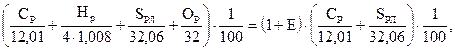
где Е – характеристика элементарного состава горючей массы топлива, определяемая как отношение расхода кислорода на окисление свободного водорода (Нг – 0,126×Ог) к расходу кислорода на окисление углерода и серы (Сг + 0,375×Sгл):
Е = 
Отсюда теоретически необходимый расход сухого воздуха (массовое содержание кислорода в воздухе равно 0,2315, что соответствует мольной концентрации 0,2095), кг/кг :
Расчетной теплотворной способностью топлива называется количества тепла, которое выделяется при полном сгорании топлива в условиях, исключающих возможность конденсации водяных паров (низшая теплотворная способность, Qнр).
С учетом изложенных соотношений, общее уравнение материального баланса процесса сгорания топлива (масса образующихся продуктов сгорания 1 кг топлива) записывается в виде [3]:

где Y — относительная влажность наружного воздуха; х s – массовое содержание влаги при полном насыщении воздуха в пересчете на 1 кг сухого воздуха; Dх1,2 — дополнительно введенное при сжигании топлива количество воды или водяного пара в пересчете на 1 кг сухого воздуха, в кг/кг; a — коэффициент избытка воздуха, определяемое как отношение общего количества воздуха к теоретически необходимому (a = L/L0); L0 – теоретически необходимый расход воздуха в кг на кг топлива.
В инженерных расчетах, при отсутствии подачи воды или пара в камеру сгорания (Yх s + Dx1,2 =0), уравнение (4.12) принимает вид (G = 1+ a L0).
Исходным уравнением для составления теплового баланса камеры сгорания служит первое начало термодинамики для потока по внешнему балансу тепла:
где Q * 1,2 — количество тепла, подведенного извне и определяемого как произведение коэффициента полезного действия камеры сгорания на тепло сгорания всего израсходованного топлива BQнр:
Q * 1,2 = hкс×BQнр. ; hкс = 1 — 
где qхим. – потери от химической неполноты сгорания топлива, %. Потери от механической неполноты сгорания; при сжигании газообразного топлива их можно считать равными нулю (qмех. = 0); qохл. – потери тепла от наружного охлаждения камер сгорания, %.
При составлении теплового баланса камеры сгорания ГТУ принимается, что внешняя работа W * 1,2 в уравнении (4.13) равна нулю, в силу того, что сгорание топлива идет при постоянном давлении (dW * = -VdP = 0).
Определение расчетных значений энтальпии в начальном Н1 и конечном состоянии, уравнение (4.13), для камеры сгорания в общем виде связано с выбором начала отсчета энтальпии.
В исследованиях процессов сгорания топлива тепло сгорания определяется уравнением стандартной температуры калориметрирования (tQ = 20 0 C). Отсюда следует, что все значения энтальпий и само уравнение теплового баланса камеры сгорания, строго говоря, должны строиться над уровнем колориметрирования топлива, при котором Н (tQ) = 0.
Это значит, что выражение теплового баланса камер сгорания с учетом всех потоков теплоносителей, отнесенных к одному кг топлива будет иметь вид [3]:
где aL0 – расход сухого воздуха по камере сгорания, отнесенный к единице количества топлива, кг/кг; С 0 pm – средняя теплоемкость воздуха в интервале температур (t1 – tQ); t3 — средняя температура продуктов сгорания при входе в газовую турбину (на выходе из камеры сгорания); Сpm — средняя температура воздуха в интервале температур (t1 – tQ); t1 – температура воздуха, поступившего в камеру сгорания из компрессора (или регенератора); Сpm — средняя температура топлива в интервале температур (tB – tQ); tB — температура топлива на входе в камеру сгорания.
Разрешая последнее уравнение относительно коэффициента a, получим:

Нетрудно видеть, что увеличением газов перед турбиной (t3) при прочих равных условиях величина (a) убывает.
Для получения количественной оценки этой связи, полученное уравнение можно без большой погрешности несколько упростить, положив tв = tQ = t1 ; сpm =idem. Величину L0 можно найти по эмпирическому уравнению Вельтера-Бертье-Коновалова, Qнр 
L0 = 
В технических расчетах обычно принимается, что тепло сгорания топлива не зависит от температуры калориметрирования, что позволяет температуру начала отсчета энтальпии принять любой, а уравнение теплового баланса камеры сгорания записать в виде по отношению к одному кг топлива:
Из уравнения теплового баланса камеры сгорания (4.17) может быть определена температура продуктов сгорания на входе в турбину t3 или коэффициент избытка воздуха a. Если коэффициент избытка воздуха определен из уравнения материального баланса (4.12) на основе прямых измерений расхода топлива и воздуха, то из уравнения теплового баланса может быть установлен КПД камеры сгорания. Таким образом коэффициент избытка воздуха a является связующей характеристикой материального и теплового баланса камер сгорания газотурбинных установок.
Анализ приведенных соотношений показывает, что коэффициент избытка воздуха при неизменных значениях граничных температур цикла, растет с увеличением pк и снижается с его уменьшением. Введение в схему ГТУ регенерации тепла отходящих газов увеличивает коэффициент избытка воздуха сравнительно с установкой без регенерации тепла отходящих газов.
Коэффициент избытка воздуха весьма существенно изменяется по длине камеры сгорания, т. е. по мере возникновения, развития и завершения процесса сгорания топлива он возрастает по длине камеры сгорания.
Величина необходимого коэффициента первичного воздуха (aп), проходящего через регистр –завихритель, зависит от физических свойств топлива, параметров (температуры и давления) поступающего в камеру сжатого воздуха и общей объемной теплонапряженности самой камеры.
Так как воздух, поступающий в камеру сгорания разделяется на два потока, которые движутся между одинаковыми начальным (на входе в камеру) и конечным (на выходе из камеры) давлениями, то можно записать условие равенства потерь напора в виде [2]:
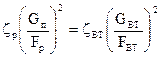
где Fp , zp — проходное сечение и коэффициент сопротивления завихрителя; Fвт , zвт — расчетное сечение и приведенный коэффициент сопротивления тракта движения вторичного воздуха.

то можно получить уравнение связи между aп и a:

Рассмотрение организации рабочего процесса в камере сгорания показывает, что весьма важную роль в его организации играет завихритель первичного воздуха. Он дозирует первичный воздух и стабилизирует пламя, его конструкция в значительной степени определяет всю аэродинамику потока. Первичный воздух, будучи закрученным завихрителем, прижимается к стенкам жаровой трубы, создавая тем самым в центре факела область пониженного давления, куда и устремляются горячие продукты сгорания, обеспечивая поджигание новой порции поступающего в камеру сгорания топлива. Наряду со струями вторичного воздуха, проникающими в зону горения создаются условия хорошего перемешивания топлива с воздухом, что решающим образом сказывается на образовании равномерного температурного поля на выходе из камеры сгорания.
Пример 4.1. Определить мольную массу, элементарный состав газа, а также массовый расход воздуха для окисления 1 кг (1 м 3 ) сжигаемого топлива следующего состава: метан – СН4 = 94,2% ; этан – С2Н6 = 2,3% ; пропилен – С3Н6 = 0,5% ; пропан – С3Н8 = 1,1 % ; азот – N2 = 1,2% ; углекислый газ — СО2 =0,7%.
Решение. Средняя мольная масса сухого газообразного топлива (mm) определяетcя из соотношения:
Тепловой расчет основных параметров камеры сгорания ГТУ
Тепловой расчет камеры сгорания предполагает определение необходимого расхода топлива 
где 


Энтальпию газов на входе в газовую турбину находим, пользуясь таблицами [3], при величине Tс=1360 K, а также по значениям параметра состава газа за ГТУ βг и молекулярной массы продуктов сгорания за ГТУ μг. В общем случае величины βг и μг рассчитываются в зависимости от состава топлива и избытка воздуха соответственно по формулам приложения 1.
Расчет состава и энтальпия продуктов сгорания газообразного топлива
 |
Объемный состав (м 3 /м 3 ), продуктов сгорания газообразного топлива может быть определен по следующим формулам:
 м 3 /м 3 . м 3 /м 3 . |
 |
 |
 м 3 /м 3 . м 3 /м 3 . |
Полный относительный объем продуктов сгорания газового топлива:
 м 3 /м 3 . м 3 /м 3 . |
Объемные доли продуктов сгорания:
 |
Параметр β для газовой смеси известного состава выражается уравнением:
 |
Молекулярная масса продуктов сгорания:
 |
В рассматриваемом режиме принимаем температуру поступающего в КС топлива (возможен его предварительный подогрев): 

Решение уравнения теплового баланса камеры сгорания выполняем, одновременно оценивая избыток воздуха 

Коэффициент избытка воздуха в камере сгорания определяем графически (рис. 1.3): прямая 1 соответствует энтальпии воздуха, найденной в конце расчета показателей осевого компрессора: 
Задаемся несколькими значениями величины 
Графическое определение коэффициента избытка воздуха в КС ГТУ
Коэффициент избытка воздуха,
1— прямая, соответствующая значению Нкк, определенному при расчете показателей осевого компрессора; 2 — кривая, полученная при расчете уравнения теплового баланса
камеры сгорания ГТУ
Определение коэффициента избытка воздуха в камере сгорания ГТУ
 | 2,1 | 2,2 | 2,3 | 2,4 | 2,5 | 2,6 |
 кДж/кг кДж/кг | 1394,8 | 1390,9 | 1387,1 | 1384,2 | 1381,2 | |
 кДж/кг кДж/кг | 193.204 | 243,815 | 289,789 | 332,573 | 371,532 | 408,114 |
В процессе расчета определено:
βг = 1; μг = 28,05; 

Расход топлива в камере сгорания ГТУ определяем из выражения теплового баланса КС: от
Расход воздуха за компрессором, поступающий в камеру сгорания ГТУ:
Величину утечек воздуха из уплотнений ротора и другие принимаем из интервала 0,3÷0,5% от

— долю воздуха, поступающую в камеру сгорания ГТУ:
Беседы о ракетных двигателях
Просто о том, что кажется сложным
Урок 08. Тепловой расчёт камеры. Способ второй – лирический (ч.4)

Мы продолжаем рассматривать особенности теплового расчёта и сегодня поговорим о том, как определить температуру продуктов сгорания в камере сгорания.
Если помните, при определении парциальных давлений газов мы задавались тремя значениями температуры в окрестности ожидаемой. Однако мы так и не выяснили, каково же её действительное значение. Для определения температуры можно использовать уравнение сохранения энергии, выраженной через энтальпии топлива и продуктов сгорания. Т.е., согласно этому закону можно утверждать, что полная энтальпия топлива равна полной энтальпии продуктов сгорания на входе в сопло при температуре, равной температуре газов в камере сгорания. Полную энтальпию топлива мы с Вами считать уже умеем. Если что-то подзабылось, вернитесь к уроку 3. Остаётся дело за малым – определить полную энтальпию продуктов сгорания при «не очень известной» температуре.
Здесь нам на помощь опять придут справочные данные. Значения полной энтальпии для простейших газов, таких как CO2, H2O, NO и пр., в зависимости от температуры известны и занесены в справочники. Посмотреть их можно, например, здесь. Конечно, возникает некоторая сложность, связанная с тем, что значения энтальпии приведены только для вполне конкретных температур, и её промежуточные значения нужно как-то определить. Здесь существует два пути: с помощью интерполяции находить промежуточные значения, вычислять полную энтальпию смеси и сравнивать с энтальпией топлива, либо можно выбрать значения для трёх заданных нами ранее температур, опять же вычислить полную энтальпию для этих трёх точек и построить по ним сглаживающий график. Затем графическим путём определить температуру, соответствующую полной энтальпии топлива. Точность такого способа определения оказывается вполне приемлемой для тепловых расчётов (единицы Кельвинов), к тому же он, на мой взгляд, более удобен и не лишён некоторого изящества 🙂 .
Для вычисления полной энтальпии продуктов сгорания воспользуемся формулой
Здесь Mi – молярная масса i-го газа в кг/кмоль, численно равная относительной молекулярной массе.
Продолжим расчёт камеры на основе НДМГ+АТ, несколько отложенный в сторону с позапрошлого урока. Состав продуктов сгорания для Т1 = 3300 К; Т2 = 3400 К; Т3 = 3500 К мы посчитали. Определим полную энтальпию продуктов сгорания для этих температур.
Выпишем значения энтальпий составляющих газов и занесём их в таблицу. Также для удобства подсчитаем произведения энтальпий и молярных масс на соответствующие парциальные давления.
Т1 = 3300 К
| pN2 | pCO2 | pCO | pH2 | pH2O | pOH | pNO | pH | pO2 | pO | pN | ||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Iп i , МДж кмоль | 104,1 | -221,0 | -5,655 | 100,2 | -100,6 | 143,2 | 197,0 | 280,6 | 110,4 | 310,7 | 420,9 | |
| Mi , кг кмоль | 28 | 44 | 28 | 2 | 18 | 17 | 30 | 1 | 32 | 16 | 14 | |
| pi , кПа | 1743 | 548,6 | 813,5 | 408,7 | 2156 | 151,7 | 43,95 | 73,97 | 39,10 | 19,15 | 2,205 | ∑pi = 6000 кПа |
| Iп i·pi | 181446 | -121241 | -4600 | 40952 | -216894 | 21723 | 8658 | 20756 | 4317 | 5950 | 928 | ∑Iп i·pi = =-58004 |
| Mi·pi | 48804 | 24138 | 22778 | 817 | 38808 | 2579 | 1319 | 74 | 1251 | 306 | 31 | ∑Mi·pi = =140906 |
Таким образом полная энтальпия при Т1 = 3300 К
Аналогично поступаем для двух других температур.
Т2 = 3400 К
| pN2 | pCO2 | pCO | pH2 | pH2O | pOH | pNO | pH | pO2 | pO | pN | ||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Iп i , МДж кмоль | 107,9 | -214,6 | -1,910 | 103,9 | -95,09 | 147,0 | 200,8 | 282,7 | 114,4 | 312,8 | 423,0 | |
| Mi , кг кмоль | 28 | 44 | 28 | 2 | 18 | 17 | 30 | 1 | 32 | 16 | 14 | |
| pi , кПа | 1716 | 504,7 | 841,8 | 434,1 | 2067 | 193,6 | 57,08 | 97,53 | 55,31 | 29,94 | 3,248 | ∑pi = 6000 кПа |
| Iп i·pi | 185156 | -108309 | -1608 | 45103 | -196551 | 28459 | 11462 | 27572 | 6327 | 9365 | 1374 | ∑Iп i·pi = =8351 |
| Mi·pi | 48048 | 22207 | 23570 | 868 | 37206 | 3291 | 1712 | 98 | 1770 | 479 | 45 | ∑Mi·pi = =139295 |
Полная энтальпия при Т2 = 3400 К
Т3 = 3500 К
| pN2 | pCO2 | pCO | pH2 | pH2O | pOH | pNO | pH | pO2 | pO | pN | ||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Iп i , МДж кмоль | 111,6 | -208,3 | 1,840 | 105,8 | -89,59 | 150,8 | 204,6 | 284,8 | 118,5 | 314,9 | 425,1 | |
| Mi , кг кмоль | 28 | 44 | 28 | 2 | 18 | 17 | 30 | 1 | 32 | 16 | 14 | |
| pi , кПа | 1684 | 457,2 | 870,8 | 464,4 | 1962 | 239,6 | 71,40 | 127,2 | 73,50 | 44,68 | 4,672 | ∑pi = 6000 кПа |
| Iп i·pi | 187934 | -95235 | 1602 | 49134 | -175776 | 36132 | 14608 | 36227 | 8710 | 14070 | 1986 | ∑Iп i·pi = =79392 |
| Mi·pi | 47152 | 20117 | 24382 | 929 | 35316 | 4073 | 2142 | 127 | 2352 | 715 | 65 | ∑Mi·pi = =137371 |
Полная энтальпия при Т3 = 3500 К
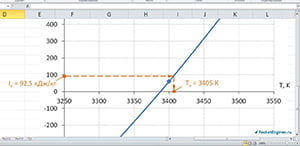
Построим график и, отложив на оси ординат величину энтальпии топлива, найдём температуру продуктов сгорания. Как видно на рисунке, Тк ≈ 3405 К.
Аналогично посчитаем молярную массу продуктов сгорания для трёх температур по формуле
Значения числителя и знаменателя записаны в таблицах. Подставляем в формулу и получаем МПС1 = 23,49 кг/кмоль, МПС2 = 23,21 кг/кмоль, МПС3 = 22,90 кг/кмоль.
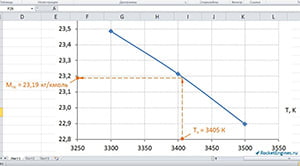
Строим график (см. рис.) и графически определяем для найденной температуры 3405 К значение молярной массы продуктов сгорания. МПС ≈ 23,19 кг/кмоль.
Также, нам понадобится газовая постоянная продуктов сгорания
Напоминаю, что Rμ = 8,314 кДж/(кмоль·К) — универсальная газовая постоянная.
На сегодня всё. Продолжим в следующем уроке.
Всем удачи!
http://megaobuchalka.ru/3/26931.html
http://rocketengines.ru/rocket-engines-studying/practice/chamber-computation/lesson-eight.html