Уравнение теплового баланса с изменением агрегатного состояния теплоносителей
3. Методические указания
Тепловая нагрузка аппаратов, расходы теплоносителя.
Тепловую нагрузку определяют из уравнения теплового баланса аппарата. В зависимости от условий протекания процесса тепловой баланс может быть выражен уравнениями:
при постоянно агрегатном состоянии теплоносителей
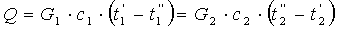 |
при изменении агрегатного состояния одного из теплоносителей
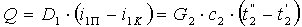 |
при изменении агрегатного состояния обоих теплоносителей
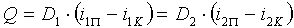 |
В этих уравнениях: Q — тепловая нагрузка; G1, G2 — расходы теплоносителей, не изменяющих агрегатного состояния; D1, D2 — расходы теплоносителей, изменяющих агрегатное состояние; c1, c2 — средние удельные теплоемкости теплоносителей; t’1, t»1 и t’2, t»2 — начальные и конечные температуры теплоносителей; i1п, i2п — теплосодержание пара; i1к, i2к — теплосодержание конденсата.
Расчет температурного режима теплообменника.
Расчет температурного режима теплообменника состоит в определении средней разности температур и вычисления средних температур теплоносителей. В зависимости от направления движения в теплообменных аппаратах рабочих сред теплообменники делятся на аппараты прямоточные, противоточные, с перекрестным и смешанным током (сложное направление течения теплоносителей).
Для прямоточной и противоточной схем среднюю разность температур определяют как среднее логарифмическое значение по формуле:
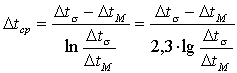 |
Если температура рабочих сред изменяется вдоль поверхности нагрева незначительно, то есть отношение
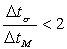 |
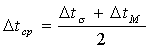 |
Формулы для вычисления средней разности температур для схем перекрестного и смешенного токов громоздки и неудобны. В расчетной практике рекомендуется для таких случаев сначала определять средне логарифмическую разность температур, как для противотока, а затем вносить соответствующую поправку (находится по графикам и таблицам).
Определение коэффициента теплопередачи и поверхности теплообмена.
Коэффициент теплопередачи К, входящий в основное уравнение теплообмена, характеризует сложный теплообмен в целом и может быть представлен как функция коэффициентов теплоотдачи по обеим сторонам от разделяющей стенки, а также термических сопротивлений стенки и загрязнений. Значение К зависит от формы стенки, разделяющей теплоносители.
Для плоской многослойной стенки:
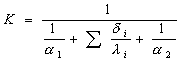 |
Для цилиндрической стенки (внутренний диаметр d1, наружный d2):
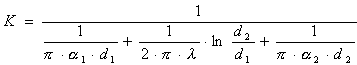 |
Коэффициент теплоотдачи определяют из соотношения:
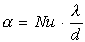 |
Поверхность теплообмена вычисляется по расчетной формуле:
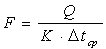 |
Если поверхность компонуется из труб, то:
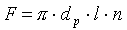 |
где dp — расчетный диаметр труб; l — длина труб; n — число труб.
ЛЕКЦИЯ 9 ОБЩИЕ ВОПРОСЫ ТЕПЛОПЕРЕДАЧИ УРАВНЕНИЕ ТЕПЛОВОГО БАЛАНСА БЕЗ ИЗМЕНЕНИЯ И ПРИ ИЗМЕНЕНИИ АГРЕГАТНОГО СОСТОЯНИЯ. ЗАКОН ФУРЬЕ
- Аркадий Левкович 3 лет назад Просмотров:
1 ЛЕКЦИЯ 9 ОБЩИЕ ВОПРОСЫ ТЕПЛОПЕРЕДАЧИ УРАВНЕНИЕ ТЕПЛОВОГО БАЛАНСА БЕЗ ИЗМЕНЕНИЯ И ПРИ ИЗМЕНЕНИИ АГРЕГАТНОГО СОСТОЯНИЯ. ЗАКОН ФУРЬЕ Перенос энергии в форме теплоты. Понятие о теплоотдаче и теплопередаче Механизмы переноса теплоты Процесс переноса теплоты называют теплообменом. В химической технологии принято называть жидкости или газы, участвующие в теплообмене, теплоносителями. В процессах теплообмена всегда присутствуют, как минимум, два теплоносителя — горячий и холодный. Перенос теплоты осуществляется тремя способами (механизмами): 1. Теплопроводность это молекулярный перенос теплоты между непосредственно соприкасающимися телами или частицами одного тела с различной температурой, при котором происходит обмен энергией движения структурных частиц (молекул, атомов, свободных электронов). В чистом виде теплопроводность наблюдается только в неподвижных средах — твердых телах. 2. Перенос теплоты конвекцией. Такой способ возможен только в подвижных средах, т.е. в жидкостях и газах. Теплота переносится макрообъемами среды при их перемещении под действием каких-либо сил. Конвекция всегда сопровождается теплопроводностью 3. Перенос теплоты излучением. В этом случае энергия переносится в виде электромагнитных волн через оптически прозрачную среду. При этом внутренняя энергия переходит в лучистую, которая впоследствии поглощается другими телами. В чистом виде такой механизм наблюдается в вакууме. Пример Солнце и планеты. В химической технологии существуют все три механизма переноса теплоты: в жидкостях это конвекция и теплопроводность; в твердых телах только теплопроводность; в газах это одновременно теплопроводность, конвекция и излучение. При описании процессов теплообмена, происходящих в промышленном оборудовании, различают два понятия: 1. Теплоотдача — перенос теплоты в пределах одной фазы от границы раздела или от стенки к жидкому (газообразному) теплоносителю (или наоборот); 2. Теплопередача — перенос теплоты от горячего теплоносителя к холодному через границу раздела или через разделяющую теплоносители теплопередающую твердую стенку. 1
2 Расчет теплообменной аппаратуры заключается в следующем: 1. Определение тепло нагрузок или тепло потоков отдельных аппаратов; 2. Определение требуемой поверхности теплопередачи с целью дальнейшего расчета основных размеров тепло аппаратов. Уравнения тепло балансов при изменении и без изменения агрегатного состояния Количество теплоты, передаваемого от более нагретого тела к менее нагретому за единицу времени, можно охарактеризовать величиной теплового потока Q (Вт) или величиной удельного теплового потока (плотность потока) q (Вт/м 2 ); q = Q / A где A — поверхность теплообмена (м 2 ). Теплообменник — аппарат, в котором происходит теплообмен между двумя теплоносителями: горячим (индекс 1) и холодным (индекс 2) (Рис.9.1.) Рис.9.1. Схема потоков в теплообменном аппарате В теплообменнике: массовые расходы горячего и холодного теплоносителей, ṁ1 и ṁ2, соответственно; температуры горячего теплоносителя на входе вх и оде ; температуры холодного теплоносителя на входе T2вх и оде T2. Количество теплоты, отдаваемой в единицу времени горячим теплоносителем Q 1 получаемое холодным теплоносителемq 2, определяется по формуле: Q + 1 = Q 2 Q пот (9.1) Q1 1 = H1 вх H Q2 = H2 H2вх (9.2) (9.3) и 2
3 где H1вх и H1 энтальпии горячего теплоносителя при температурах на входе в аппарат и оде из аппарата, соответственно, Вт; H2вх и H2 энтальпии холодного теплоносителя при температурах на входе в аппарат и оде из аппарата, соответственно, Вт; Q пот — тепловые потери в окружающую среду, Вт. Уравнения тепло балансов без изменения агрегатного состояния теплоносителей Если теплоноситель не изменяет своего агрегатного состояния, для определения количества теплоты формулы (9.2) и (9.3) можно преобразовать к виду: m 1 и m 2 c1 ( ) Q 1 = m 1c1 вх ( T T ) Q2 m2 c2 2 2вх = массовые расходы горячего и холодного теплоносителей, кг/с; (9.4) (9.5) — удельная изобарная теплоемкость горячего теплоносителя (Дж/кгК) при его средней температуре T 1 ср вх + = ; 2 c 2 — удельная изобарная теплоемкость холодного теплоносителя (Дж/кг К) при его средней температуреt 2 ср T2 вх + T2 =. 2 Уравнения тепло балансов с изменением агрегатного состояния теплоносителей 1. Если теплоноситель изменяет свое агрегатного состояния, например, конденсируется насыщенный пар, то для определения количества теплоты формулу (9.2) можно записать следующим образом: Q1 = m 1h1пара m 1c1 m 1 массовый расход пара, кг/с; h1пара удельная энтальпия конденсирующегося пара, (Дж/кг); c 1 — удельная изобарная теплоемкость конденсата при температуреt 1. (Дж/кгК). (9.6) Если конденсат пара выводится при температуре конденсации, т.е. записать: ( h1пара c1конд ) m 1 1 Q = 1 = m1 конд r r1 — удельная теплота конденсации насыщенного пара (Дж/кг). T конд 1 =, можно (9.7) 3
4 2. В случае, если жидкий теплоноситель кипит, то для определения количества теплоты формулу (9.3) можно записать следующим образом: m 2 ( h2пара c2кип T2кип ) m 2 2 Q = 2 = m2 r массовый расход кипящей жидкости; h 2пара удельная энтальпия образующегося при кипении пара; (9.8) c 2 кип — удельная изобарная теплоемкость жидкости при температуре кипения T 2 кип ; r2 — удельная теплота парообразования жидкости. Молекулярный и конвективный перенос. Феноменологический закон теплопроводности Фурье Температурным полем называют совокупность значений температур во всех точках рассматриваемой среды. Оно характеризует распределение температур в пространстве и во времени, может быть стационарным или нестационарным. Изотермическая поверхность — геометрическое место точек в среде с одинаковой температурой. Температурный градиент — вектор, направленный в сторону максимального возрастания температуры, т.е. являющийся производной по нормали к изотермической поверхности. T = gradt, n где n — единичный вектор, «нормальный» к изотермической поверхности. Фурье экспериментально установил, что при переносе теплоты теплопроводностью удельный тепловой поток q пропорционален градиенту температур, т.е.: T q = T = T gradt, (9.9) n где λt — коэффициент теплопроводности (Вт/(мК)). Знак «-» указывает, что теплота переносится в сторону уменьшения температуры. Фурье. Уравнение (9.9) называется феноменологическим законом теплопроводности Коэффициент теплопроводности для металлов равен Вт/(мК); для жидкостей 0,2 0,7 Вт/(мК); для газов 0,01 0,06 Вт/(мК). 4
5 Перенос теплоты конвекцией Уравнение теплоотдачи Перенос теплоты конвекцией осуществляется движущимися макрообъемами подвижной среды — жидкостью или газом. Различают: 1. Естественную (свободную конвекцию), которая вызвана разностью плотностей в различных точках объема (например, из-за разности температур); 2. Вынужденную конвекцию, возникающую в условиях принудительного движения жидкостей и газов с применением мешалок и насосов. Конвективный перенос намного интенсивнее молекулярной теплопроводности. В ядре потока, в турбулентной области, теплота переносится в основном конвекцией, а вблизи границы раздела или твердой стенки — только теплопроводностью. Главное термическое сопротивление переносу теплоты из ядра потока к твердой стенке или наоборот сосредоточено в тепловом пограничном слое. Уменьшая его толщину перемешиванием или увеличивая скорость потока, можно интенсифицировать теплоотдачу. Толщина теплового пограничного слоя пропорциональна коэффициенту температуропроводности а, м 2 /с: a = T, (9.10) c p Толщина гидродинамического пограничного слоя пропорциональна коэффициенту кинематической вязкости =, м 2 /с, т.е. δтепл
ν. Отношение Pr = называется теплообменным критерием Прандтля. a В общем случае δтепл δгидр. Если Pr = 1, то толщина теплового пограничного слоя равна толщине гидродинамического пограничного слоя. Такая картина характерна для газов. При этом будет наблюдаться подобие поля температур и поля скоростей, появляется возможность моделирования одного процесса другим. Таким образом, можно сделать вывод, что теплоотдача — процесс достаточно сложный. Математически описать ее не просто, т.к. неизвестен температурный градиент у стенки, также неизвестен профиль температур вдоль поверхности теплообмена. 5
6 Уравнение для описания теплоотдачи было экспериментально получено И.Ньютоном. Он установил, что скорость переноса теплоты пропорциональна разности температур между ядром потока теплоносителя и температурой на стенке. Уравнение теплоотдачи: ( T ) = A T ст (9.11) Q где — коэффициент теплоотдачи, Вт/м 2 К, Т — температура в ядре потока теплоносителя, Tст — температура стенки, A — поверхность стенки, м 2. Коэффициент теплоотдачи показывает, сколько теплоты в единицу времени передается через единицу поверхности из ядра потока к разделяющей теплоносители стенке (или наоборот — от стенки в ядро потока) при разности температур между ядром потока и стенкой в 1 градус. Использование этой зависимости для расчета теплоотдачи на практике достаточно сложно, т.к. неизвестна температура стенки. Величина коэффициента теплоотдачи зависит от множества параметров: скорости движения теплоносителя, геометрических размеров аппарата, физическохимиеских свойств (плотности, вязкости, теплоемкости и теплопроводности теплоносителя), состояния поверхности и т.д. Получить значения коэффициента теплоотдачи аналитически, решая уравнения описывающие теплообмен, затруднительно. Поэтому, также как и в гидравлике, приходится применять теорию подобия, обобщая опытные данные в виде критериальных зависимостей для типо случаев теплоотдачи. 6
Фазовые переходы и уравнение теплового баланса
теория по физике 🧲 термодинамика
Фазовые переходы — это термодинамические процессы, приводящие к изменению агрегатного состояния вещества.
Плавление и отвердевание
Для расчета количества теплоты, необходимого для процесса плавления, следует применять формулу:
m — масса вещества, λ (Дж/кг) — удельная теплота плавления.
Плавление каждого вещества происходит при определенной температуре, которую называют температурой плавления. Все проводимое тепло идет на разрушение кристаллической решетки, при этом увеличивается потенциальная энергия молекул. Кинетическая энергия остается без изменения и температура в процессе плавления не изменяется.
Удельная теплота плавления показывает, какое количество теплоты необходимо сообщить 1 кг данного вещества, чтобы перевести его из твердого состояния в жидкое при условии, что оно уже нагрето до температуры плавления. В процессе отвердевания 1 кг данной жидкости, охлажденной до температуры отвердевания, выделится такое же количество теплоты.
Внимание! Удельная теплота плавления — табличная величина.
Определение Отвердевание, или кристаллизация — переход состояния из жидкого состояния в твердое (это процесс, обратный плавлению).
Отвердевание происходит при той же температуре, что и плавление. В процессе отвердевания температура также не изменяется. Количество теплоты, выделяемое в процессе отвердевания:
Парообразование и конденсация
Количество теплоты, необходимое для процесса кипения, вычисляют по формуле:
m — масса вещества, r (Дж/кг) — удельная теплота парообразования.
Парообразование происходит при определенной температуре, которую называют температурой кипения. В отличие от испарения, процесс парообразования идет со всего объема жидкости. Несмотря на то, что к кипящему веществу подводят тепло, температура не изменяется. Все затраты энергии идут на увеличение промежутком между молекулами. Температура кипения зависит от рода вещества и внешнего атмосферного давления.
Удельная теплота парообразования показывает, какое количество теплоты необходимо затратить, чтобы перевести в пар 1 кг жидкости, нагретой до температуры кипения. Такое же количество теплоты выделится в процессе конденсации 1 кг пара, охлажденного до температуры конденсации.
Внимание! Удельная теплота парообразования — табличная величина.
Определение Конденсация — процесс, обратный кипению. Это переход вещества из газообразного состояния в жидкое.
Конденсация происходит при температуре кипения, которая также не изменяется во время всего процесса. Количество теплоты, выделяемое в процессе конденсации:
Тепловые процессы при нагревании и охлаждении
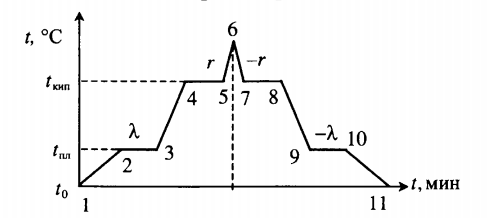
Все фазовые переходы, а также процессы нагревания и остывания вещества можно отобразить графически. Посмотрите на график фазовых переходов вещества:
Он показывает зависимость температуры вещества от времени в процессе его нагревания и остывания. Опишем процессы, отображаемые на графике, в таблице.
| Процесс | Что происходит | Количество выделенной теплоты | ||||||||||||||||||||||||||||||||||||||||||||||||
| 1–2 | Нагревание твердого тела | |||||||||||||||||||||||||||||||||||||||||||||||||
| 2–3 | Плавление при температуре плавления (tпл) | |||||||||||||||||||||||||||||||||||||||||||||||||
| 3–4 | Нагревание жидкости | |||||||||||||||||||||||||||||||||||||||||||||||||
| 4–5 | Кипение при температуре кипения (tкип) | |||||||||||||||||||||||||||||||||||||||||||||||||
| 5–6 | Нагревание пара | |||||||||||||||||||||||||||||||||||||||||||||||||
| 6–7 | Охлаждение пара | |||||||||||||||||||||||||||||||||||||||||||||||||
| 7–8 | Кипение при температуре кипения (tкип) | |||||||||||||||||||||||||||||||||||||||||||||||||
| 8–9 | Охлаждение жидкости | |||||||||||||||||||||||||||||||||||||||||||||||||
| 9–10 | Отвердевание при температуре плавления (tпл) | |||||||||||||||||||||||||||||||||||||||||||||||||
| 10–11 | Охлаждение твердого тела |
| Что происходит | График | Формула количества теплоты | |||||||||||||||||||||||||||||||||||||
| Полностью растопили лед, имеющий отрицательную температуру. | 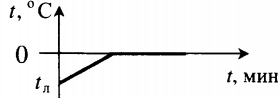 | ||||||||||||||||||||||||||||||||||||||
| Лед, взятый при отрицательной температуре, превратили в воду при комнатной температуре. | 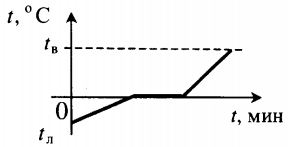 | ||||||||||||||||||||||||||||||||||||||
| Взяли лед при температуре 0 о С и полностью испарили. | 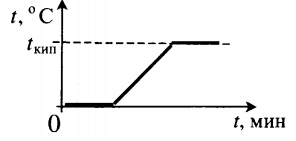 | ||||||||||||||||||||||||||||||||||||||
| Взяли воду при комнатной температуре и половину превратили в пар. | 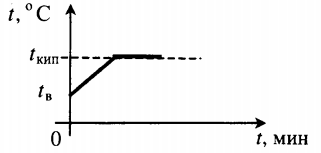 |
| Единицы измерения | Температуру можно оставлять в градусах Цельсия, так как изменение температуры в градусах Цельсия равно изменению температуры в Кельвинах. |
| Кипяток | Вода, которая при нормальном атмосферном давлении имеет температуру в 100 о С. |
| Объем воды 5 л | m = 5 кг, так как: m = ρ V =10 3 · 5 · 10 − 3 м 3 = 5 к г Внимание! Равенство V (л) = m (кг) справедливо только для воды. |
Пример №1. Какое количество теплоты нужно сообщить льду массой 2 кг, находящемуся при температуре –10 о С, чтобы превратить его в воду и нагреть ее до температуры +30 о С?
Можно выделить три тепловых процесса:
- Нагревание льда до температуры плавления.
- Плавление льда.
- Нагревание воды до указанной температуры.
Поэтому количество теплоты будет равно сумме количеств теплоты для каждого из этих процессов:
Q = Q 1 + Q 2 + Q 3
Q = c л m ( 0 − t 1 ) + λ m + c в m ( t 2 − 0 )
Удельные теплоемкости и удельную теплоту плавления смотрим в таблицах:
- Удельная теплоемкость льда = 2050 Дж/(кг∙К).
- Удельная теплоемкость воды = 4200 Дж/(кг∙К).
- Удельная теплота плавления льда = 333,5∙10 3 Дж/кг.
Q = 2050 · 2 ( 0 − ( − 10 ) ) + 333 , 5 · 10 3 · 2 + 4220 · 2 · 30 = 961200 ( д ж ) = 961 , 2 ( к Д ж )
Уравнение теплового баланса
Суммарное количество теплоты, которое выделяется в теплоизолированной системе равно количеству теплоты (суммарному), которое в этой системе поглощается.
Математически уравнение теплового баланса с учетом знаков количества теплоты записывается так:
Q о т д = − Q п о л
Отданное количество теплоты меньше нуля (Qотд 0).
Подсказки к задачам на уравнение теплового баланса
| Теплообмен происходит в калориметре | Потерями энергии можно пренебречь. |
| Жидкость нагревают в некотором сосуде | Начальные и конечные температуры жидкости и сосуда совпадают. |
| В жидкость опускают термометр | Через некоторое время он покажет конечную температуру жидкости и термометра. |
| Мокрый снег | Содержит воду и лед при 0 о С. Учтите, что лед плавится, если он находится при температуре 0 о С и получает энергию от более нагретого тела. Вода кристаллизируется при температуре 0 о С, если она отдает энергию более холодному телу. Если лед и вода находятся при температуре 0 о С, то никаких агрегатных переходов между ними не происходит. |
Частные случаи теплообмена
| В воду комнатной температуры бросили ком снега, содержащий некоторое количество воды, после чего установилась некоторая положительная температура. | 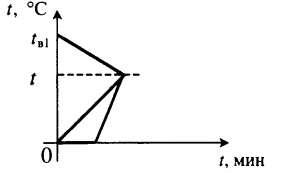 Уравнение теплового баланса: Уравнение теплового баланса:Q 1 + Q 2 + Q 3 = 0 c в m в 1 ( t − t в 1 ) + c в m в 2 ( t − 0 ) + λ m л + c в m л ( t − 0 ) = 0 | ||||||||||||||
| Для получения некоторой положительной температуры воды используют горячую воду и лед, имеющий отрицательную температуру. | 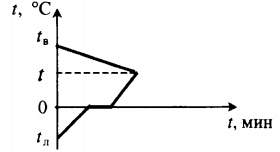 Уравнение теплового баланса: Уравнение теплового баланса:c в m в ( t − t в ) + c л m л ( 0 − t л ) + λ m л + c в m л ( t − 0 ) = 0 | ||||||||||||||
| В воду комнатной температуры бросают раскаленное твердое тело, в результате часть воды испаряется. | 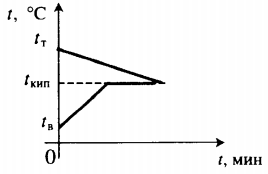 Уравнение теплового баланса: Уравнение теплового баланса:c т m т ( 100 − t т ) + c в m в ( 100 − t в ) + r m п = 0 | ||||||||||||||
| Воду комнатной температуры нагревают до кипения, вводя пар при t = 100 о С. | 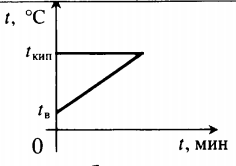 Уравнение теплового баланса: Уравнение теплового баланса:− r m п + c в m в ( 100 − t в ) = 0 | ||||||||||||||
| Лед, имеющий температуру плавления, нагревают до положительной температуры, вводя пар при t = 100 о С. | 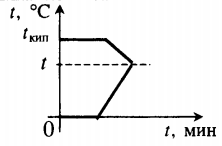 Уравнение теплового баланса: Уравнение теплового баланса:− r m п + c в m п ( t − t к и п ) + λ m л + c в m л ( t − t п л ) = 0 Пример №2. В кастрюлю, где находится вода объемом 2 л при температуре 25 о С, долили 3 л кипятка. Какая температура воды установилась? Количество теплоты, отданное кипятком, равно количеству теплоты, принятому более прохладной водой. Поэтому: c m 1 ( t − t 0 ) = − c m 2 ( t − t к и п ) m 1 ( t − t 0 ) = − m 2 ( t − t к и п ) m 1 t + m 2 t = m 1 t 0 + m 2 t к и п ( m 1 + m 2 ) t = m 1 t 0 + m 2 t к и п t = m 1 t 0 + m 2 t к и п m 1 + m 2 . . t = 2 · 25 + 3 · 100 2 + 3 . . = 350 5 . . = 70 ( ° C ) Взаимные превращения механической и внутренней энергииЕсли в тексте задачи указан процент одного вида энергии, перешедший в другой, то он указывается в виде десятичной дроби перед этой энергией, которой тело обладало вначале. Частные случаи закона сохранения энергии
|
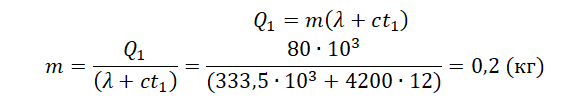
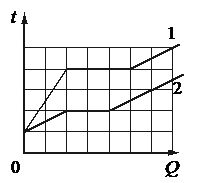 На рисунке представлены графики зависимости температуры t двух тел одинаковой массы от сообщённого им количества теплоты Q. Первоначально тела находились в твёрдом агрегатном состоянии.
На рисунке представлены графики зависимости температуры t двух тел одинаковой массы от сообщённого им количества теплоты Q. Первоначально тела находились в твёрдом агрегатном состоянии.