ChemStudy
Рефераты и курсовые по химии
Водород
8. Взаимодействие метана с водяным паром (разложение метана).
Метан взаимодействует с водяным паром в присутствии соответствующих катализаторов при нагревании (1100 °С) по уравнению
СН4 + Н2Опар + 204 кДж (при постоянном давлении).
Необходимое для реакции тепло следует подводить или извне, или применяя “внутреннее сгорание”, т. е. подмешивая воздух или кислород таким образом, чтобы часть метана сгорала до диоксида углерода курс обучения английскому языку в Москве
СН4 + 2 О2 = СО2 + 2 Н2Опар + 802 кДж (при постоянном давлении).
При этом соотношение компонентов выбирают с таким расчётом, чтобы реакция в целом была экзотермичной
12 СН4 + 5 Н2Опар + 5 О2 = 29 Н2 + 9 СО + 3 СО2 + 85,3 кДж.
Из монооксида углерода посредством “конверсии СО” также получают водород. Удаление диоксида углерода производят вымыванием водой под давлением. Получаемый методом разложения метана водород используют главным образом при синтезе аммиака и гидрировании угля.
9. Взаимодействие водяного пара с фосфором (фиолетовым).
2 Р + 8 Н2О = 2 Н3РО4 + 5 Н2.
Обычно процесс проводят таким образом: пары фосфора, получающиеся при восстановлении фосфата кальция в электрической печи, пропускают вместе с водяным паром над катализатором при 400-600 °С (с повышением температуры равновесие данной реакции смещается влево). Взаимодействие образовавшейся вначале Н3РО4 с фосфором с образованием Н3РО3 и РН3 предотвращают быстрым охлаждением продуктов реакции (закалка). Этот метод применяют прежде всего, если водород идёт для синтеза аммиака, который затем перерабатывают на важное, не содержащее примесей удобрение — аммофос (смесь гидро- и дигидрофосфата аммония).
10. Электролитическое разложение воды.
Чистая вода практически не проводит тока, поэтому к ней прибавляются электролиты (обычно КОН). При электролизе водород выделяется на катоде. На аноде выделяется эквивалентное количество кислорода, который, следовательно, в этом методе является побочным продуктом.
Получающийся при электролизе водород очень чист, если не считать примеси небольших количеств кислорода, который легко удалить пропусканием газа над подходящими катализаторами, например над слегка нагретым палладированным асбестом. Поэтому его используют как для гидрогенизации жиров, так и для других процессов каталитического гидрирования. Водород, получаемый этим методом довольно дорог.
Физические свойства. Водород (т. пл. -259, т. кип. -253 °С) — бесцветный газ, не имеющий запаха. В воде он растворяется незначительно — 2:100 по объёму. Для него характерна растворимость в некоторых металлах.
ЛОМБАРДЫ , кредитные учреждения, предоставляющие ссуды под залог движимого имущества; впервые учреждены в 15 в. во Франции ростовщиками, выходцами из Ломбардии.
АДРИАН Коринфский (ум . 251), христианский мученик, пострадавший в Коринфе в гонение императора Деция. Память в Православной церкви 17 (30) апреля.
УГОЛИНИ (Ugolini) Амедео (1896-1954) , итальянский писатель. Участник Движения Сопротивления. Представитель неореализма. Сборник новелл «Десять поэм в прозе» (1949), романы «Один, как и все» (1946) и «На десять сольди табака» (1950) посвящены Движению Сопротивления.
Конверсия метана с целью получения водорода.
Метод конверсии состоит в окислении метана водяным паром или кислородом по следующим основным реакциям:
CH4 + H2O 
CH4 + CO2 
CH4 + ½O2 
CH4 + 2O2 
CO + H2O 
Выбор окислителей определяется экономичностью процесса. Полное превращение метана практически достигается при температуре выше 1200°C. В избытке водяного пара протекает следующая реакция:
CH4 + 2H2O 
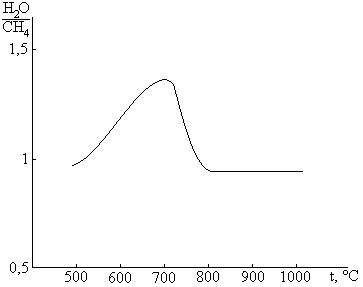
При низких температурах реакция (1) смещается влево, а (5) – вправо. Значит, в конечной газовой фазе будет находиться большое количество CH4. При высоких температурах наоборот – большое количество CO. Отсюда одноступенчатый процесс (6) невыгоден, и процесс проводят в 2 стадии: (1) + (5).
I стадия – окисление CH4.
Эта стадия может протекать гомогенно и гетерогенно (в присутствии катализатора). Механизм гомогенной конверсии метана может заключаться во взаимодействии пара как с метаном, так и с продуктами его разложения.
В присутствии кислорода
Эти реакции протекают при t > 1000°C.
В условиях гетерогенно-каталитического процесса значительно снижается температура процесса. В этом случае механизм следующий:
CH4 
C + H2O 
CH4 + H2O 
Лучшими катализаторами для реакции конверсии является никелевый катализатор, нанесённый на оксид алюминия и промотированный MgO и Cr2O3. Однако этот катализатор чувствителен к соединениям серы. Расход пара в присутствии катализатора происходит по стехиометрии, и не происходит выделение углерода.
II стадия – окисление окиси углерода.
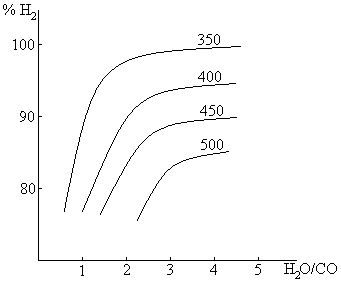
Реакция (5) – равновесная и с увеличением температуры смещается влево. Однако, увеличивая концентрацию водяного пара, смещают реакцию вправо. Зависимость % выхода H2 от соотношения H2O/CO доказывает это
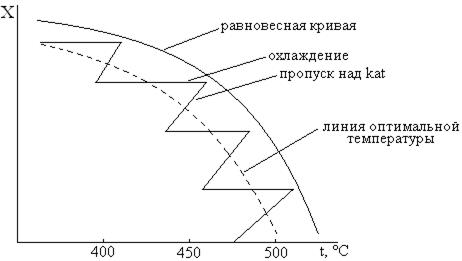
Эта реакция не зависит от давления, и этот метод увеличения скорости реакции здесь неприменим. Более того, реакция (5) протекает с выделением тепла, и проведение реакции в 1 ступени приводит к повышению температуры и смещению равновесия влево. Поэтому реакцию проводят в несколько ступеней, при которых происходит следующая последовательность: пропускание реакционной смеси над катализатором – охлаждение для смещения равновесия вправо и закаливания смеси, и цикл повторяют.
На данной стадии для быстрого установления равновесия смесь пропускают над катализатором.
Железохромовый катализатор, промотированный оксидами Al, K, Ca, обеспечивает достаточную степень конверсии CO при 450-500°C – 96-98%. Цинк-хром-медный катализатор обеспечивает конверсию остаточного содержимого CO 0,2-0,4%, работает при 200-300°C, но очень чувствителен к ядам.
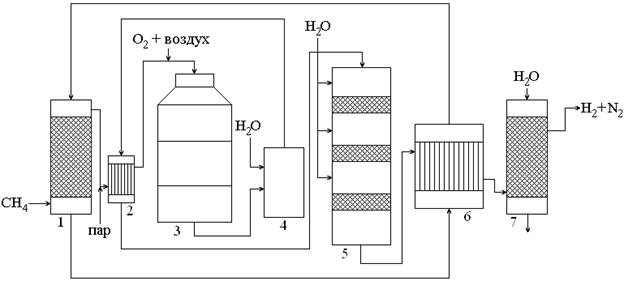
Схема процесса конверсии метана следующая
1. Природный газ с содержанием CH4 – 97% поступает в сатуратор (1), где нагревается до 80°C и насыщается водяным паром, затем поступает в теплообменник (2).
2. В теплообменнике (2) газ нагревается до 500°C отходящими конверторными газами, смешивается с кислородом или воздухом и подаётся в конвертор (3).
3. В конверторе (3) сначала идут экзотермические реакции:
CH4 + ½O2 
CH4 + 2O2 
и температура повышается до 1000°C. Затем протекают эндотермические реакции:
CH4 + H2O 
CH4 + CO2 
Конвертированный газ содержит H2 – 51-54%, N2 (если подавали воздух) – 20%, CO – 20%, CO2 – 7%, CH4 – 0,5%.
4. Затем газ увлажняется в увлажнителе (4), охлаждается до 400-500°C в теплообменнике (2) и поступает в конвертор CO (5).
5. В конверторе CO (5) газ проходит ряд тарелок с катализатором, охлаждаясь между ними конденсатом.
6. Далее проходит через теплообменник (6).
7. И в промывной башне (7) очищается от твёрдой части и от CO, CO2, O2 методом последовательной конденсации.
В итоге получается либо чистый водород в случае использования для конверсии метана чистого кислорода, либо азото-водородная смесь, если используют в качестве окислителя воздух.
Дата добавления: 2015-06-17 ; просмотров: 6559 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. источники: http://helpiks.org/3-88554.html http://acetyl.ru/f/r512.php |