Хлорид натрия: способы получения и химические свойства
Хлорид натрия NaCl — соль щелочного металла натрия и хлороводородной кислоты. Белое кристаллические вещество. Плавится и кипит без разложения. Умеренно растворяется в воде (гидролиза нет);
Относительная молекулярная масса Mr = 58,44; относительная плотность для ж. и тв. состояния d = 2,165; tпл = 800,8º C; tкип = 1465º C;
Способ получения
1. Хлорид натрия можно получить путем взаимодействия натрия и разбавленной хлороводородной кислоты, образуются хлорид натрия и газ водород:
2Na + 2HCl = 2NaCl + H2↑.
2. При комнатной температуре, в результате взаимодействия натрия и хлора, образуется хлорид натрия:
2Na + Cl2 = 2NaCl
3. Концентрированный раствор гидроксида натрия реагирует с концентрированным раствором хлорида аммония при кипении. При этом образуются хлорид натрия, газ аммиак и вода:
NaOH + NH4Cl = NaCl + NH3↑ + H2O
4. При взаимодействии с разбавленной и холодной хлороводородной кислотой пер окси д натрия образует хлорид натрия и пероксид водорода:
5. Разбавленная хлороводородная кислота реагирует с гидроксидом натрия . Взаимодействие хлороводородной кислоты с гидроксидом натрия приводит к образованию хлорида натрия и воды:
NaOH + HCl = NaCl + H2O
6. В результате взаимодействия сульфата натрия и хлорида бария образуется сульфат бария и хлорид натрия:
Качественная реакция
Качественная реакция на хлорид натрия — взаимодействие его с нитратом серебра, в результате реакции происходит образование белого творожного осадка:
1. При взаимодействии с нитратом серебра , хлорид натрия образует нитрат натрия и осадок хлорид серебра:
NaCl + AgNO3 = NaNO3 + AgCl↓
Химические свойства
1. Хлорид натрия вступает в реакцию со многими сложными веществами :
2.1. Хлорид натрия взаимодействует с кислотами :
2.1.1. Хлорид натрия в твердом состоянии при кипении реагирует с концентрированной серной кислотой с образованием сульфата натрия и газа хлороводорода:
а если температуру опустить до 50º С, то твердый хлорид натрия и концентрированная серная кислота образуют гидросульфат натрия и газ хлороводород:
2.2. Хлорид натрия способен вступать в реакцию обмена со многими солями :
2.2.1. Твердый хлорид натрия реагирует с концентрированной и горячей серной кислотой и твердым перманганатом калия . Взаимодействие хлорида натрия с перманганатом калия и серной кислотой приводит к образованию сульфата марганца, натрия, калия, газа хлора и воды:
2.2.2. Хлорид натрия взаимодействует с гидросульфатом натрия при температуре 450–800º C . При этом образуются сульфат натрия и хлороводородная кислота:
2.2.3. При взаимодействии холодного хлорида натрия с насыщенным нитритом серебра выделяются нитрат натрия и осадок хлорид серебра:
NaCl + AgNO2 = NaNO2 + AgCl↓
Please wait.
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 6e0df9b229080c36 • Your IP : 85.95.188.35 • Performance & security by Cloudflare
Состав хлорида натрия (NaCl), свойства, применение, токсичность
хлорид натрия, также называемая поваренной солью или поваренной солью, представляет собой бинарную неорганическую соль натрия щелочного металла и галогена хлора. Это самый большой компонент пищевой соли, а его минеральная форма известна как галит. Молекулярная формула NaCl, и описывает стехиометрическое соотношение его ионов (Na + Cl — ), а не у дискретной молекулы (Na-Cl)
Хлорид натрия представляет собой кристаллическое белое твердое вещество, которое образуется в результате сочетания натрия, серебристо-белого металла, который бурно реагирует с водой, и элемента хлора, ядовитого, едкого, бледно-зеленого газа..
На верхнем изображении показана часть кристаллов NaCl. Как это возможно, что два элемента столь же опасны, как Na и Cl2, может образовываться пищевая соль? Во-первых, химическое уравнение его образования:
Ответ заключается в природе ссылки в NaCl. Будучи ионным, свойства Na + и Cl — они по диагонали отличаются от их нейтральных атомов.
Натрий является жизненно важным элементом, но в его ионной форме. На + является основным внеклеточным катионом с концентрацией приблизительно 140 мг-экв / л, и вместе с сопровождающими его анионами Cl — и HCO3 — (бикарбонат), в основном ответственны за величину осмолярности и внеклеточного объема.
Кроме того, Na + отвечает за генерацию и проведение нервных импульсов в нейрональных аксонах, а также за инициацию сокращения мышц.
NaCl использовался с древних времен для придания аромата пище и сохранения мяса благодаря его способности уничтожать бактерии и предотвращать порчу.
Это также необходимо для производства гидроксида натрия (NaOH) и молекулярного хлора (Cl2) путем взаимодействия NaCl с водой при гидролизе:
В катоде (-) Н накапливается2 (г) и NaOH. Между тем Cl накапливается на аноде (+)2 (G). Гидроксид натрия используется при производстве мыла и хлора при производстве пластика ПВХ.
- 1 Структура хлорида натрия
- 1.1 Унитарная ячейка
- 2 свойства
- 2.1 Молекулярная формула
- 2.2 Молекулярный вес
- 2.3 Физическое описание
- 2,4 Цвет
- 2.5 Вкус
- 2.6 Точка кипения
- 2.7 Точка плавления
- 2.8 Растворимость в воде
- 2.9 Растворимость в органических растворителях
- 2.10 Плотность
- 2.11 Давление пара
- 2.12 Стабильность
- 2.13 Разложение
- 2.14 Вязкость
- 2.15 Коррозия
- 2,16 рН
- 3 использования
- 3.1 В еду
- 3.2 Промышленное использование
- 3.3 Дома
- 3.4 Другое использование
- 3.5 Терапевтическое использование
- 4 Токсичность
- 4.1 Проглатывание
- 4.2 Раздражение и физический контакт
- 5 ссылок
Структура хлорида натрия
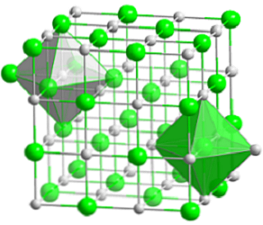
Компактная кубическая структура хлорида натрия представлена на верхнем рисунке. Объемные зеленые сферы соответствуют анионам Cl — , в то время как белый, к катионам Na + . Обратите внимание, что кристалл NaCl состоит из сети ионов, упорядоченных по электростатическим взаимодействиям в соотношении 1: 1..
Хотя столбцы показаны на изображении, связи не ковалентные, а ионные. Использование столбцов полезно при отображении координационной геометрии вокруг иона. Например, в случае NaCl каждый Na + окружен шестью Cl — (белый октаэдр), и каждый Cl — из шести Na + (зеленый октаэдр).
Следовательно, он имеет координацию (6,6), номера которой указывают, сколько соседей окружает каждый ион. Число справа указывает на соседей Na + , в то время как слева — .
Другие представления опускают использование полос, чтобы выделить октаэдрические отверстия, которые имеет структура, которые являются результатом межузельного пространства между шестью анионами Cl. — (или катионы Na + упаковано. Такое расположение наблюдается в других моно (MX) или многоатомных неорганических солях и называется солью драгоценного камня..
Унитарная ячейка
Элементарная ячейка каменной соли является кубической, но какие именно кубы точно представляют ее на изображении выше? Октаэдры дают ответ. Оба покрывают в общей сложности четыре маленьких кубика.
У этих кубиков есть части ионов в их вершинах, краях и гранях. Соблюдая осторожность, ион Na + он расположен в центре и двенадцать из них по краям. Ион на одном ребре может быть разделен на четыре куба. Таким образом, есть 4 иона Na + (12 × 1/4 + 1 = 4).
Для ионов Cl — , восемь расположены в вершинах и шесть по краям. Поскольку ионы, расположенные в вершинах, делят пространство с восемью другими кубами, а на краях с шестью, они имеют 4 иона Cl — (8 × 1/8 + 6 × 1/2 = 4).
Предыдущий результат интерпретируется следующим образом: в элементарной ячейке NaCl имеется четыре катиона Na + и четыре Cl-аниона — ; пропорция, которая соответствует химической формуле (Na + для каждого Cl — ).
http://gomolog.ru/reshebniki/9-klass/eremin-2019/42/4.html
http://ru.thpanorama.com/articles/qumica/cloruro-de-sodio-nacl-estructura-propiedades-usos-toxicidad.html