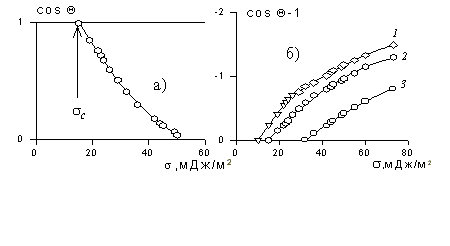2.3.2. Смачивание и растекание на границе твердое тело – жидкость – газ
В большинстве случаев жидкость на поверхности твердого тела остается в виде капли, большей или меньшей толщины, контактирующей с твердым телом под определенным углом, который называется краевым углом смачивания и обозначается буквой Q (рис. 1.24). Растекание капли по поверхности прекратится при достижении равновесия, которое без учета сил тяжести может быть описано уравнением Юнга:

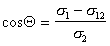
где индексы 1, 2, 3 – обозначают, соответственно, твердую, жидкую и газовую фазы.
Работа адгезии выражается уравнением Дюпре:
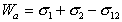
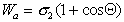
Рис. 1.24. Капля жидкости на поверхности твердого тела (схема)
Работа адгезии при 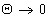
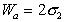
Следует помнить, что определение работы адгезии в реальных системах предполагает равновесие фаз, насыщенных относительно друг друга.
Кроме того, твердая поверхность, по которой происходит растекание жидкости, не свободна. Она обычно покрыта пленкой вещества, адсорбированного из газо-паровой фазы. Эта пленка имеет поверхностное давление p, поэтому
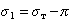
Смачивание неоднородных, пористых или шероховатых поверхностей сопровождается запиранием пузырьков воздуха в неровностях. В результате этого краевые углы смачивания сухой и предварительно увлажненной поверхностей различаются. Такое явление носит название «гистерезис смачивания». Гистерезис смачивания проявляется также при загрязнении поверхности, в результате чего она становится неоднородной при закреплении на ней твердых частиц или жировых пленок. В этом случае поверхность ведет себя как составная.
Шероховатость поверхности учитывается введением коэффициента шероховатости r, представляющего отношение площади поверхности реального тела к площади идеально гладкой поверхности, тогда
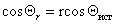
Можно отметить, что если краевой угол смачивания гладкой поверхности, например полимерной пленки, меньше 90 o , то шероховатость (ткань из волокон этого полимера) уменьшает его, если же он больше 90 o , то шероховатость его увеличивает. Для составной поверхности, которая специфична для большинства текстильных материалов, наличие участков различной природы может быть учтено введением коэффициентов x, характеризующих долю поверхности с различными свойствами. Например, если текстильный материал изготовлен из волокон двух видов 1 и 2, то
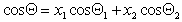
Если переплетение нитей таково, что получается сетчатый или дырчатый материал, то уравнение (2.50) принимает вид
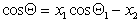
где х2 – доля открытой поверхности.
Как мы обсуждали выше, поверхностное натяжение можно разделить на компоненты дисперсионных и полярных сил, а при нахождении межфазового натяжения для многих жидких границ можно ограничиться лишь дисперсионной составляющей. Такое ограничение позволяет провести обсуждение явления смачивания (по крайней мере, низкоэнергетических поверхностей, к каковым можно отнести подавляющее большинство волокнообразующих полимеров), в рамках теории дисперсионных сил.
Как показал Н. В. Чураев смачивание неполярной жидкостью твердой поверхности возможно, если будет соблюдаться условие смачивания, которое выражается уравнением
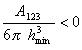
где А123 – составная постоянная Гамакера при взаимодействии жидкости (фаза 2) с твердым телом (фаза 1) на границе с воздухом (фаза 3); hmin — наименьшая толщина пленки, которая фактически соответствует Ван-дер-Ваальсову расстоянию, т.е. hmin = (0,22¸0,24) нм. Например, для воды на поверхности тефлона А123 = -7·10 — 21 Дж.
Учет только дисперсионных сил приводит к уравнению
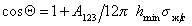
При расчетах углов смачивания твердых поверхностей следует учитывать поверхностное давление пленки, образованной при адсорбции из газо-паровой фазы. Тогда с учетом уравнения (1.2.48), уравнение Юнга (1.2.45) следует записать в виде
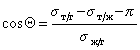
Способ расчета поверхностного давления предложили Бэнгхэм и Разорук:
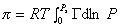
где P – равновесное давление, Г– равновесная адсорбция газа (пара), Ps – давление насыщения.
При больших углах смачивания и слабом взаимодействии жидкости с твердым телом поверхностное давление обычно не учитывают.
Для неполярных жидкостей на низкоэнергетической поверхности твердого тела для работы адгезии было получено выражение
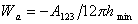
Поэтому уравнение Дюпре (1.2.46) можно записать
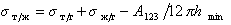
Для дисперсионной составляющей жидкости
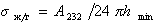
где А232 – постоянная Гамакера взаимодействия жидкости через прослойку газа (пара).
Сочетая уравнения (1.2.47), (1.2.55) и (1.2.56), получаем
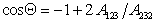
Очевидно, что Q = 0, т.е. при полном смачивании, cosQ = 1, если
Уравнение (1.2.57) позволяет прогнозировать вероятность смачивания (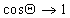
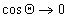
Чаще, однако, прибегают к определению постоянной Гамакера по известному значению межфазового натяжения на границе «твердое тело — газ». Эту характеристику поверхности твердого тела находят при распространении подхода Джирифалько и Гуда, рассмотренного нами выше для границы двух жидкостей, на поверхность раздела «жидкость — твердое тело», уравнения (1.2.23), (1.2.35).
Так приложение уравнения (1.2.34) к уравнению Юнга для случая смачивания неполярной жидкостью поверхности полимерного материала позволяет получить уравнение, известное как уравнение Фоукса, при
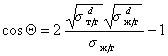
Если жидкости неполярны и 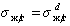
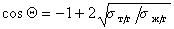
Уравнение (1.2.59) Зисман предложил использовать для определения поверхностного натяжения твердых тел. Очевидно, что при 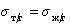
Естественно, что метод Зисмана ограничен некоторыми условиями, в частности, из уравнения (1.2.57) следует, что полное смачивание возможно при дисперсионной неразличимости твердого тела и жидкости, т.е. при А232= А123.
В действительности такого условия никогда невозможно достигнуть хотя бы потому, что если жидкость и твердое тело будут иметь одинаковый химический состав, их постоянные Гамакера будут различаться из-за различий в плотности.
Другое ограничение, связанное с применением метода Зисмана, основано на том, что использовать для измерения краевых углов смачивания следует лишь неполярные жидкости. Наиболее целесообразно применять гомологические ряды жидкостей. При величине поверхностного натяжения жидкостей более 35 мДж/м 2 метод Зисмана уже дает высокую погрешность, так как необходимо учитывать вклад полярных сил, которые в отличие от дисперсионной составляющей могут иметь и отрицательное значение. С другой стороны, приложение для смачивания твердых тел полярными жидкостями уравнения Ву (1.2.36) позволяет рассчитать полярную составляющую поверхностного натяжения жидкости, если для одной из неполярных жидкостей измерить краевой угол смачивания. Для расчета используют уравнение
Рис. 1.25. Зависимость смачивания поверхностей от поверхностного натяжения жидкостей. Материал поверхности: 1- FC-721; 2- ПТФЭ (тефлон); 3 — полиэтилен
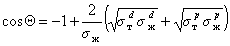
Этот метод позволил разделить величину поверхностного натяжения жидкостей на полярную и дисперсионную компоненты и определить поверхностное натяжение многих волокнообразующих полимеров.
Пример зависимости косинуса угла смачивания поверхности пленок различными жидкостями приведен на рис.1.25. Для описания этих зависимостей Зисман предложил использовать эмпирическое уравнение
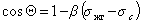
где bэмпирическая постоянная, sс – «критическое» поверхностное натяжение твердого тела, при котором происходит полное смачивание твердого тела жидкостью. Очевидно, что cos Q =1 при условии sжг = sс .
Как мы обсуждали выше, этот критерий в известной мере является условным, хотя и отражает энергетическое состояние поверхности твердого тела.
Реальное значение поверхностного натяжения твердого тела экспериментально определить невозможно, также как и рассчитать его теоретически. В этой связи метод Зисмана нашел широкое применение в практике исследования полимерных материалов, а также полимерных покрытий тканей, используемых в качестве отделочных материалов
Коллоидная химия: смачивание. смачивание. Тема Смачивание
| Название | Тема Смачивание |
| Анкор | Коллоидная химия: смачивание |
| Дата | 16.10.2021 |
| Размер | 160.8 Kb. |
| Формат файла |  |
| Имя файла | смачивание.pptx |
| Тип | Документы #248889 |
Подборка по базе: 5 тема .docx, Поліщук Роман Тема 37-Подагра.ppt, Эссе. Тема 8. Сергеева М..docx, Семинар. Тема 11. Право собственности (общие положения).docx, ВПП Тема 7 Занятие 2.doc, СР Тема 1.1..docx, Вопросы для СК тема 1 БОХ. Натточеева, 139 группа. (1).docx, Занятия в ТДК тема 4.docx, Раздел 3. Тема 1. Конфликт. Способы решения конфликтных ситуаций, Вопросы для СК тема 1 БОХ.docxТема 3. СмачиваниеЗадачи:
В гетерогенных системах различают
СМАЧИВАНИЕ Пример: капля жидкости, нанесенная на поверхность твердого тела (существует явление смачивания одной жидкости другой). При этом могут наблюдаться два крайних случая: 1 случай. Капля жидкости самопроизвольно растекается на поверхности, пока не покроет всю поверхность или пока слой жидкости не станет мономолекулярным. Это полное смачивание. Пример: капля воды на обезжиренном стекле. 2 случай. Капля жидкости на твердой поверхности самопроизвольно принимает почти сферическую форму. Твердая поверхность не смачивается жидкостью, наблюдается полное несмачивание. Пример: капля ртути на неметаллической поверхности. Существуют различные промежуточные случаи, когда поверхность частично смачивается жидкостью. Мера смачивания — краевой угол Ө, или угол смачивания. Краевой угол (Ө) — угол, который образует капля с поверхностью твердого тела со стороны жидкости. Это угол между твердой поверхностью и касательной в точке соприкосновения фаз (угол всегда измеряют со стороны жидкости). Рис. 1. Различные случаи неполного смачивания. На рис. 1 показаны капли, образующие с поверхностью краевые углы Ө 90°. Если вода на твердой поверхности образует Ө 90°, поверхность — гидрофобная. Значения краевого угла, образуемого водой на поверхности различных твердых тел в атмосфере воздуха: кварц — 0°; малахит — 17°; графит — 55-60°; тальк — 69°; сера — 78°; парафин — 106°; фторопласт — 108°. Чем больше краевой угол, тем в меньшей степени жидкость смачивает поверхность твердого тела. Степень смачивания, значит, и краевой угол зависят от соотношения величин поверхностного натяжения на границах: воздух-твердое тело Өтв.г, жидкость-твердое тело Өтв.ж и воздух-жидкость Өж.г. Обозначим поверхности натяжения на границах раздела фаз: σ1,3 — твердое тело-жидкость; Силы σ1,2 и σ1,3 стремятся уменьшить размеры капли и придать ей форму шара. σ2,3 — наоборот, стремятся растянуть каплю, за счет взаимодействия с ней. Рис. 2. К выводу уравнения для краевого угла (уравнение Юнга). При образовании равновесного краевого угла (капля приняла форму) все силы должны уравновешивать друг друга. При этом силы σ1,3 и σ2,3 действуют в плоскости поверхности твердого тела, а вместо силы σ1,2 нужно взять ее проекцию на плоскость, т.к. точка приложения сил может только передвигаться на поверхности и не может от нее оторваться. Это II закон Лапласа или уравнение Юнга. поверхность — гидрофобная (олеофильная). В системе из 2-х жидкостей и твердого тела его поверхность будет смачивать та жидкость, полярность которой ближе к полярности твердого тела, или у которой разность полярностей меньше. Смачивающая способность лучше у той жидкости, у которой σ меньше.
Теплота смачивания Теплота смачивания — теплота, выделяющаяся при взаимодействии жидкости с поверхностью другой жидкости или твердого тела. Дифференциальная и интегральная теплоты смачивания зависят от количества жидкости, смачивающей поверхность того или иного тела. Поле поверхностных сил проникает внутрь смачивающей жидкости на определенную глубину, равную толщине поверхностного слоя в фазе этой жидкости. Потенциал поля снижается от максимального значения на границе раздела фаз до нуля на границе поверхностного слоя внутри смачивающей жидкости. H2 — после смачивания; Дифференциальная теплота смачивания λd. λd — теплота, выделившаяся при добавлении бесконечно малого количества жидкости на поверхность при данном заполнении х (при данном количестве смачивающей жидкости, нанесенной на единицу поверхности) и рассчитанную на единицу количества (на 1 моль) жидкости. λd характеризует поле поверхностных сил в данной точке или в данном сечении, находящихся на определенном расстоянии от границы раздела фаз. Она снижается по мере удаления от смачиваемой поверхности, т.е. от источника поверхностных сил. При нанесении жидкости на поверхность в малых количествах добавление каждой последующей порции сопровождается выделением все меньшего количества теплоты. Максимальное значение λd соответствует границе раздела фаз, т.е. значению, получаемому при экстраполяции к нулевому количеству нанесенной жидкости. Минимальное значение (0) соответствует моменту полной компенсации поверхностной энергии энергией взаимодействия жидкости с поверхностью. Интегральная теплота смачивания λi . λi — теплота, выделяющаяся при нанесении какого-то количества жидкости х на единицу площади поверхности. Чем большее количество жидкости взаимодействует с поверхностью, тем больше λi. Интегральная теплота смачивания связана с дифференциальной соотношением: Интегральную теплоту смачивания при нанесении жидкости, взятой с избытком, который уже не взаимодействует с поверхностью, называют полной или просто теплотой смачивания. Для ее определения интеграл берется от нуля до бесконечности. Рис. 3. Зависимость интегральной λi и дифференциальной λd теплот смачивания от количества нанесенной жидкости. Чем больше смачивающей жидкости, тем меньше λd и больше λi . В пределе, когда избыточное количество жидкости уже не взаимодействует с поверхностью, λd = 0, а λi = полной теплоте смачивания (ΔQ). При малых количествах жидкости, пока вся эквипотенциальная поверхность не покрыта монослоем, λd = const. При смачивании реальных твердых тел, поверхность которых не является эквипотенциальной, λd снижается с самых первых порций жидкости, так как в первую очередь с жидкостью взаимодействуют наиболее активные участки поверхности. Интегральная теплота смачивания измеряется количеством энергии (работы), отнесенной к единице поверхности: Дифференциальная теплота измеряется соответственно (как производная по количеству вещества на единицу поверхности): Если процесс смачивания идет из паровой фазы (смачивание предшествует конденсации пара), то Qi — суммарный тепловой эффект; λконд — теплота конденсации пара; L — теплота смачивания уже конденсированного пара (чистая теплота адсорбции). Работа когезии и работа адгезии. Работа когезии — это работа разрыва между молекулами, находящимися в одной фазе, отнесенная к единице площади поверхности. Работа адгезии — это работа разрыва поверхности между разными фазами, отнесенная к единице площади (Дж/м2). Различают 2 случая: 1) Фазы 1 и 3 — жидкости (взаимно нерастворимые). Уравнение Дюпре: Значения σ1,2 и σ2,3 легко определить экспериментально или по табличным данным. σ1,3 можно рассчитать по уравнению Антонова: где и — поверхностное натяжение 2-х взаимно насыщенных жидкостей на границе с воздухом; — поверхностное натяжение на границе раздела фаз между 2-мя взаимно насыщенными жидкостями.
Уравнение Дюпре (7) для расчета работы адгезии на такой границе фаз трудно определить, т.к. трудно определить поверхностное натяжение твердого тела на границе с воздухом и жидкостью — σ2,3 и σ1,3 . Удобную для расчета этой величины форму дает соотношение, получаемое в результате сочетания уравнения Дюпре (7) с законом Юнга (2): источники: http://topuch.ru/tema-smachivanie/index.html |