Номенклатура жиров
Общее название жиров – триацилглицерины (триглицериды).
Существует несколько способов назвать молекулу жира.
Например, жир, образованный тремя остатками стеариновой кислоты, будет иметь следующие названия:
Физические свойства жиров
Жиры растворимы в органических растворителях и нерастворимы в воде. С водой жиры не смешиваются.
| Животные жиры — предельные | Растительные жиры (масла) — непредельные |
| Твёрдые, образованы предельными кислотами – стеариновой и пальмитиновой. Все животные жиры, кроме рыбьего – твёрдые. | Жидкие, образованы непредельными кислотами – олеиновой, линолевой и другими. Все растительные жиры, кроме пальмового масла – жидкие. |
Химические свойства жиров
1. Гидролиз (омыление) жиров
Жиры подвергаются гидролизу в кислой или щелочной среде или под действием ферментов.
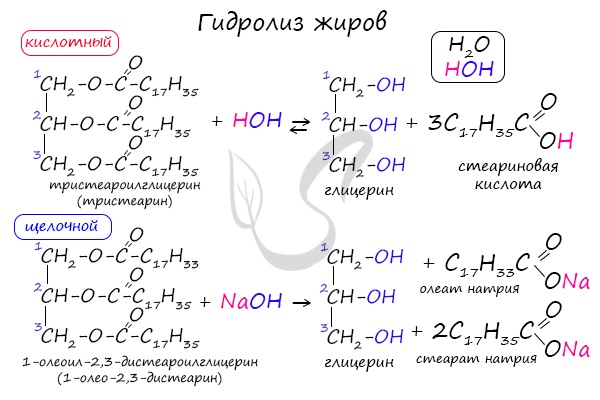
1.1. Кислотный гидролиз
Под действием кислот жиры гидролизуются до глицерина и карбоновых кислот, которых входили в молекулу жира.
| Например, при гидролизе тристеарата глицерина в кислой среде образуется стеариновая кислота и глицерин |
1.2. Щелочной гидролиз — омыление жиров
При щелочном гидролизе жиров образуется глицерин и соли карбоновых кислот, входивших в состав жира.
| Например, при гидролизе тристеарата глицерина гидроксидом натрия образуется стеарат натрия . |
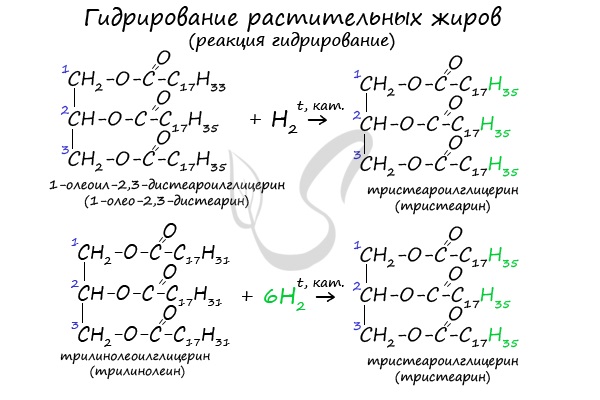
2. Гидрирование (гидрогенизация) ненасыщенных жиров
Гидрогенизация жиров — это процесс присоединения водорода к остаткам непредельных кислот, входящих в состав жира.
При этом остатки непредельных кислот переходят в остатки предельных, жидкие растительные жиры превращаются в твёрдые (маргарин).
| Например, триолеат глицерина при гидрировании превращается в тристеарат глицерина: |
| Количественной характеристикой степени ненасыщенности жиров служит йодное число, показывающее, какая масса йода может присоединиться по двойным связям к 100 г жира. |
3. Мыло и синтетические моющие средства
При щелочном гидролизе жиров образуются мыла – соли высших жирных кислот.
Стеарат натрия – твёрдое мыло.
Стеарат калия – жидкое мыло.
Моющая способность мыла зависит от жесткости воды. Оно хорошо мылится и стирает в мягкой воде, плохо стирает в жёсткой воде и совсем не стирает в морской воде, так как содержащие в ней ионы Ca 2+ и Mg 2+ дают с высшими кислотами нерастворимые в воде соли.
| Например, тристеарат глицерина взаимодействует с сульфатом кальция |
Поэтому наряду с мылом используют синтетические моющие средства.
Их производят из других веществ, например из алкилсульфатов — солей сложных эфиров высших спиртов и серной кислоты.
Спирт реагирует с серной кислотой с образованием алкилсульфата .
Далее алкилсульфат гидролизуется щелочью:
Эти соли содержат в молекуле от 12 до 14 углеродных атомов и обладают очень хорошими моющими свойствами. Кальциевые и магниевые соли этих веществ растворимы в воде, а потому такие мыла моют и в жесткой воде. Алкилсульфаты содержатся во многих стиральных порошках.
Уравнение жир из глицерина и
Жиры — органические соединения, по строению являющиеся сложными эфирами трехатомного спирта глицерина и высших карбоновых (жирных) кислот.
К жирным кислотам (их формулы лучше выучить 😉 относятся:
- Пальмитиновая — C15H31COOH (предельная)
- Стеариновая — C17H35COOH (предельная)
- Олеиновая — C17H33COOH (непредельная, 1 двойная связь в радикале)
- Линолевая — C17H31COOH (непредельная, 2 двойные связи в радикале)
- Линоленовая — C17H29COOH (непредельная, 3 двойные связи в радикале)
Растительные и животные жиры
Жиры образуются в организме растений и животных, служат запасным питательным веществом. В строении растительных и животных жиров есть некоторые важные отличия.
Заметьте, что растительные жиры чаще жидкие и в них входят преимущественно остатки непредельных жирных кислот, а животные жиры — твердые и содержат остатки предельных жирных кислот.
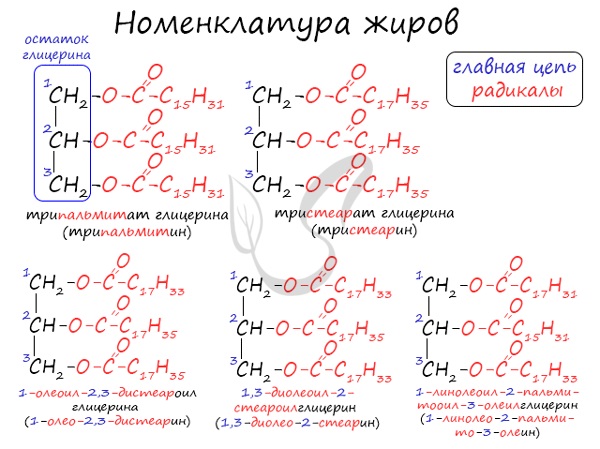
Номенклатура жиров
По систематической номенклатуре жиры принято называть триацилглицеринами. Названия жирам дают в зависимости от ацилов — остатков жирных кислот, входящих в их состав. Для формирования единого названия к остаткам кислот добавляют суффикс «оил».
В соответствии с тривиальной номенклатурой, жиры называют, добавляя окончание «ин» к названию кислоты и приставку, указывая, сколько гидроксогрупп в молекуле глицерина подверглось этерификации. В общем лучше 1 раз увидеть, чем 100 раз услышать 😉
Получение жиров
Жиры (по строению сложные эфиры) получаются в реакции этерификации, протекающей между трехатомным спиртом глицерином и высшими карбоновыми (жирными) кислотами.
В зависимости от того, какие именно кислоты участвуют в реакции, образуются различные жиры.
Химические свойства жиров
- Гидрирование растительных жиров
В состав растительных жиров входят непредельные кислоты, которые поддаются гидрированию и превращаются в предельные. Таким путем в пищевой промышленности получают маргарин.
Как сложные эфиры, жиры способны вступать в реакцию гидролиза, который может быть кислотным и щелочным. В результате кислотного гидролиза образуется глицерин и исходные жирные кислоты, в результате щелочного гидролиза — глицерин и соли жирных кислот.
Реакция щелочного гидролиза жиров называется реакцией омыления, в результате получаются соли жирных кислот — мыла. Кислотный гидролиз протекает обратимо, щелочной — необратимо.
В состав твердого мыла входят соли Na, в состав жидкого — K.
© Беллевич Юрий Сергеевич 2018-2022
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Урок 32. Жиры
Жирами называют сложные эфиры глицерина и высших карбоновых кислот:
где R, R’ и R» – углеводородные радикалы высших карбоновых (жирных) кислот, преимущественно от С3 до С17. Карбоновые кислоты могут быть различными, но всегда нормального строения и, как правило, с четным числом атомов углерода.
Жиры – главная составная часть жировых клеток животных и растений – являются одним из важнейших пищевых резервов организма. При окислении жиров выделяется значительно больше энергии, чем при окислении углеводов и белков.
Три наиболее распространенные в природе жирные кислоты – это предельные кислоты: пальмитиновая (С16), стеариновая (С18) – и непредельная олеиновая (С18) кислота. У большинства ненасыщенных жирных кислот, входящих в состав жиров, масел и биологических мембран, преобладающим является цисизомер, трансизомер встречается редко. Чем выше степень ненасыщенности жирной кислоты, тем ниже ее температура плавления (табл. 16).
Наиболее распространенные в биообъектах жирные кислоты
| Структурная формула | Название | Температура плавления, °С |
|---|---|---|
| СН3(СН2)10СООН СН3(СН2)12СООН СН3(СН2)14СООН СН3(СН2)16СООН СН3(СН2)18СООН | Лауриновая 10 Миристиновая 10 Пальмитиновая 10 Стеариновая 10 Арахиновая | 44 10 58 10 63 10 70 10 77 10 |
| СН3(СН2)5СН=СН(СН2)7СООН СН3(СН2)7СН=СН(СН2)7СООН СН3(СН2)4(СН=СНСН2)2(СН2)6СООН СН3СН2(СН=СНСН2)3(СН2)6СООН СН3(СН2)4(СН=СНСН2)4(СН2)2СООН | Пальмитин-олеиновая 10 Олеиновая 10 Линолевая 10 Линоленовая 10 Арахидоновая | –1 10 16 10 –5 10 –11 10 –49 10 |
Названия жиров. Природные жиры (триацилглицерины) являются триэфирами глицерина и жирных кислот. Обычное название этих соединений – триглицериды. Известны не только глицериды одинаковых кислот (простые глицериды), но и преимущественно разных кислот (смешанные глицериды). Например:
Животные жиры содержат главным образом глицериды предельных кислот и являются твердыми веществами. Растительные жиры, часто называемые маслами, содержат глицериды непредельных карбоновых кислот. Это, например, жидкие подсолнечное, конопляное и льняное масла.
Сельскохозяйственные культуры,
из которых получают растительные масла
Химические свойства жиров




Задача. Напишите структурные формулы всех возможных триглицеридов, образованных остатками (по одному) олеиновой, пальмитиновой и стеариновой кислот.
Решение
Возможны три варианта, различающиеся расположением остатков названных кислот при центральном атоме С-2 глицерина:
УПРАЖНЕНИЯ
1. 2-Олеил-1,3-дистеарилглицерин, содержащийся в кокосовом масле, гидрируют (Н2, Pt) по двойной связи в тристеарин. Напишите уравнение реакции гидрирования. Укажите, какому веществу соответствует температура плавления +43 °С и какому +72 °С.
2. Дайте названия жирам, образованным глицерином и: а) линолевой кислотой;
б) пальмитин-олеиновой кислотой; в) комбинацией этих двух кислот. Приведите их структурные формулы.
3. Какие жирные кислоты образуются при гидролизе 2-линолеил-1,3-диолеилглицерина? Какой другой триацилглицерин дает такие же жирные кислоты и в той же пропорции? Составьте уравнение реакции гидролиза одного из этих жиров.
4. Напишите две возможные формулы жира, имеющего в молекуле 57 атомов углерода и вступающего в реакцию с бромом в мольном соотношении 1:2.
5. При сгорании 1 моль жира образуется 57 моль углекислого газа и 54 моль воды. Напишите две возможные формулы жира, образованного кислотами с четным числом углеродных атомов.
6. Образец жира может вступить в реакцию с 0,4 моль водорода. Продукт гидрирования вступает в реакцию гидролиза с 0,6 моль NaOH, при этом образуется соль только одной кислоты, масса соли равна 183,6 г. Вычислите относительную молекулярную массу жира и приведите одну из возможных его формул.
7. Образец жира вступает в реакцию кислотного гидролиза. Масса продуктов гидролиза на 2,7 г больше массы исходного жира. В результате гидролиза образовалась только одна кислота массой 38,4 г. Вычислите молекулярную масcу жира и приведите одну из возможных его формул.
Ответы на упражнения к теме 2
Урок 32
1.
2.
3.
Другой возможный триацилглицерин:
4. Углеродный состав молекулы жира складывается из трех атомов С глицерина и трех остатков карбоновых кислот Сх, Су, Сz. Причем 3 + х + у + z = 57. Если х = у = z, то 3х = 54, х = 18, или в молекуле кислотной компоненты жира 18 атомов С. Кроме того, в формуле жира должны содержаться две двойные связи:
5. Поскольку из 1 моль жира образуется 57 моль СО2, в молекуле этого жира 57 атомов С (ср. с упражнением 4). Число атомов Н в формуле жира: 2•54 = 108. За вычетом 5 атомов Н остатка глицерина на три остатка кислоты приходится 103 атома Н: 35 + 35 + 33 и др.
Две возможные формулы жира:
6. При гидролизе жиров на связывание образующихся кислот в виде солей расходуется трехкратное мольное количество щелочи. Поэтому 

Расход водорода в реакции гидрирования: 

Молярная масса соли:
М(соли) = m/ 
Подставим значения атомных масс элементов в общую формулу соли СnH2n+1COONa (сумма Аr элементов формулы равна Мr(соли)) и найдем n:
12n + 2n + 1 + 44 + 23 = 306, 14n = 238, n = 17.
Возможная формула жира:
7. Прибавка по массе продуктов гидролиза обусловлена присоединившейся водой. Причем количество вещества воды (в моль) в три раза больше количества вещества гидролизуемого жира: 

А вот количества веществ гидролизной воды и образующейся кислоты одинаковы: 

Проведем необходимые расчеты:

http://studarium.ru/article/191
http://him.1sept.ru/2004/41/17.htm