Смачивание и растекание жидкостей
Смачивание – это поверхностное явление, заключающееся во
взаимодействии жидкости с твердым или другим жидким телом при наличии одновременного контакта трех несмешивающихся фаз, одна из которых обычно является газом (воздухом).
При нанесении капли жидкости на поверхность твердого тела (или другой жидкости) можно наблюдать разные явления. В одном случае нанесенная жидкость сохраняет форму капли, в другом случае капля растекается по поверхности. Рассмотрим первый случай (рис. 9.10)
 |
Рис. 9.10 Смачивание жидкостью твердого тела
Линия соприкосновения трех фаз называется периметром смачивания. Угол q называется краевым углом смачивания. Он отсчитывается со стороны жидкости. Поскольку капля находится в состоянии равновесия, действие сил на нее скомпенсировано. Рассмотрим эти силы. Как известно, силы поверхностного натяжения направлены на сокращение площади контакта фаз по касательной к поверхности. На рис. 9.10 эти силы представлены векторами, выходящими из точки соприкосновения всех трех фаз 0.
sТ-Г – стремиться уменьшить площадь контакта твердого тела с газом, поэтому растягивает пленку жидкости по твердому телу.
sТ-Ж – стремится уменьшить площадь контакта твердого тела с жидкостью, поэтому стягивает каплю жидкости в шарик.
sЖ-Г – стремится уменьшить площадь контакта жидкости с газом, поэтому стягивает каплю жидкости в шарик (шарообразная поверхность имеет наименьшую площадь).
Рассмотрим равнодействующую сил, действующих на каплю в точке 0 вдоль поверхности твердого тела. Это силы поверхностного натяжения sТ-Г, sТ-Ж, а также проекция sЖ-Г на выбранную ось

В состоянии равновесия равнодействующая сил равна 0:
Полученное соотношение (9.16) называется законом Юнга.
Краевой угол смачивания q или cosq являются количественной характеристикой смачивания. Чем меньше угол q и соответственно больше cosq, тем лучше смачивается поверхность.
Закон Юнга позволяет выразить cosq через поверхностные межфазные натяжения:

Сочетание уравнения Дюпре (9.15) с законом Юнга (9.16) позволяет выразить работу адгезии Wa через косинус краевого угла смачивания q.
Из уравнения (9.16) выразим разность
Полученную разность подставим в уравнение 9.15
Уравнение (9.18) называют уравнением Дюпре — Юнга. Оно позволя-ет рассчитать работу адгезии, если известно поверхностное натяжение жидкости и краевой угол смачивания. Обе эти величины сравнительно легко определяются экспериментально: q – путем проектирования капли на экран (с помощью несложной установки) и измерения краевого угла на проекции капли. С помощью уравнения Дюпре – Юнга (9.18) легко найти соотношение между работой когезии смачивающей жидкости и работой адгезии между жидкостью и смачиваемым телом.
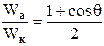
или
С использованием полученных соотношений рассмотрим возможные случаи поведения капли жидкости на твердой поверхности (или на другой жидкости) (табл. 9.4)
Как видно из табл. 9.4 предельным случаем смачивания является растекание жидкости по поверхности, которое наблюдается при нулевом краевом угле смачивания.
Растекание жидкостей по поверхности
Особо остановимся на предельном случае смачивания – растекании жидкости по поверхности, которое наблюдается при q = 0 0 (см. табл. 9.4), когда работа адгезии равна работе когезии (Wa = Wк). Очевидно, что чем больше преобладает работа адгезии над работой когезии, тем лучше будет растекаться жидкость по поверхности. Величина
называется коэффициентом растекания или критерием Гаркинса.
Если f > 0 – жидкость растекается (Wa > Wк)
Если f
Гидрофильность и гидрофобность поверхностей имеет огромное значение в природе, в технологических процессах. Процессами гидрофилизации и гидрофобизации поверхности можно управлять, нанося специальные покрытия (лакокрасочные) или обрабатывая поверхность растворами поверхностно — активных веществ.
В табл. 9.5 приведены значения краевых углов смачивания для некоторых веществ.
Краевые углы смачивания водой некоторых веществ
| Вещество | q | Вещество | q | Вещество | q |
| Кварц | 0 0 | Графит | 55 0 | Парафин | 106 0 |
| Малахит | 17 0 | Тальк | 69 0 | Фторопласт | 108 0 |
Из веществ, приведенных в таблице, гидрофильными свойствами обладают: кварц, малахит, графит, тальк, а гидрофобными – парафин и фторопласт.
Процесс растекания зависит от соотношения работ адгезии и когезии, а те в свою очередь определяются величинами поверхностного натяжения на границе раздела разных фаз.
На основе изложенного можно сделать некоторые общие выводы:
1.Процесс растекания зависит как от s поверхности, по которой происходит растекание, так и от s жидкости, которая растекается.
2.Поверхности, по которым происходит растекание делятся на высокоэнергетические и низкоэнергетические.
Критерии смачивания, несмачивания и
| Несмачивание жидкостью поверхности q > 90 0 (тупой угол) | Смачивание жидкостью поверхности q 0 (острый угол) |
 | |
| предельные случаи | |
| 1) q = 180 0 (полное несмачивание, на практике не встречается) cos180 0 = -1 Wa = 0 | 1) q = 0 0 (полное смачивание, т.е. растекание) cos0 0 = 1 Wa = Wк |
| 2) q = 90 0 (неполное смачивание) cos90 0 = 0 Wa = 1/2Wк | 2) q = 90 0 (неполное смачивание) cos90 0 = 0 Wa = 1/2Wк |
| в общем виде | |
| 90 0 0 -1 0 0 0 2 . s таких поверхностей зависит от твердости и точки плавления веществ (табл. 9.4). Примерами таких веществ служат металлы, оксиды металлов, соли, кварц, стекло, рубин, алмаз. Стремление к понижению свободной поверхностной энергии в таких телах очень велико. Выигрыш в энергии от того, что эта поверхность будет модифицирована за счет адсорбции или просто покрыта другой жидкостью, обычно больше, чем свободная поверхностная энергия большинства органических и неорганических жидкостей на границе их с паром. Поэтому жидкости смачивают высокоэнергетические поверхности и полностью растекаются на них. Например, по поверхности жидкой ртути (s = 475 мДж/м 2 ) растекаются практически все жидкости. Однако, если ртуть загрязнена, то растекание не происходит, вода, например, скатывается в шарики. Это один из приемов проверки чистоты ртути. б) Низкоэнергетические поверхности имеют значение s 2 . Это твердые полимеры, органические соединения, оксиды неметаллов, поверхность воды. Значения s для таких поверхностей соизмеримы с таковыми для органических и неорганических жидкостей. Поэтому в данном случае смачивание и несмачивание будет зависеть от соотношения поверхностных натяжений жидкости и поверхности. Можно отметить, что самые низкоэнергетические поверхности (фторопласты, парафины) не смачиваются большинством жидкостей. 3.Растекающиеся жидкости имеют разное значение поверхностного натяжения. Чем выше значение s, тем выше работа когезии (см. 9.4) и тем хуже растекаются такие жидкости. Чем ниже s, тем меньше работа когезии и тем легче растекаются жидкости. Например, вода, обладающая высоким значением s (72 мДж/м 2 ), плохо растекается по разным поверхностям, в то время как углеводороды (бензин, гексан, бензол, s от 18 до 30), растекаются практически по любым поверхностям. Например, нефть растекается по воде, образуя пятна огромной площади; а вода по нефти не растекается, собирается в капли. Это связано с тем, что sводы > sнефти примерно в 3 раза. Поскольку работы адгезии и когезии определяются величинами поверхностных натяжений на границах раздела фаз, то, изменяя значения s введением различных веществ в жидкость или модифицируя поверхность обработкой различными композициями, можно обеспечить перевод процесса несмачивания в смачивание, а смачивания в растекание и наоборот. Капиллярные явления Капиллярные явления наблюдаются в капиллярах и капиллярно-пористых телах, содержащих жидкость. Капиллярные явления заключаются в поднятии или опускании уровня жидкости в капиллярах по сравнению с уровнем жидкости в сосуде, в который опущены эти капилляры (рис. 9.11 и 9.12). Капиллярное поднятие или опускание жидкостей связано с возникновением кривизны поверхности (выпуклый или вогнутый мениск). В свою очередь появление кривизны поверхности связано с процессами смачивания (q 0 , вогнутый мениск) или несмачивания (q > 90 0 , выпуклый мениск) жидкостями стенок капилляров. Давление в фазах, разделенных искривленной поверхностью, отличается от давления в фазах с плоской поверхностью. Причиной возникновения давления является действие сил поверхностного натяжения, которые стремятся уменьшить площадь поверхности раздела фаз (выпрямить ее), Силы эти направлены вдоль поверхности, а равнодействующая этих сил (sр) будет направлена к центру кривизны поверхности (рис. 9.13) Рис. 9.11. Капиллярное поднятие жидкости r0 – радиус капилляра; r – радиус кривизны поверхности жидкости (мениска); q – краевой угол смачивания, q 0 ; h – высота поднятия жидкости.
Рис. 9.12. Отрицательное капиллярное поднятие жидкости, q > 90 0 Рис. 9. 13. Схема, иллюстрирующая возникновение капиллярного Возникающее дополнительное давление Dр, называемое капил-лярным давлением, в одном случае будет направлено вниз и будет способствовать опусканию уровня жидкости (рис. 9.13,а), в другом случае будет направлено вверх и вызовет поднятие жидкости в капиллярах (рис. 9.13,в). Надо отметить, что капиллярные явления возникают только в капиллярах, радиус которых соизмерим с радиусом кривизны поверхности. В широких трубках такие явления не возникают. Для поверхности, имеющей форму правильной сферы: где Dр – капиллярное давление; s – поверхностное натяжение жидкости; r – радиус кривизны поверхности. Для цилиндрической поверхности (возникающей при опускании двух параллельных пластин в жидкость, когда расстояние между пластинами мало) длиной l и радиусом r: Уравнения (9.21) и (9.22) известны под названием уравнений Лапласа. Из них следует, что, чем выше значение s и меньше радиус кривизны, тем выше возникающее давление. При равновесии лапласовское давление равно гидростатическому давлению столба жидкости высотой h (рис. 9.11 и 9.12) Dр = ± 2s/r = (r – r0)gh, (9.23) где r – плотность жидкости; r0 – плотность насыщенного пара; g – ускорение свободного падения; r – радиус кривизны (мениска). Если выразить радиус кривизны через радиус капилляра и краевой угол смачивания, то получим r0 = r cosq ® Из уравнения 9.23 и 9.24 для высоты капиллярного поднятия h получим выражение Уравнение 9.25 называется формулой Жюрена. Эта формула значительно упрощается для случая, когда краевой угол q близок к 0 0 (если жидкость растекается по поверхности). Такой случай реализуется для воды и углеводородов в стеклянных капиллярах. Тогда получим упрощенное выражение Из этой формулы следует, что чем выше s и меньше радиус капилляра, тем выше капиллярное поднятие. Эта формула используется при определении величины поверхностного натяжения жидкости. Капиллярным поднятием жидкостей объясняется ряд известных явлений и процессов. Пропитка бумаги, тканей обусловлена капиллярным поднятием жидкостей в порах; водонепроницаемость тканей обеспечивает-ся их гидрофобностью и как следствие – отрицательным капиллярным поднятием; подъем воды из почвы по стволам растений происходит благодаря волокнистому строению древесины; капиллярными явлениями обусловлены процессы кровообращения в кровеносных сосудах; процессы адсорбции на мелкопористых сорбентах, которые сопровождаются капиллярной конденсацией. Подъем глубинных вод в грунтах и почвах обеспечивает влагой растительность. Для предотвращения высыхания почвы (испарения воды с поверхности) проводят рыхление (боронование) с целью разрушения капилляров и трещин, по которым поднимается влага. Интересным примером проявления капиллярного давления может служить возникновение капиллярной стягивающей силы между частицами, пластинками при наличии между ними прослойки жидкости с вогнутым мениском (при хорошем смачивании частиц жидкостью). Например, сухой песок – сыпучее вещество. При небольшом увлажнении песок хорошо формуется, т.к. между частицами возникают капиллярные силы, стягивающие частицы. При сильном увлажнении песок расплывается, т.к. между частицами исчезает мениск, частицы со всех сторон окружены жидкостью. Еще один пример капиллярного стягивания – это «прилипание» друг к другу стеклянных пластинок, между которыми находится очень тонкая прослойка воды (одна капля). Такие пластинки очень трудно оторвать друг от друга. 1.4.1. Метод измерения капиллярного поднятия жидкостиЭтот метод считают наиболее точным, потому что для него разработана довольно точная теория, а экспериментальные данные легко контролируются. Метод измерения капиллярного поднятия основан на определении разности уровней жидкости в капилляре радиуса r и в широком сосуде. Расчет проводится по формуле Жюрена
где hm– предельная высота поднятия жидкости в капилляре, Q – краевой угол смачивания жидкостью материала капилляра, Dr — разность плотностей жидкости и пара. Жидкость поднимается или опускается по капилляру до тех пор, пока высота мениска не достигнет высоты, при которой масса столба жидкости не уравняет давление внутри и снаружи капилляра. Процесс установления предельной высоты поднятия мениска жидкости в капилляре происходит достаточно долго. Так, например, для чистой воды h = 0,995 hm достигается за 1,5 мин. Метод измерения капиллярного поднятия жидкости является одним из более точных и простых по аппаратурному оформлению и применяется там, где продолжительность формирования поверхности раздела фаз не ограничивается. Устройства, принцип действия которых основан на методе измерения капиллярного поднятия жидкости, состоят из основного элемента — широкой трубки 1 (см. рис. 1.6), верхний и нижний конец которой сообщаются с калиброванным капилляром 2. Для точного определения поверхностного натяжения необходимо с максимальной точностью измерить разность уровней жидкости в узком и широком капиллярах, что составляет известную трудность. Поэтому как один из возможных вариантов может быть использован метод уравнивания высоты столбов жидкости в капиллярах при помощи избыточного давления на мениск в узком капилляре. В данном случае измеряется то давление, которое необходимо, чтобы уровень жидкости в капилляре не превышал уровня жидкости в сосуде, с которым капилляр сообщается. Расчет проводится по формуле
где P- измеренное уравновешивающее давление. К недостаткам всех вариантов метода капиллярного поднятия жидкости следует отнести зависимость измеренного поверхностного натяжения от краевого угла смачивания жидкостью материала капилляра, что позволяет определить поверхностное натяжение при существовании поверхности в течение не менее 10 с; отсутствие возможности обновления поверхности в капилляре; высокую погрешность измерения динамического поверхностного натяжения. Кроме того, формула Жюрена, основанная на уравнении Лапласа для цилиндрического капилляра, не учитывает количества жидкости, находящейся в мениске (высотой x). Краевой угол смачивания капилляра жидкостью должен быть равен нулю и в каждом опыте необходимы довольно большие объемы растворов. Радиус большого капилляра 1 должен быть не менее 5 см. Щелочность раствора не должна приводить к растворению вещества капилляра. Для повышения точности измерений поверхностного натяжения следует вводить поправки, используя таблицы Сагдена. Капиллярные явленияЭтот видеоурок доступен по абонементуУ вас уже есть абонемент? Войти Уверены ли вы, что понимаете, каким образом работает обычное полотенце? Или почему клей склеивает поверхности? Или почему горит свечка? А почему с мылом руки мыть намного эффективнее, чем без мыла? Ответы на все эти вопросы вы получите на данном уроке. Потому что все они, так или иначе, связаны со смачиванием поверхностей и капиллярными явлениями. источники: http://xumuk.ru/colloidchem/20.html http://interneturok.ru/lesson/physics/10-klass/osnovy-termodinamiki/kapillyarnye-yavleniya |





 (9.24)
(9.24) (9.25)
(9.25)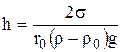 (9.26)
(9.26)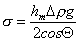 , (1. 1.58)
, (1. 1.58)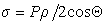 , (1. 1.59)
, (1. 1.59)