Гидролиз
Гидролиз (греч. hydor — вода и lysis — разрушение) — процесс расщепления молекул сложных химических веществ за счет реакции с молекулами воды.
В химии, как и в жизни, разрушается чаще всего нестойкое и слабое (стойкое и сильное выдерживает удар). Запомните, что гидролиз (вода) разрушает «слабое» — это правило вам очень пригодится.
Любая соль состоит из остатка основания и кислоты. Абсолютно любая:
- NaCl — производное основания NaOH и кислоты HCl
- KNO3 — производное основания KOH и кислоты HNO3
- CuSO4 — производное основания Cu(OH)2 и кислоты H2SO4
- Al3PO4 — производное основания Al(OH)3 и кислоты H3PO4
- Ca(NO2)2 — производное основания Ca(OH)2 и кислоты HNO2
Чтобы успешно решать задания по теме гидролиза и писать реакции, вам следует запомнить, какие основания и кислоты являются слабыми, а какие — сильными.
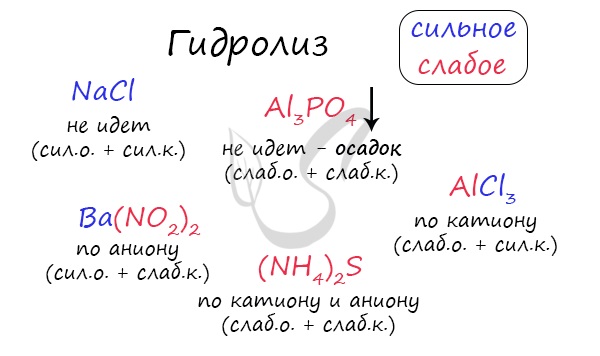
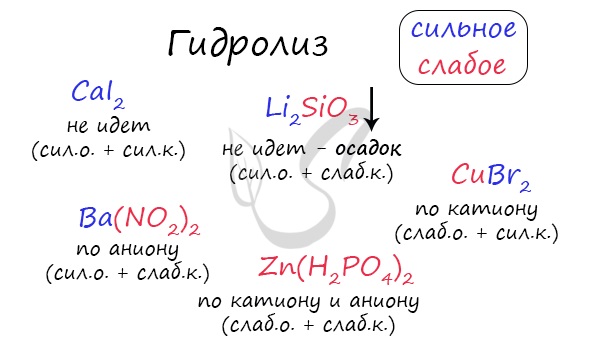
При изучении гидролиза я рекомендую ученикам сохранить на гаджет схему, которую вы видите ниже. Для того, чтобы приобрести нужный опыт — она незаменима. Пользуйтесь ей как можно чаще, подглядывайте в нее и она незаметно окажется в вашем интеллектуальном составляющем 😉
По катиону, по аниону или нет гидролиза?
Итак, если в состав соли входит остаток сильного основания и остаток сильной кислоты — гидролиза не происходит. Примеры: NaCl, KBr, CaSO4. Также гидролиза не происходит, если соль нерастворима (вне зависимости от того, чем она образована): AlPO4, FeSO3, CaSO3.
Если в состав соли входит остаток слабого основания и остаток сильной кислоты, то гидролиз идет по катиону. Помните, что гидролиз разрушает слабое, в данном случае — катион. Примеры: AlCl3, MgBr2, Cr2SO4, NH4NO3.
Катион NH4 + и его основание NH4OH , несмотря на растворимость, является слабым, поэтому гидролиз будет идти по катиону в соли NH4Cl. Замечу также, что Ca(OH)2 считается растворимым основанием, поэтому гидролиза соли CaCl2 не происходит.
Если в состав соли входит остаток сильного основания и остаток слабой кислоты, то гидролиз идет по аниону. Примеры: K3PO4, NaNO2, Ca(OCl)2, Ba(CH3COO)2, Li2SiO3.
Если соль образована остатком слабого основания и слабой кислоты, то гидролиз идет и по катиону, и по аниону. Примеры: Mg(NO2)2, Al2S3, Cr2(SO3)3, CH3COONH4.
Среда раствора
Среда раствора может быть нейтральной, кислой или щелочной. Определяется типом гидролиза. Некоторые задания могут быть построены так, что, увидев соль, вы должны будете определить ее тип раствора.
Обрадую вас: если вы усвоили тему гидролиза, сделать это проще простого. В случае, когда гидролиз не идет или идет и по катиону, и по аниону среда раствора — нейтральная.
Если гидролиз идет по катиону (разрушается остаток основания) среда — кислая, если гидролиз идет по аниону (разрушается остаток кислоты), то среда раствора будет щелочная. Изучите примеры.
Однако замечу, что в дигидрофосфатах, гидросульфитах и гидросульфатах среда всегда кислая из-за особенностей диссоциации. Примеры: NH4H2PO4, LiHSO4. В гидрофосфатах среда щелочная из-за того, что константа диссоциации по третьей ступени меньше, чем константа гидролиза. Примеры: K2HPO4, Na2HPO4.
Попробуйте определить среду раствора для соединений из самостоятельного задания, которое вы только что решили. Ниже будет располагаться решение.
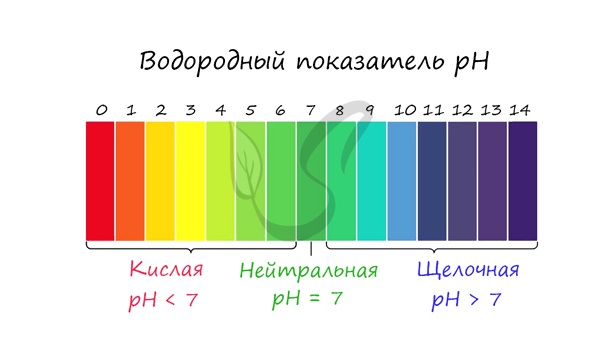
С целью запутать в заданиях часто бывают даны синонимы. Так «среду раствора» могут заменить водородным показателем pH.
Запомните, что кислая среда характеризуется pH 7.
Например, в соли CaCl2 среда раствора будет нейтральной (pH=7), а в растворе AlCl3 — кислой (pH
Частные реакции катионов первой аналитической группы
Читайте также:
|
| Ион | Реагент | Условия проведения реакции | Уравнение реакции в молекулярном и ионном виде | Внешний эффект реакции | Вывод |
Реакции обнаружения катиона калия К +
1. Гидротартрат натрия NaHC4H4O6,или винная кислота,в присутствии ацетата натрия при достаточной концентрации ионов калия К + в растворе дает белый кристаллический осадок гидротартрата калия:
Осадок растворяется в сильных кислотах и щелочах, поэтому реакцию проводят в нейтральной или слабокислой средах:
Реакцию следует проводить при охлаждении под струей водопроводной воды, так как растворимость осадка гидротартрата калия КНС4Н4О6 повышается при увеличении температуры.
Для ускорения выпадения осадка стенки пробирки потирают стеклянной палочкой для образования центров кристаллизации.
Реакция протекает при больших концентрациях ионов калия К + и является малочувствительной. Ионы аммония NH + 4 мешают определению ионов калия К + из-за того, что тоже дают белый кристаллический осадок с этими реагентами и поэтому соли аммония предварительно разлагают при нагревании.
Реакция является фармакопейной.
2. Гексанитрокобальтат (III) натрия Na3[Co(NO2)6] в нейтральном или слабокислом растворе с ионом калия К + дает желтый кристаллический осадок гексанитрокобальтата (III) калия-натрия:
В щелочной среде реакцию обнаружения К + проводить нельзя, так как в этой среде гексанитрокобальтат (III) натрия разлагается с образованием гидроксида кобальта (III) бурого цвета:
В сильных кислотах осадок K2Na[Co(NO2)6] растворяется с образованием нестойкой кислоты гексанитрокобальтата (III) водорода H3[Co(NO2)6].
Реакцию обнаружения ионов калия следует проводить в отсутствии ионов NH4 , так как последние дают аналогичный осадок с Na3[Co(NO2)6]. Рассматриваемая реакция обнаружения иона калия более чувствительна, чем реакция с гидротартратом натрия и является также фармакопейной.
3. Окрашивание пламени. При выполнении этой реакции платиновую проволочку, впаянную в стеклянную палочку, смачивают хлороводородной кислотой и вносят в бесцветное пламя горелки. Прокаливают до тех пор, пока окрашивание пламени не прекратится. Затем раскаленной проволокой касаются мелкого порошка или опускают ее в раствор соли калия и снова вносят в бесцветное пламя горелки. Если в образце или растворе присутствуют ионы калия, то пламя горелки окрашивается в фиолетовый цвет. Присутствие ничтожных следов натрия, окрашивающего пламя в желтый цвет, маскирует окраску.
Эта реакция используется при анализе фармацевтических препаратов.
Реакции обнаружения катиона натрия Na +
1. Гексагидроксостибиат калия K[Sb(OH)6] образует с ионом натрия белый кристаллический осадок гексагидроксостибиат (V) натрия:
Обнаружение иона Na + с помощью гексагидроксостибиата (V) калия проводят в нейтральном или слабощелочном растворе, так как кислоты разлагают реагент:
образуя белый аморфный осадок метасурьмяной кислоты. Щелочи растворяют осадок Na[Sb(OH)6] с образованием хорошо растворимой средней соли:
Соли аммония, дающие в результате гидролиза кислую реакцию среды, также разлагают исходный реактив с образованием метасурьмяной кислоты. Поэтому добиваются отсутствия в растворе ионов NH + 4 до определения в нем ионов К + .
Для образования центров кристаллизации и скорейшего выпадения осадка гексагидроксостибиата (V) натрия реакцию проводят при охлаждении и потирают стенки пробирки стеклянной палочкой.
2. Микрокристаллоскопическая реакция. Ацетат уранила UO2(CH3COO)2 образует в уксуснокислой среде с солями натрия желтоватые кристаллы уранилацетата натрия Na[(UO2)(CH3COO)3]:
При выполнении реакции раствор соли натрия выпаривают досуха и обрабатывают ацетатом уранила. Выпавшие кристаллы имеют форму желтоватых тетраэдров (или октаэдров) под микроскопом ( рис. 8.1).
Рис. 8.1. Кристаллы уранилацетата натрия
Реакция используется в фармакопее.
3. Окрашивание пламени. Соли натрия окрашивают бесцветное пламя горелки в желтый цвет. Реакция очень характерна и является фармакопейной.
Установить присутствие натрия в исследуемом веществе по окрашиванию бесцветного пламени можно только тогда, когда желтая окраска пламени сохраняется 25-30 с.
Реакции обнаружения катиона аммония NH + 4
1. Щелочи NaOH и КОН разрушают аммонийные соли с выделением аммиака:
Выделяющийся аммиак можно обнаружить с помощью влажной красной или фиолетовой лакмусовой бумажки. Образующиеся по реакции
гидроксид-ионы ОН — изменяют окраску лакмуса в синий цвет. Подобную реакцию можно провести в газовой камере (см. рис. 7.8). При большой концентрации выделяющегося аммиака его можно обнаружить и по запаху. Реакция фармакопейная.
2. Реактив Несслера (смесь K2[HgI4] и КОН). Этот реактив дает с аммонийными солями красно-бурый осадок:
При очень малых количествах солей аммония вместо осадка образуется желтый раствор; при большом их количестве — осадок растворяется. Реакция очень чувствительна. Ионы калия и натрия не мешают определению ионов аммония.
Дата добавления: 2014-11-13 ; просмотров: 58 ; Нарушение авторских прав
Что такое гидролиз солей
| Гидролиз соли — взаимодействие ионов соли с ионами воды, приводящее к образованию слабого электролита |
В общем случае под гидролизом понимают обменное разложение веществ водой, как органических, так и неорганических. Из неорганических веществ чаще всего гидролизу подвергаются соли.
Количественно гидролиз соли характеризуется степенью гидролиза, который зависит от природы самой соли, концентрации раствора, температуры:
| Степень гидролиза (h) равна отношению числа гидролизованных молекул (n) к общему числу растворенных молекул (N) h=n/N |
Схема реакции гидролиза:
- XY — соль;
- HOH — молекула воды;
- XH — кислота;
- HOY — основание.
Скорость гидролиза растет с:
- повышением температуры;
- увеличением разведения раствора.
Реакция гидролиза, как правило, обратимая, при этом равновесие реакции можно смещать в ту или другую сторону, добавляя к раствору соли сильную кислоту, либо сильное основание.
Всего возможны 4 варианта гидролиза солей, в зависимости от способа образования соли:
- гидролиз по катиону — соль образована сильной кислотой и слабым основанием: NH4NO3, NH4Cl; ZnCl2; [Cu(NO3)2]; AlCl3;
- гидролиз по аниону — соль образована слабой кислотой и сильным основанием: KNO2, Na2CO3; Na2SO3; K2S; CH3COONa;
- гидролиз по катиону и аниону — соль образована слабой кислотой и слабым основанием: NH4CN; Al2S3; NH4NO2; CH3COONH4;
- соли, образованные сильной кислотой и сильным основанием, гидролизу не подвергаются.
- сильные кислоты: HNO3, H2SO4, HCl, HBr, HI, HClO4, H2CrO4;
- слабые кислоты: HNO2, HF, HCN, H2SO3, H2CO3, H2S, CH3COOH;
- сильные основания: LiOH, NaOH, KOH, Ca(OH)2, Ba(OH)2, Sr(OH)2;
- слабые основания: NH4OH, Fe(OH)2, Fe(OH)3, Cr(OH)3, Cu(OH)2, Zn(OH)2, Al(OH)3.
| Сильные основания | Слабые основания | ||
|---|---|---|---|
| Сильные кислоты | гидролиза нет pH=7 | гидролиз по катиону pH 7 | гидролиз по катиону и аниону pH≈7 |
Гидролиз по катиону
- NH4NO3 — нитрат аммония образован сильной кислотой и слабым основанием;
- NH4OH — слабое основание;
- HNO3 — сильная кислота.
Уравнение гидролиза по катиону в ионном виде:
В процессе гидролиза катион NH4 + связывает гидроксид-ионы [OH — ] воды (красный цвет), в результате чего появляется избыток катионов водорода [H + ] и раствор становится кислым [H + ]>[OH — ] (pH K + + NO2 — + H OH ↔ HNO2 + K + + OH —
При гидролизе солей по аниону все происходит с точностью, до наоборот — анион слабой кислоты NO2 — связывает катион водорода [H + ] (выделены синим цветом), в результате чего появляется избыток гидроксид ионов [OH — ], раствор становится щелочным [H + ] — ] (pH>7).
Гидролиз по катиону и аниону
- NH4CN — цианид аммония образован слабой кислотой и слабым основанием;
- HCN — слабая кислота;
- NH4OH — слабое основание.
Уравнение гидролиза по аниону и катиону в ионном виде:
NH4 + + CN — + H OH ↔ NH4OH + HCN
Реакция раствора соли NH4CN слабощелочная, поскольку Kд(NH4OH)>Kд(HCN).
Кислотность раствора зависит от силы образующихся кислоты и основания. Гидролиз солей, образованных слабыми кислотами и основаниями, идет до конца, если в процессе реакции выпадает осадок или образуется газ.
Ионы солей, образованных сильными кислотами и основаниями, не образуют с ионами воды малодиссоциирующих соединений, поэтому не гидролизуются, раствор при этом остается нейтральным.
Соли, образованные двух(трех)основными кислотами и(или) двух(трех)кислотными основаниями гидролизуются ступенчато.
Ступенчатый гидролиз
1) Соль образована слабой многоосновной кислотой и сильным основанием — кол-во ступеней такого гидролиза зависит от основности слабой кислоты.
В качестве примера разберем гидролиз карбоната калия K2CO3.
Соль образована слабой двухосновной кислотой (H2CO3) и сильным основанием (KOH), поэтому, ее гидролиз протекает по аниону (см. выше).
Поскольку кислота H2CO3 является двухосновной, то и гидролиз будет двухступенчатым.
Первая ступень гидролиза карбоната калия:
K2 CO3 + H OH ↔ KOH+K HCO3
Продуктами первой ступени гидролиза карбоната калия являются гидроксид калия (KOH) и кислая соль (KHCO3).
Сокращенное ионное уравнение первой ступени гидролиза:
Вторая ступень гидролиза карбоната калия:
K2 HCO3 + H OH ↔ KOH+ H2CO3
Продуктами второй ступени гидролиза карбоната калия является всё тот же гидроксид калия (KOH) и слабая угольная кислота (H2CO3).
Сокращенное ионное уравнение второй ступени гидролиза:
Гидролиз второй ступени протекает в значительно меньшей степени, чем гидролиз первой ступени. Поскольку в процессе гидролиза увеличивается концентрация гидроксид-ионов, среда раствора получившейся соли K2CO3 является щелочной.
2) Соль образована сильной кислотой и слабым многокислотным основанием — кол-во степеней такого гидролиза определяется кислотностью слабого основания.
В качестве примера разберем гидролиз хлорида никеля NiCl2 (II).
Соль образована сильной кислотой (HCl) и слабым основанием (Ni(OH)2), поэтому, ее гидролиз протекает по катиону (см. выше).
Первая ступень гидролиза хлорида никеля в ходе которой катионы никеля связывают гидроксид-ионы воды:
Ni Cl2+H OH ↔ NiOH Cl+HCl
Продуктами первой ступени гидролиза хлорида никеля являются сильная кислота (HCl) и основная соль(NiOHCl).
Сокращенное ионное уравнение первой ступени гидролиза:
Вторая ступень гидролиза:
NiOH Cl+H OH ↔ Ni(OH)2 +HCl
Продукты второй ступени гидролиза хлорида никеля являются сильная кислота и слабое основание.
Сокращенное ионное уравнение второй ступени гидролиза:
Гидролиз второй ступени протекает в значительно меньшей степени, чем гидролиз первой ступени. Поскольку в процессе гидролиза увеличивается концентрация ионов водорода, среда получившегося раствора NiCl2 является кислой.
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
http://lektsii.com/1-6402.html
http://prosto-o-slognom.ru/chimia/04_9_gidroliz_solej.html