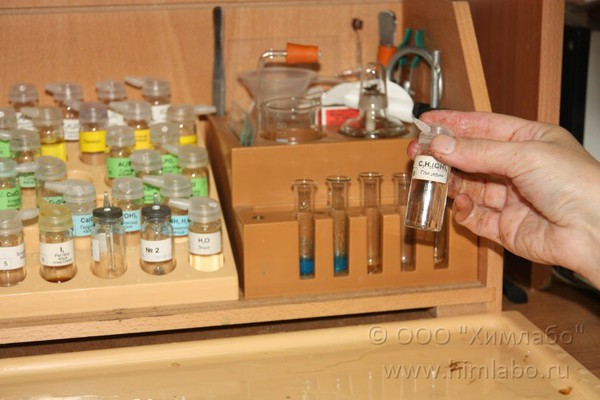
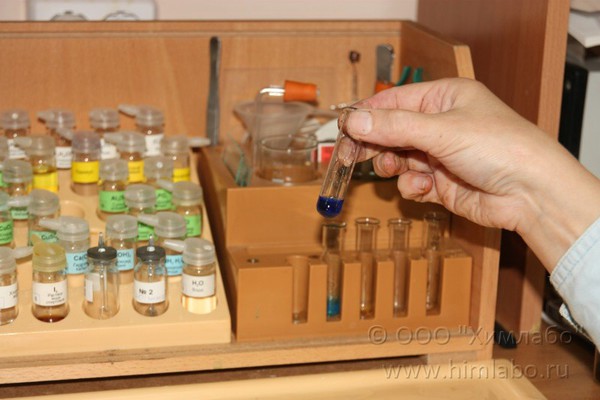
Качественная реакция на глицерин
При проведении опыта используем Микролабораторию для химического эксперимента
Цель опыта: изучить качественную реакцию на глицерин.
Оборудование: пробирки (2 шт.).
Реактивы: раствор гидроксида натрия NaOH, раствор сульфата меди(II) CuSO4, глицерин C3H5(OH)3.
Ход работы
1. В две пробирки вносим по 20-25 капель сульфата меди(II).
2. Добавляем к нему избыток гидроксида натрия.
3. Образуется осадок гидроксида меди(II) голубого цвета.
4. В одну пробирку по каплям добавляем глицерин.
5. Встряхиваем пробирку до исчезновения осадка и образования темно-синего раствора глицерата меди(II).
6. Сравниваем окраску раствора с окраской гидроксида меди(II) в контрольной пробирке.
Вывод:
Качественной реакцией на глицерин является его взаимодействие с гидроксидом меди (II).
Оказываем содействие в подготовке технических требований для тендерной документации.
Внимание! Изображение товара может отличаться от полученного Вами товара. Производитель оставляет за собой право изменять комплектацию и технические характеристики товара без предварительного уведомления без ухудшения функциональных и качественных показателей. Информация о товаре носит справочный характер и не является публичной офертой, определяемой Статьей 437 ГК РФ.
Убедительная просьба, при покупке учебного оборудования согласовывать с менеджером важные для Вас характеристики, комплектацию и цену учебного оборудования.
Конспект урока по теме «Глицерин». 10-й класс
Разделы: Химия
Класс: 10
Тип урока: урок изучения нового материала
Цель урока: дать понятие о многоатомных спиртах
Задачи урока:
- Образовательные: раскрыть зависимость: состав —> строение —> свойства —> применение глицерина
- Развивающие: продолжить формирование умений: наблюдать за физическими и химическими явлениями, объяснять наблюдаемые явления.
- Воспитательные: формирование интереса к предмету
Использованная литература: Рудзитис Г.Е., Фельдман Ф.Г. Органическая химия, 10 класс
Используемое оборудование:
- Реактивы: растворы сульфата меди (II), натрий кристаллический, глицерин, вода, хлорид натрия, снег
- Оборудование: медиапроектор, презентация, пробирки, фильтровальная бумага, спиртовка, спички, лучинка
I. Организационный момент: приветствие
II. Актуализация опорных ЗУН
Устная фронтальная беседа
— Что такое спирты? (Спирты – производные углеводородов, в молекулах которых один или несколько атомов водорода замещены гидроксильными группами)
— Какова общая формула одноатомных спиртов? (CnH2n+1OH)
— Какие виды изомерии характерны для спиртов? (Изомерия углеродного скелета, изомерия положения гидроксильной группы)
— Как даются названия спиртам? (Названия производятся от названий соответствующих углеводородов с добавлением суффикса –ол)
III. Логический переход к новому материалу. Определение темы и цели урока.
Многоатомные спирты – органические соединения, в молекулах которых содержится несколько гидроксильных групп, соединенных с углеводородными радикалами.
СН2ОН-СН2ОН — этандиол-1,2, этиленгликоль
СН2ОН-СНОН-СН2ОН — пропантриол – 1,2,3 , глицерин
Цель урока: рассмотреть глицерин, его физические и химические свойства, способы его получения и применение
Определение темы урока (Глицерин)
IV. Формирование новых ЗУН
1. Получение глицерина
Впервые глицерин получил К. В. Шееле (1779 г) и повторно М.Э. Шеврель (1813г).
В лаборатории глицерин получают из галогенопроизводых соответствующих углеводородов.
Чтобы сдвинуть равновесие реакции вправо. Выделяющуюся соляную кислоту нейтрализуют щелочью.
Глицерин на производстве получают из пропилена, который образуется при крекинге и пиролизе нефти, а также из жиров.
2. Физические свойства
Глицерин – бесцветная сиропообразная жидкость сладковатого вкуса, хорошо растворяется в воде и в этаноле, кипит при температуре 290 0 С, гигроскопичен.
Опыт №1. Понижение точки замерзания водных растворов глицерина.
В пробирку налить 5 мл глицерина и сверху постепенно наслаивается такой же объем подкрашенной фуксином воды, встряхнуть. Пробирку поместить в охладительную смесь (смесь снега и твердого хлорида натрия), в смесь одновременно поместить пробирку с водой.
Вопросы во время демонстрации:
— Что наблюдаете? (жидкость становится однородной и окрашивается)
— Какой вывод можно сделать в результате опыта? (Глицерин – незамерзающая жидкость и может быть использована в качестве незамерзающих жидкостей для охлаждения моторов)
Опыт №2. Гигроскопиность глицерина
На лист фильтровальной бумаги нанести несколько капель воды, на второй лист – несколько капель глицерина. Оставить на время.
3. Химические свойства.
Химические свойства глицерина схожи с химическими свойствами одноатомных спиртов.
1. Взаимодействие с кристаллическим натрием
Опыт 3. Реакция с натрием
В пробирку налить 2-3 мл глицерина, опустить в раствор металлический натрий величиной с горошину. Пробирку слегка подогреть, поджечь выделяющийся газ.
Вопросы во время демонстрации
— Что наблюдаете? (выделяется газ, обугливание)
— Какой газ выделяется? (водород, т.к. лучинка горит синим пламенем)
Взаимодействие с гидроксидом меди (II), в присутствии щелочи. Осадок растворяется и образуется раствор ярко-синего цвета – глицерат меди.
Опыт 4. В пробирку налить гидроксид натрия и по каплям до образования осадка приливаем сульфат меди, к полученному осадку приливаем глицерин.
Уравнение реакции дано в упрощенном виде, ибо одновременно образуются и соединения более сложного состава. Данная реакция доказывает, что многоатомные спирты обладают слабыми кислотными свойствами. Эта реакция является качественной на многоатомные спирты.
Увеличение числа гидроксильных групп в молекулах многоатомных спиртов придает большую подвижность атомам водорода по сравнению с одноатомными спиртами. Это результат взаимного влияния гидроксильных групп друг на друга.
4. Взаимодействие с азотной кислотой.
В результате образуется нитроглицерин – сложный эфир азотной кислоты и глицерина.
Для практического применения нитроглицерина его переводят в динамит, пропитывая нитроглицерином инфузорную землю или древесную муку. Автором динамита является А. Нобель
Взаимодействие с галогеноводородами
СН2ОН – СНОН – СН2ОН + 3HCl —> СН2Сl – СНСl – СН2Сl + 3Н2О
Глицерин применяют для получения нитроглицерина и динамита. Глицерин используется в парфюмерии и медицине (для изготовления мазей, смягчающих кожу), в кожевенном производстве (для предохранения кож от высыхания), в текстильной промышленности (для придания тканям мягкости и эластичности). В медицине 1%-й раствор нитроглицерина в спирте служит в качестве одного из средств, расширяющих кровеносные сосуды.
6. Генетическая связь многоатомных спиртов с другими классами органических соединений
Вернемся к опыту с фильтровальной бумагой
— Что наблюдаете? (бумага с водой высохла, а с глицерином стала еще важнее)
— Что можно сказать о глицерине? (глицерин может поглощать влагу, тем самым увлажнять предметы).
Раскрыть генетическую схему
VI. Сообщение д/з: параграф 24
Итак, сегодня на уроке мы познакомились с многоатомными спиртами на примере глицерина, рассмотрели его физические и химические свойства, способы получения и применение. На этом урок окончен.
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. источники: http://urok.1sept.ru/articles/636792 http://acetyl.ru/o/a31f3i.php |