АБСОРБЦИЯ
Тема 3.3. Абсорбция 12ч., в т.ч. лаб. раб. и практ. занят 6ч.
Студент должен:
знать:
— физические основы и теорию процесса абсорбции (равновесие между фазами, принципы составления материального теплового баланса, уравнение рабочей линии);
— порядок расчета насадочного и барботажного абсорбера;
— сущность и методы проведения десорбции;
уметь:
— составлять материальный и тепловой баланс;
— определять расход поглотителя;
— строить равновесную и рабочую линию процесса;
— определять основные габаритные размеры абсорберов, пользуясь справочниками.
Назначение абсорбции. Абсорбция при разделении гомогенных газовых смесей и очистки газов. Выбор абсорбента. Физическая абсорбция и абсорбция, сопровождаемая химическим взаимодействием. Десорбция.
Равновесие между фазами при абсорбции. Влияние температуры и давления на растворимость газов в жидкостях. Материальный баланс процесса и уравнения рабочей линии при абсорбции и десорбции. Расход абсорбента. Тепловой баланс абсорбции. Отвод тепла при абсорбции.
Абсорбцией называют процесс избирательного поглощения компонентов из газовых или парогазовых смесей жидкими поглотителями – абсорбентами.
Принцип абсорбции основывается на различной растворимости компонентов газовых и парогазовых смесей в жидкостях при одних и тех же условиях. Поэтому выбор абсорбентов осуществляют в зависимости от растворимости в них поглощаемых компонентов, которая определяется:
· физическими и химическими свойствами газовой и жидкой фаз;
· температурой и давлением осуществления процесса;
· содержанием газа в смеси.
При выборе абсорбента необходимо учитывать такие его свойства, как селективность (избирательность) по отношению к поглощаемому компоненту, токсичность, пожароопасность, стоимость, доступность и др.
Различают физическую абсорбцию и химическую абсорбцию (хемосорбцию). При физической абсорбции поглощаемый компонент образует с абсорбентом только физические связи. Процесс этот в большинстве случаев является обратимым. На этом свойстве основано выделение поглощенного компонента из раствора – десорбция. Если поглощаемый компонент вступает в реакцию с абсорбентом и образует химическое соединение, то процесс называют хемосорбцией.
Процесс абсорбции обычно является экзотермическим, т. е. сопровождается выделением теплоты.
Абсорбция широко используется в промышленности для разделения углеводородных газов на нефтеперерабатывающих установках, получения соляной и серной кислот, аммиачной воды, очистки газовых выбросов от вредных примесей, выделения ценных компонентов из газов крекинга или пиролиза метана, из газов коксовых печей и т. д.
Равновесие в процессах абсорбции определяется правилом фаз Гиббса (В.4), представляющим обобщение условий гетерогенного равновесия:
Поскольку процесс абсорбции осуществляется в двухфазной (газ – жидкость) и трехкомпонентной (один распределяемый и два распределяющих компонента) системе, число степеней свободы – три.
Таким образом, равновесие в системе газ (пар) – жидкость может характеризоваться тремя параметрами, например температурой, давлением и составом одной из фаз.
Равновесие в системе газ – жидкость определяется законом растворимости Генри, согласно которому при данной температуре мольная доля газа в растворе (растворимость) пропорциональна парциальному давлению газа над раствором:
где р – парциальное давление газа над раствором; х – мольная концентрация газа в растворе; Е – коэффициент пропорциональности (коэффициент Генри).
Закон Генри распространяется в первую очередь на слаборастворимые газы, а также на растворы с низкими концентрациями хорошо растворимых газов при отсутствии химической реакции.
Коэффициент Е имеет размерность давления, совпадающую с размерностью р, и зависит от природы растворяющегося вещества и температуры. Установлено, что с увеличением температуры растворимость газа в жидкости уменьшается. Когда в равновесии с жидкостью находится смесь газов, закону Генри может следовать каждый из компонентов смеси в отдельности.
Поскольку тепловой эффект, сопровождающий процесс абсорбции, отрицательно сказывается на положении линии равновесия, он должен обязательно учитываться при расчетах. Количество теплоты, выделяющейся при абсорбции, может быть определено по зависимости
где qд — дифференциальная теплота растворения в пределах изменения концентрации х1 – х2; L – количество абсорбента.
Если абсорбция ведется без отвода теплоты, то можно допустить, что вся выделяющаяся теплота идет на нагревание жидкости, и температура последней повышается на величину
где с – теплоемкость раствора.
Для понижения температуры исходную газовую смесь и абсорбент охлаждают, отводя теплоту, выделяющуюся в процессе абсорбции, с помощью встроенных (внутренних) или наружных теплообменников.
Парциальное давление растворяемого газа в газовой фазе, соответствующее равновесию, может быть определено по закону Дальтона, согласно которому парциальное давление компонента в газовой смеси равно общему давлению, умноженному на мольную долю этого компонента в смеси, т. е.
где Р – общее давление газовой смеси; у – мольная концентрация распределяемого в смеси газа.
Сопоставляя уравнения (10.2) и (10.1), найдем
где Аравн = Е/Р – константа фазового равновесия, применимая для областей действия законов Генри и Дальтона.
Пусть Раб – давление паров чистого абсорбента в условиях абсорбции; раб – парциальное давление паров абсорбента в растворе; Р – общее давление; х – мольная доля абсорбируемого газа в растворе; у – мольная доля распределяемого газа в газовой фазе; уаб – мольная доля абсорбента в газовой фазе.
Согласно закону Рауля парциальное давление компонента в растворе равно давлению пара чистого компонента, умноженному на его мольную долю в растворе:
По закону Дальтона (10.2) парциальное давление абсорбента в газовой фазе равно
Анализ факторов, влияющих на равновесие в системах газ (пар) – жидкость, позволил установить, что к параметрам, улучшающим условия абсорбции, относятся повышенное давление и пониженная температура, а к факторам, способствующим десорбции, — пониженное давление, повышенная температура и введение в абсорбент добавок, уменьшающих растворимость газов в жидкостях.
Материальный баланс процесса абсорбции выражается дифференциальным уравнением
где G – поток газовой смеси (инертного газа), кмоль/с; L – поток абсорбента, кмоль/с; Yн и Yк – начальное и конечное содержание распределяемого вещества в газовой фазе, кмоль/кмоль инертного газа; Хк и Хн – начальное и конечное содержание распределяемого вещества в абсорбенте, кмоль/кмоль абсорбента; М – количество распределяемого вещества, перенесенного из фазы G в фазу L в единицу времени, кмоль/с.
Из уравнения материального баланса (10.9) можно определить необходимый общий расход абсорбента
Процесс абсорбции характеризуется также степенью извлечения (поглощения), представляющей отношение количества фактически поглощенного компонента к количеству, поглощаемому при полном его извлечении,
Кинетика процесса абсорбции характеризуется тремя основными стадиями, которые соответствуют схеме, представленной на рис. 9.4.
Первая стадия – перенос молекул абсорбируемого компонента из ядра потока газа (пара) к поверхности раздела фаз (поверхности жидкости).
Вторая стадия – диффундирование молекул абсорбируемого компонента через поверхностный слой жидкости (граница раздела фаз).
Третья стадия – переход молекул абсорбируемого вещества от поверхности раздела фаз в основную массу жидкости.
Кинетические закономерности абсорбции соответствуют общему уравнению массопередачи для двухфазных систем:
Экспериментально установлено, что вторая стадия процесса абсорбции идет с большей скоростью и не влияет на общую скорость процесса, ограниченную скоростью наиболее медленной стадии (первой или третьей).
Движущая сила процесса абсорбции для I и III стадий в уравнениях (10.5а) и (10.6а) может быть выражена через другие параметры:
В уравнениях (10.5б) и (10.6б) р – рабочее парциальное давление распределяемого газа в газовой смеси; рравн – равновесное давление газа над абсорбентом, соответствующее рабочей концентрации в жидкости; С – рабочая объемная мольная концентрация распределяемого газа в жидкости; Сравн – равновесная объемная мольная концентрация распределяемого газа в жидкости, соответствующая рабочему парциальному давлению его в газовой смеси.
При таком выражении движущей силы процесса абсорбции уравнение равновесной зависимости принимает вид
где Ψ – коэффициент пропорциональности, кмоль/(м 3 *Па).
Коэффициенты массопередачи выражаются для уравнений (10.5а) и (10.6а) в виде
для уравнений (10.5б) и (10.6б)
В уравнениях (10.7) и (10.8) βу, βр – коэффициенты массоотдачи от потока газа к поверхности контакта фаз; βх, βС — коэффициенты массоотдачи от поверхности контакта фаз к потоку жидкости.
Коэффициенты массоотдачи по газу и жидкости βу и βх могут быть определены из критериальных уравнений, имеющих вид:
для жидкой фазы Nuдиф х = f*(Re, Prдиф х).
Величина коэффициента Ψ оказывает существенное влияние на кинетику процесса абсорбции. Если Ψ имеет высокие значения (высокая растворимость компонента – диффузионное сопротивление сосредоточено в газовой фазе), то 1/(βc*Ψ)
Дата добавления: 2015-08-14 ; просмотров: 7360 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Материальный баланс абсорбции.
Для составления материального баланса возьмем абсорбционную колонну. Когда концентрации фаз мало изменяются по высоте абсорбера, то уравнение 
Где, yн,ук — концентрация компонента в газовой фазе, <кг комп/кг смеси>
хн,хк — концентрация компонента в жидкой фазе, <кг комп/кг жидк>,
G, L- количество фазы, кг/час.
Если концентрация компонента на входе и на выходе изменяется значительно, то
Где, Gин – количество инертного газа, кг/час,
L0 — количество жидкости без растворенного компонента, кг/час,
Yн,Yк – мольный кг компонента и мольный кг газа
у- мольная доля компонента,
Мк – молекулярная масса компонента,
Мин – молекулярная масса инертного газа,
х – мольная доля жидкости.
Кинетика абсорбции.
Кинетика абсорбции характеризуется тремя стадиями.

I и IIIстадии абсорбции осуществляются за счет разницы компонента на границе раздела фаз, и в объеме газовой фазы или жидкости (они протекают по диффузионным законам). IIстадия протекает мгновенно и никакого сопротивления не оказывает.
Законы диффузии.
Конвективная диффузия – это перенос вещества из участка с большей концентрацией в меньшую концентрацию объемами, струйками текучих сред в результате их взаимного перемешивания.
Количество вещества, протекаемого от основного потока до встречи с ламинарным слоем определяется по закону Щукарева:
М – количество компонента, переходящего из газа в жидкость,
β – коэффициент массотдачи,
F- поверхность контакта (абсорбции)
коэффициент массоотдачи представляет собой количество вещества, диффузирующего в единицу времени из окружающей среды к единице поверхности раздела фаз при разности концентрации компонента в объеме среды и у поверхности равным 1.
В ламинарном слое протекают молекулярно-диффузиционный процесс, который описывается законом Фика:
Д – коэффициент диффузии,
Физический смысл коэффициента диффузии (Д) представляет собой количество вещества, переходящего в единицу времени через единицу поверхности при градиенте концентрации, равном 1.
Коэффициент диффузии для газов:
где Т- абсолютная температура,
Vа ,Vв – молекулярные объемы газов,
Ма ,Мв – молекулярные массы газов.
Пример:NH3 и воздух.
V возд = 29,9 м 3 /моль
После подстановки данных:
ДNH3 в возд =0,208 * 10 -4 м 2 /с,
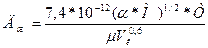
Vа – атомный объем компонента,
ά – поправочный коэффициент,
μ – вязкость жидкости.
После подстановки данных:
βd/Д= 0,023(Wdρ/μ) 0.8 *(μ/ρД) 0,4 – массопередача
άd/= 0,023(Wdρ/μ) 0.8 *(Ср*ρ) 0,4 – теплопередача
после решения системы 2-х уравнений
Решая систему уравнений:
II М= у / -mу процесс растворения
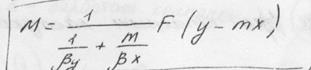
Коэффициент абсорбции или массопередачи:
F – коэффициент абсорбции
(у-mх)=∆уср – средняя движущая сила процесса абсорбции
Основное уравнение абсорбции:
Основное уравнение, с которого начинается расчет абсорбционного аппарата:
Реферат: Абсорбция 2
| Название: Абсорбция 2 Раздел: Рефераты по химии Тип: реферат Добавлен 12:11:11 23 июня 2011 Похожие работы Просмотров: 2147 Комментариев: 21 Оценило: 2 человек Средний балл: 5 Оценка: неизвестно Скачать |

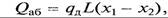
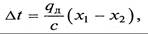

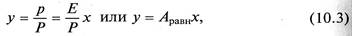


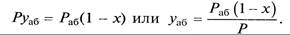
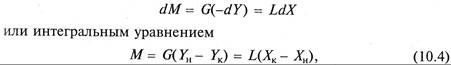

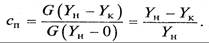
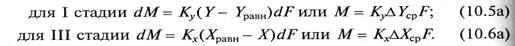
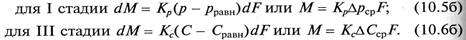
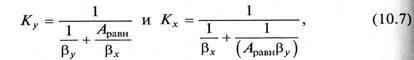
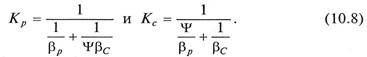
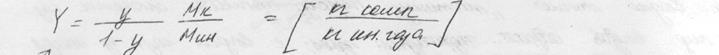





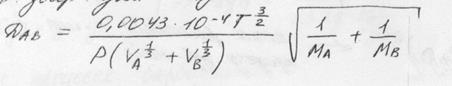



 (1)
(1) (2)
(2) -парциальное давление поглощаемого газа, находящегося в равновесии с раствором, имеющим концентрацию хА (в мол. долях);
-парциальное давление поглощаемого газа, находящегося в равновесии с раствором, имеющим концентрацию хА (в мол. долях); — концентрация газа в растворе (в мол. долях), равновесном с газовой фазой, в которой парциальное давление поглощаемого компонента равнорА ; Е — коэффициент пропорциональности, называемый коэффициентом, или константой Генри.
— концентрация газа в растворе (в мол. долях), равновесном с газовой фазой, в которой парциальное давление поглощаемого компонента равнорА ; Е — коэффициент пропорциональности, называемый коэффициентом, или константой Генри. (3)
(3) Рисунок 2- Растворимость газа в жидкости при различных температурах (t1 >t2 >t3 и соответственно E1 >E2 >E3 )
Рисунок 2- Растворимость газа в жидкости при различных температурах (t1 >t2 >t3 и соответственно E1 >E2 >E3 ) (4)
(4) (5)
(5)
 (6)
(6) (7)
(7)

 (8)
(8) (9)
(9) (10)
(10) (11)
(11) (12)
(12) (13)
(13) .
.