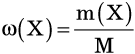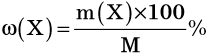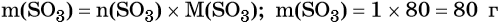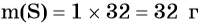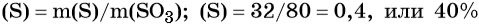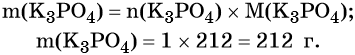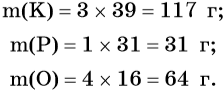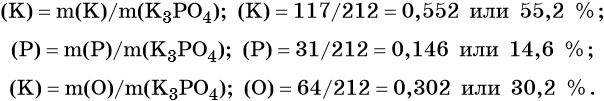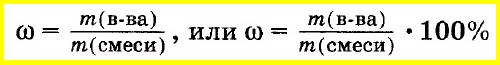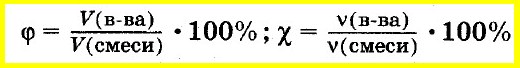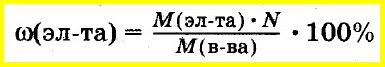Массовая доля
О чем эта статья:
Что такое массовая доля
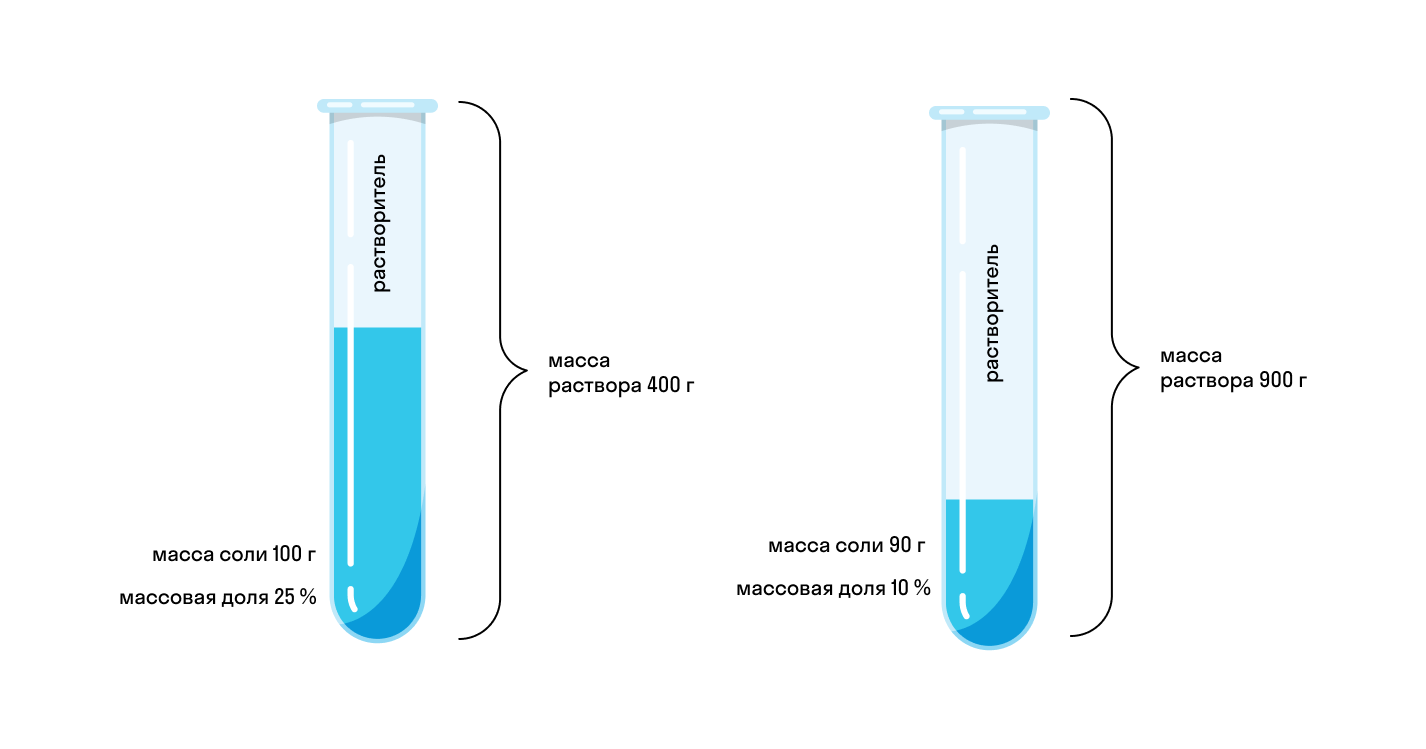
Начнем с примера: допустим, мы приготовили два раствора соли. Первый имеет массу 400 г и для него использовано 100 г соли. Масса второго 900 г и для него использовали 90 г соли. Какой раствор будет более концентрированным? Чтобы это понять, нужно выяснить процент соли в каждом растворе. Можно сказать иначе — нужно определить, какую долю в растворе занимает соль.
Массовая доля — это отношение растворенного вещества к массе раствора. Она может измеряться в процентах (от 0 до 100%) или в долях от единицы (от 0 до 1).
Как найти массовую долю растворенного вещества, расскажет формула:
где — обозначение массовой доли;
В нашем примере и без формул понятно, что в первом растворе соль занимает 25%, а в то втором — только 10%. А что будет, если в первый раствор добавить еще столько же соли и воды? Очевидно, что на концентрацию это не повлияет. Доля соли останется прежней, пусть даже масса раствора увеличилась.
Массовая доля химического элемента — это отношение между относительной массой его атомов и относительной молекулярной массой соединения, частью которого является данный элемент.
Как видите, фактическая масса сложного вещества или его отдельного компонента не имеет значения. Если мы не знаем этих показателей, для расчетов берутся относительные величины.
Такое определение массовой доли элемента выражается формулой:
В данном случае:
— количество атомов искомого элемента;
— относительная атомная масса элемента;
— относительная молекулярная масса сложного вещества.
Если нужен показатель в процентах, результат надо умножить на 100%.
Относительная атомная и молекулярная масса
В формуле нахождения массовой доли мы видим две важные составляющие: относительную массу атома элемента (Ar) и относительную массу молекулы вещества (Mr). Разберемся, что это такое. И та, и другая величина — это отношение реальной массы к эталонной единице, за которую взята 1/12 массы атома углерода.
Относительная атомная масса элемента (Ar) говорит о том, насколько масса его атома больше 1/12 массы атома углерода. Для каждого элемента эта величина является постоянной и ее можно увидеть в таблице Менделеева.
Относительная молекулярная масса соединения (Mr) складывается из относительных атомных масс всех элементов в составе его молекулы. Она показывает, насколько молекула вещества больше 1/12 массы атома углерода.
Это не измеряемые величины, то есть они не имеют единиц измерения. Буква r в обозначениях относительной атомной и молекулярной массы восходит к английскому слову relative — «относительный».
Как найти массовую долю элемента в веществе
Выше мы рассмотрели формулу для вычисления массовой доли химического элемента в веществе и узнали, откуда берутся ее составляющие. Применим эти знания на практике.
Пример 1
Оксид магния массой 8 г образовался при вступлении 4,8 г магния в реакцию с кислородом. Каковы массовые доли магния и кислорода в полученном оксиде?
Решение:
Для начала вычислим массу кислорода. Согласно закону сохранения массы веществ в соединении можно воспользоваться формулой m(O) = m(MgO) − m(Mg).
m(O) = 8 − 4,8 = 3,2 г
Вспоминаем, как найти массовую долю элемента в веществе: нужно понять, какую часть соединения оно составляет.
Зная массы каждого компонента оксида, сделать расчет несложно:
Ответ: массовые доли магния и кислорода в оксиде магния составляют 60% и 40% соответственно.
Пример 2
Потренируемся находить массовую долю элемента в сложном веществе. Определим, какую часть этилового спирта С2H6O составляет водород.
Решение:
В данном случае у нас нет конкретных указаний на массы элементов или всего вещества. Но мы можем воспользоваться другой формулой массовой доли в химии, которая позволяет работать с относительными величинами:
Согласно таблице Менделеева относительная атомная масса водорода равна единице.
Вычислим относительную молекулярную массу соединения С2H6O, которая складывается из соответствующих масс каждого элемента:
Mr(С2H6O) = 2M(C) + 6M(H) + M(O) = 212 + 6 1 + 16 = 46.
Полученные данные подставим в формулу и определим массовую долю элемента в соединении:
Ответ: в этиловом спирте массовая доля водорода составляет 13%.
Как вычислить массовую долю вещества в растворе
Вспомним, что такое концентрация раствора. Она говорит о том, в каком соотношении находятся растворенное вещество и растворитель, а другими словами — сколько растворенного вещества содержится в единице объема или массы. Концентрация может быть безразмерной величиной и выражаться в процентах, но также ее можно выразить в массовых или в молярных долях.
В случае с растворами применима та же формула:
Если нужно значение в процентах, результат надо умножить на 100%.
Пример
Требуется приготовить 0,5 л раствора карбоната натрия плотностью 1,13 г/мл. Определите массу карбоната натрия при условии, что концентрация раствора должна быть 13%.
Решение:
Вначале нам нужно узнать массу раствора, что легко сделать, когда известны его объем и плотность. Воспользуется формулой m(р–ра) = ρ × V
m(р–ра) = 500 × 1,13 = 565 г.
Дальше вспомним, как находить массовую долю растворенного вещества:
Поскольку концентрация раствора — это и есть массовая доля растворенного вещества, подставим ее в уравнение:
m(Э) = 0,13 × 565 = 73,45 г.
Ответ: для раствора понадобится 73,45 г карбоната натрия.
Вопросы для самопроверки:
Как обозначается массовая доля и в чем она выражается?
В чем разница между молекулярной массой вещества и его молярной массой?
Как найти массовую долю элемента в веществе, если мы знаем массу элемента и массу вещества?
Как рассчитать массовую долю вещества в растворе?
В каких безразмерных и размерных величинах можно выразить концентрацию раствора?
Вычисление массовой доли химического элемента в веществе
Одним из основных законов химии является закон постоянства состава вещества (рассмотрен ранее в уроке 5).
На основании данного закона проводятся различные практически значимые вычисления, в том числе вычисления массовой доли химического элемента в веществе.
Массовой долей вещества ω(X) называют отношение массы данного вещества в системе к массе всей системы. Для некоего вещества X:
где ω(Х) — массовая доля вещества Х, m(X) — его масса; M — масса всей системы.
Массовая доля является величиной безразмерной. Ее выражают в долях от единицы или в процентах, если долю от единицы умножить на 100:
В качестве системы может выступать как молекула химического соединения, так и смесь, раствор и т. д. Рассмотрим несколько типовых заданий.
Пример 1. Рассчитайте массовую долю серы в оксиде серы (VI).
Решение: Молярная масса оксида серы (VI) M(SO3) = 80 г/моль, атомная масса серы в этом соединении 32 г/ моль. Для расчётов выбираем образец оксида серы количеством вещества 1 моль. Масса этого вещества составит:
Исходя из формулы SO3 можно заключить, что в 1 моль SO3 будет содержаться 1 моль серы, масса которой составит:
Тогда массовая доля серы в оксиде серы (VI) будет равна:
Ответ: 0,4, или 40%.
Пример 2. Рассчитайте массовые доли элементов в фосфате калия K3PO4.
Решение: Молярная масса M(K3PO4) = 212 г/моль. Для расчётов выбираем образец фосфата калия количеством вещества 1 моль. Масса этого вещества составит:
Исходя из формулы K3PO4 можно заключить, что в 1 моль этого соединения будет содержаться 3 моль калия, 1 моль фосфора и 4 моль кислорода, масса которых составит:
Определим массовые доли элементов:
Тренировочные задания
1. Количественное содержание элементов калия, серы и кислорода в сульфите калия равно
1) 20,2; 30,4; 49,4
2) 49,4; 20,2; 30,4
3) 30,4; 49,4; 20,2
4) 49,4; 30,4; 20,2
2. Количественное содержание элементов бария, серы и кислорода в сульфите бария равно
1) 63,1; 22,1; 14,8
2) 63,1; 14,8; 22,1
3) 14,8; 22,1; 63,1
4) 22,1; 63,1; 14,8
3. Количественное содержание элементов кальция, фосфора и кислорода в фосфате кальция равно
1) 20,0; 41,3; 38,7
2) 38,7; 20,0; 41,3
3) 38,7; 41,3; 20,0
4) 41,3; 38,7; 20,0
4. Количественное содержание элементов натрия, фосфора и кислорода в фосфате натрия равно
1) 42,1; 18,9; 39,0
2) 18,9; 39,0; 42,1
3) 39,0; 42,1; 18,9
4) 18,9; 42,1; 39,0
5. Количественное содержание элементов калия, фосфора и кислорода в фосфате калия равно
1) 14,6; 30,2; 55,2
2) 30,2; 55,2; 14,6
3) 55,2; 14,6; 30,2
4) 55,2; 30,2; 14,6
6. Количественное содержание элементов алюминия, серы и кислорода в сульфате алюминия равно
1) 15,8; 56,1; 28,1
2) 28,1; 56,1; 15,8
3) 56,1; 15,8; 28,1
4) 15,8; 28,1; 56,1
7. Количественное содержание элементов кальция, углерода и кислорода в карбонате кальция равно
1) 18,0; 48,0; 40,0
2) 48,0; 40,0 18,0
3) 40,0; 48,0; 12,0
4) 40,0 12,0; 48,0
8. Количественное содержание элементов алюминия, фосфора и кислорода в фосфате алюминия равно
1) 22,1; 25,4; 52,5
2) 22,1; 52,5; 25,4
3) 52,5; 25,4; 22,1
4) 25,4; 52,5; 22,1
9. Количественное содержание элементов кальция, азота и кислорода в нитрате кальция равно
1) 24,4; 17,1; 58,5
2) 17,1; 58,5; 24,4
3) 58,5; 24,4; 17,1
4) 24,4; 58,5; 24,4
10. Количественное содержание элементов магния, азота и кислорода в нитрате магния равно
1) 16,2; 64,9; 18,9
2) 16,2; 18,9; 64,9
3) 18,9; 64,9; 16,2
4) 64,9; 16,2; 18,9
Уравнения на массовую долю химического элемента
Ключевые слова конспекта: массовая доля вещества в смеси или растворе, молярная доля вещества, объемная доля вещества, массовая доля элемента в соединении, масса элемента, массовая доля элемента.
Массовую долю вещества в смеси или растворе вычисляют как отношение массы вещества, входящего в состав смеси, к массе всей смеси. Массовую долю часто выражают в процентах. Для этого отношение массы вещества к массе смеси умножают на 100%:
Аналогично объемную долю вещества вычисляют как отношение объема вещества к объему смеси, а молярную долю вещества — как отношение количества вещества одного из компонентов смеси к сумме количеств веществ всех компонентов смеси:
Массовую долю элемента в соединении вычисляют как отношение массы элемента, входящего в состав данного соединения, к массе всего соединения:
Зная молекулярную формулу соединения, массу элемента, входящего в его состав, вычисляют как произведение молярной массы элемента на число атомов этого элемента в соединении.
В этом случае массовую долю элемента в соединении рассчитывают как отношение этой величины к молярной массе всего соединения:
Цитаты из пособия «Задачи по химии 8-9 кл.» (авт. О.С. Габриелян и др.) использованы в учебных целях. Ссылка на покупку книги указана в конце конспекта.
ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ
Задача № 1. 25 г оксида магния смешали с 35 г оксида алюминия. Определите массовую долю оксида магния в данной смеси.
Ответ. ω(MgO) = 0,417, или 41,7%.
Задача № 2. Вычислите объемную долю азота в смеси газов, содержащей 32 л азота, 48 л углекислого газа, 36 л гелия и 14 л водорода.
Ответ. φ(N2) = 0,246, или 24,6%.
Задача № 3. Вычислите молярную и массовую долю (в %) оксида углерода (II) в смеси, содержащей 16,8 л (н. у.) оксида углерода (II) и 13,44 л (н. у.) оксида углерода (IV).
Ответ. χ(СО) = 55,56%, ω(СО) = 44,3%.
Задача № 4. В воде растворили 15 г хлорида натрия. Вычислите массу полученного раствора, если массовая доля соли в нем равна 5%.
Ответ: m(р-ра) = 300 г.
Задача № 5. Образец сплава меди с цинком имеет массу 75 г. Массовая доля меди в этом сплаве равна 64%. Определите массу цинка в данном образце.
Ответ. m(Zn) = 27 г.
[highlight]Задача № 6.[/highlight] Объемная доля аммиака в смеси с кислородом равна 40%. Вычислите плотность данной смеси по воздуху.
Ответ. Dвозд(смеси) = 0,896.
Задача № 7. Найдите массовую долю кислорода в фосфате натрия.
Ответ. ω (O) = 39%.
[highlight]Задача № 8.[/highlight] Определите массовую долю фосфора в смеси, содержащей 55 г фосфата натрия и 70 г дигидрофосфата натрия.
Ответ. ω(Р) = 22,77%
[highlight]Задача № 9.[/highlight] Массовая доля серы в техническом сульфате натрия равна 20,48%. Рассчитайте массовую долю примесей в данном продукте (в %).
Ответ. ω (примесей) = 9,12%.
Задача № 10. Плотность смеси оксида азота (II) и оксида азота (IV) по водороду равна 17,8. Найдите массовую долю оксида азота (IV) в данной смеси.
Ответ. ω(NO2) = 45,2%.
Решение задач с долей вещества в смеси, в соединении. Выберите дальнейшие действия:
http://himi4ka.ru/ogje-2018-po-himii/urok-27-vychislenie-massovoj-doli-himicheskogo-jelementa.html
http://uchitel.pro/%D1%80%D0%B5%D1%88%D0%B5%D0%BD%D0%B8%D0%B5-%D0%B7%D0%B0%D0%B4%D0%B0%D1%87-%D1%81-%D0%B4%D0%BE%D0%BB%D0%B5%D0%B9-%D0%B2%D0%B5%D1%89%D0%B5%D1%81%D1%82%D0%B2%D0%B0-%D0%B2-%D1%81%D0%BC%D0%B5%D1%81%D0%B8/