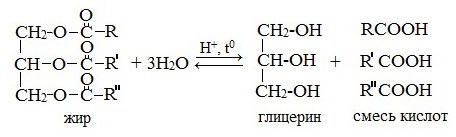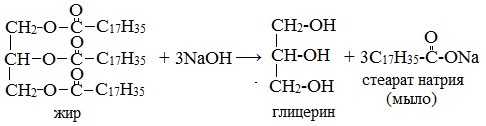Номенклатура жиров
Общее название жиров – триацилглицерины (триглицериды).
Существует несколько способов назвать молекулу жира.
Например, жир, образованный тремя остатками стеариновой кислоты, будет иметь следующие названия:
Физические свойства жиров
Жиры растворимы в органических растворителях и нерастворимы в воде. С водой жиры не смешиваются.
| Животные жиры — предельные | Растительные жиры (масла) — непредельные |
| Твёрдые, образованы предельными кислотами – стеариновой и пальмитиновой. Все животные жиры, кроме рыбьего – твёрдые. | Жидкие, образованы непредельными кислотами – олеиновой, линолевой и другими. Все растительные жиры, кроме пальмового масла – жидкие. |
Химические свойства жиров
1. Гидролиз (омыление) жиров
Жиры подвергаются гидролизу в кислой или щелочной среде или под действием ферментов.
1.1. Кислотный гидролиз
Под действием кислот жиры гидролизуются до глицерина и карбоновых кислот, которых входили в молекулу жира.
| Например, при гидролизе тристеарата глицерина в кислой среде образуется стеариновая кислота и глицерин |
1.2. Щелочной гидролиз — омыление жиров
При щелочном гидролизе жиров образуется глицерин и соли карбоновых кислот, входивших в состав жира.
| Например, при гидролизе тристеарата глицерина гидроксидом натрия образуется стеарат натрия . |
2. Гидрирование (гидрогенизация) ненасыщенных жиров
Гидрогенизация жиров — это процесс присоединения водорода к остаткам непредельных кислот, входящих в состав жира.
При этом остатки непредельных кислот переходят в остатки предельных, жидкие растительные жиры превращаются в твёрдые (маргарин).
| Например, триолеат глицерина при гидрировании превращается в тристеарат глицерина: |
| Количественной характеристикой степени ненасыщенности жиров служит йодное число, показывающее, какая масса йода может присоединиться по двойным связям к 100 г жира. |
3. Мыло и синтетические моющие средства
При щелочном гидролизе жиров образуются мыла – соли высших жирных кислот.
Стеарат натрия – твёрдое мыло.
Стеарат калия – жидкое мыло.
Моющая способность мыла зависит от жесткости воды. Оно хорошо мылится и стирает в мягкой воде, плохо стирает в жёсткой воде и совсем не стирает в морской воде, так как содержащие в ней ионы Ca 2+ и Mg 2+ дают с высшими кислотами нерастворимые в воде соли.
| Например, тристеарат глицерина взаимодействует с сульфатом кальция |
Поэтому наряду с мылом используют синтетические моющие средства.
Их производят из других веществ, например из алкилсульфатов — солей сложных эфиров высших спиртов и серной кислоты.
Спирт реагирует с серной кислотой с образованием алкилсульфата .
Далее алкилсульфат гидролизуется щелочью:
Эти соли содержат в молекуле от 12 до 14 углеродных атомов и обладают очень хорошими моющими свойствами. Кальциевые и магниевые соли этих веществ растворимы в воде, а потому такие мыла моют и в жесткой воде. Алкилсульфаты содержатся во многих стиральных порошках.
Уравнения реакций гидрогенизации жидких жиров
Химические свойства жиров обусловлены наличием:
- сложных эфирных связей;
- двойных связей в углеводородных радикалах жирных кислот;
- наличием глицерина в составе жира.
Гидролиз, или омыление
В зависимости от условий гидролиз бывает:
- кислотный (в присутствии кислоты в качестве катализатора);
- щелочной (под действием щелочей);
- водный (без катализатора, при высоких t 0 и P);
- ферментативный (происходит в живых организмах).
1. Кислотный гидролиз
Жирам как сложным эфирам свойственна обратимая реакция гидролиза, катализируемая минеральными кислотами:
2. Щелочной гидролиз (реакция Шевреля)
При участии щелочей гидролиз жиров происходит необратимо — щелочи превращают образующиеся кислоты в соли и тем самым устраняют возможность взаимодействия кислот с глицерином. Продуктами в этом случае являются мыла — соли высших карбоновых кислот и щелочных металлов:
Натриевые соли — твердые мыла, калиевые — жидкие. Реакция щелочного гидролиза жиров, и вообще всех сложных эфиров, называется также омылением.
3. Водный гидролиз
Промышленный метод гидролиза жиров заключается в обработке их водяным паром при температуре 200 0 С под давлением.
4. Ферментативный гидролиз
В организмах человека и животных жиры, поступающие в составе пищи, подвергаются гидролитическому расщеплению с участием специальных ферментов – липаз.
Гидрогенизация (гидрирование) жидких жиров
Жидкие жиры превращают в твердые путем реакции гидрогенизации (каталитического гидрирования). При этом водород присоединяется по двойной связи, содержащейся в углеводородном радикале молекул масел:
Продукт гидрогенизации масел — твердый жир (искусственное сало, саломас – сало из масла). Маргарин — пищевой жир, состоит из смеси гидрогенизированных масел (подсолнечного, кукурузного, хлопкого и др.), животных жиров, молока и вкусовых добавок (соли, сахара, витаминов и др.).
В условиях процесса гидрогенизации масел (высокая температура, металлический катализатор) происходит изомеризация части кислотных остатков, содержащих цис-связи С=С, в более устойчивые транс-изомеры. Повышенное содержание в маргарине (особенно, в дешевых сортах) остатков транс-ненасыщенных кислот увеличивает опасность атеросклероза, сердечно-сосудистых и других заболеваний.
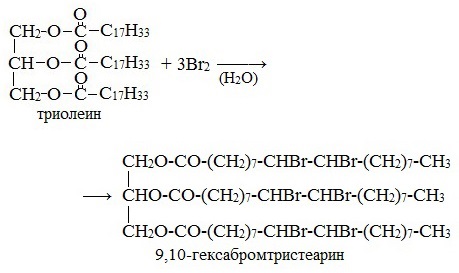
Присоединение галогенов жидкими жирами
Растительные масла обесцвечивают бромною воду:
Реакции окисления и полимеризации (для жидких ненасыщенных жиров)
Жиры, содержащие остатки ненасыщенных кислот (высыхающие масла), под действием кислорода воздуха окисляются и полимеризуются.
При длительном хранении жиры портятся (прогоркают). Под действием воздуха, света и микроорганизмов происходит частичный гидролиз жиров с образованием свободных жирных кислот и продуктов их превращения, обычно имеющих неприятный запах и вкус. Срок годности жиров увеличивается при низкой температуре и в присутствии консервантов (чаще всего поваренной соли).
Гидрирование (гидрогенизация) жиров
Сущность процесса гидрирования заключается в целенаправленном изменении жирнокислотного состава масел и жиров в результате присоединения водорода по двойным связям ненасыщенных жирных кислот.
Гидрированные жиры называют саломасом. В результате изменения жирнокислотного состава происходит изменение свойств масел и жиров: повышаются их температуры плавления, пластичность, твердость, стойкость к окислению и термическому воздействию.
Так, например, гидрирование глицеридов линолевой и линоленовой кислот до глицеридов олеиновой кислоты и ее изомеров (транс-изомер олеиновой кислоты – элаидиновая кислота) в 10…15 раз повышает стойкость жиров к окислению кислородом воздуха. Общий характер зависимости температуры плавления и твердости жиров от содержания насыщенных кислот в их триглицеридах показан на рисунке 1.

При гидрировании происходит также миграция (перемещение) двойных связей в молекулярной цепи жирных кислот (изомеризация), что также заметно влияет на физические и химические свойства жиров.
Гидрированию подвергают соевое, подсолнечное, хлопковое, рапсовое (низкоэруковое) и некоторые другие растительные масла, находящиеся в жидком состоянии, а также животные жиры и свободные жирные кислоты, извлеченные из соапстоков.
Важнейшей областью применения саломасов является производство маргариновой продукции. Здесь используются частично гидрированные растительные масла с температурой плавления 31…34 о С и твердостью 160…320 г/см. Саломасы с температурой плавления 35…37 о С и твердостью 550…750 г/см широко используются в кондитерском и кулинарном производстве. Масла и жиры с высокой степенью гидрирования (tпл. = 40…50 о С) – саломасы технического назначения – находят применение в производстве туалетного и хозяйственного мыла, технических смазок, стеариновой кислоты.
Химические и физико-химические основы гидрирования жиров
Гидрирование жиров всегда проводится в присутствии катализаторов. Химическая сущность процесса гидрирования состоит в присоединении водорода к двойным связям углеводородных радикалов остатков жирных кислот глицеридов:
Гидрирование жиров является гетерогенным процессом и протекает на границе раздела двух фаз жир – катализатор. Скорость таких процессов пропорциональна площади поверхности катализатора. Поэтому для гидрирования применяют катализаторы с высокой удельной поверхностью – 100 м 2 /г и выше.
В начальной стадии процесса гидрирования происходит насыщение поверхности катализатора водородом, или активация катализатора (рисунок 2, а). Это наиболее медленная стадия, поэтому она лимитирует скорость протекания всего процесса.
После насыщения поверхности катализатора водородом процесс гидрирования в общем случае может протекать двумя путями. Активированный катализатор может либо присоединить водород к двойным связям жирных кислот (рисунок 2, б) – в этом случае пройдёт собственно гидрирование; либо одновременно присоединить и оторвать атом водорода – тогда произойдет смещение двойной связи вдоль молекулярной цепи (рисунок 2, в), т.е. осуществится структурная изомеризация. На катализаторе может происходить также и геометрическая (пространственная) цис-, транс-изомеризация жирнокислотных остатков.

Следует отметить, что в отличие от гидрирования реакция изомеризации не требует расхода водорода, поэтому она может протекать и после прекращения его подачи в реакционный аппарат.
Селективность процесса гидрирования
Под селективностью (избирательностью) реакции понимают вероятность ее протекания по одному из нескольких возможных направлений. С этой точки зрения для процесса гидрирования жиров характерны следующие общие закономерности:
- полиненасыщенные жирные кислоты гидрируются ступенчато, т.е. последовательно превращаются в кислоты с меньшим числом двойных связей, например: линоленовая → линолевая → олеиновая → стеариновая;
- скорость гидрирования жирных кислот тем выше, чем больше их ненасыщенность, например, скорость перехода линолевой кислоты в олеиновую в 2…10 раз выше скорости перехода олеиновой кислоты в стеариновую;
- скорость гидрирования практически не зависит от химического строения триглицеридов; скорость гидрирования, например, олеиновой кислоты одинакова в триолеине и в моноолеине.
Если перечисленные основные закономерности соблюдаются полностью, то процесс гидрирования жиров является абсолютно селективным. При абсолютно селективном гидрировании смесей ненасыщенных кислот, например, линолевой и олеиновой, насыщение водородом линолевой кислоты до олеиновой будет предшествовать образованию стеариновой кислоты из олеиновой.
Селективность процесса гидрирования сильно зависит от природы катализатора. Для гидрирования применяют никелевые и никель-медные катализаторы двух видов: дисперсные (порошкообразные) и стационарные (сплавные – в форме гранул или пористой массы). Достоинством дисперсных катализаторов является высокая селективность (94…97 %) и стабильность хода процесса гидрирования, недостатком – трудность отделения катализатора от образовавшегося саломаса. Стационарные катализаторы закреплены в аппаратуре неподвижно и поэтому не требуют по окончании процесса гидрирования специального отделения от саломаса. Недостатками таких катализаторов являются сложность их регенерации и низкая селективность.
Влияние технологических режимов на селективность и скорость гидрирования жиров
Основными технологическими параметрами, определяющими течение процесса гидрирования жиров, являются температура, интенсивность перемешивания, давление водорода. Их влияние на скорость гидрирования жиров в общем виде представлено на рисунке 3.
Температура
Повышение температуры жиров от точки их плавления до ∼180 о С приводит к резкому снижению их вязкости и, соответственно, к повышению скорости диффузии молекул. Соотношение скорости массопереноса и скорости присоединения водорода смещается при этом из диффузной в кинетическую область (рисунок 3, кр. 1), т.е. скорость процесса гидрирования в целом будет определяться скоростью протекания химической реакции.
Максимальная скорость и селективность процесса гидрирования наблюдаются в интервале температур от 180 до 200 о С, при которых и проводится получение пищевого саломаса. Дальнейшее повышение температуры приводит к возрастанию степени адсорбции непредельных соединений на катализаторе и образованию никелевых мыл, что заметно снижает скорость гидрирования жиров (рисунок 3, кр. 1).

Интенсивность перемешивания
С увеличением интенсивности перемешивания скорость гидрирования возрастает до тех пор, пока не достигнет определенного предела. Если скорость подвода молекул реагентов к катализатору ниже скорости присоединения водорода к двойным связям, то реакция протекает в диффузионной области (рисунок 3, кр. 2). В этом случае повышение интенсивности перемешивания приводит к увеличению скорости гидрирования. Если же скорость подвода молекул реагирующих веществ и отвода образующихся продуктов выше скорости присоединения водорода, то реакция протекает в кинетической области, и дальнейшая интенсификация перемешивания не влияет на ее скорость.
Для селективного гидрирования реакцию необходимо проводить в кинетической области, что достигается при интенсивном перемешивании реакционной массы и ее барботировании водородом.
Давление водорода
С повышением давления водорода увеличивается скорость гидрирования жиров, но падает селективность процесса. Для обеспечения высокой селективности процесса при получении пищевого саломаса гидрирование проводят при давлении водорода не более 0,2 МПа. Повышение давления водорода до 3 МПа и более целесообразно при выработке глубокогидрированных саломасов, которые используются для получения технического стеарина или поверхностно-активных веществ. Селективность реакции гидрирования в этом случае значения не имеет.
Побочные процессы при гидрировании
При гидрировании жиров кроме основных реакций присоединения водорода к непредельным жирным кислотам и их изомеризации протекают и побочные реакции, многие из которых обуславливают производственные потери жира. К таким реакциям относятся следующие процессы.
- термодеструкция глицеридов, которая приводит к образованию акролеина СН2=СН—СН=О (токсичен!), быстрополимеризующихся кетенов R–CH=C=O и свободных жирных кислот. Термодеструкция усиливается при температурах более 230 о С и при снижении интенсивности перемешивания реакционной массы.
- гидролиз глицеридов до свободных жирных кислот и глицерина. Основной причиной гидролиза является примесь воды в поступающем водороде.
- термодеструкция гидропероксидов глицеридов жирных кислот приводит к образованию смеси насыщенных и ненасыщенных альдегидов, спиртов и кислот. Характерный для гидрированных жиров «саломасный» запах придает им примесь альдегидов фракции С6–С11 при их наличии в саломасе в количестве всего 10–7 % (!).
- разрушение витаминов. При гидрировании происходит термическое разрушение витамина А, частично – витамина D, но не затрагиваются витамины Е (токоферолы).
Технология гидрирования жиров
Для проведения промышленного гидрирования жиров используются многочисленные технологические схемы, которые могут быть классифицированы следующим образом:
- по характеру движения жирового сырья через реактор различают периодический и непрерывный процессы гидрирования;
- по характеру движения газа через реактор различают гидрирование методом насыщения и гидрирование с внешней циркуляцией водорода. При гидрировании методом насыщения определенное количество водорода, подаваемого в реактор, циркулирует внутри него в течение всего процесса и выводится из аппарата только при его разгрузке. При гидрировании с внешней циркуляцией водорода последний подается в реактор в значительном избытке. Непрореагировавший водород непрерывно выводится из реактора, а затем возвращается в процесс вновь.
- по типу применяемых катализаторов различают гидрирование на суспендированных и стационарных катализаторах. Суспендированный катализатор подается в реактор вместе с жиром и выводится из него вместе с саломасом. Стационарный катализатор закреплен в реакторе и выгружается из него лишь при необратимой потере активности.
В зависимости от назначения вырабатываемого саломаса используют ту или иную технологическую схему производства.
Требования к сырью
Главное требование к сырью, поступающему на гидрирование, – высокая степень очистки жиров от примесей, которые вызывают отравление катализаторов. Наиболее сильное дезактивирующее действие на катализаторы оказывают соединения серы в виде сульфидов, мыла, фосфолипиды, вода, госсипол и его производные.
Даже ничтожные количества серы в виде сульфидов (0,001…0,002 %) быстро и необратимо отравляют катализатор. По этой причине гидрирование рапсового и горчичного масел, которые содержат повышенное количество соединений серы, протекает медленно, с увеличенным расходом катализатора.
Щелочные мыла отравляют катализатор, адсорбируясь на его поверхности. Фосфолипиды сравнительно легко образуют фосфорнокислые соли никеля, разрушая тем самым катализатор гидрирования. Вода в условиях высокотемературного гидрирования стимулирует гидролиз глицеридов и окисление катализатора, что также снижает его активность.
Таким образом, чтобы уменьшить расход катализатора и водорода, снизить температуру гидрирования, уменьшить распад жиров, необходимо гидрируемое сырье и водород максимально освободить от перечисленных примесей. С этой целью проводят рафинацию масел и жиров по полному циклу обработки, а также глубокую сушку жирового сырья, очистку и осушку водорода.
Технологические режимы
Основным элементом промышленных установок для гидрирования жиров является гидрогенизационный аппарат или – чаще – группа (батарея) таких аппаратов. В качестве гидрогенизационного аппарата используют реакторы с мешалками объемом 5…12 м 3 или колонные (вертикальные) барботажные аппараты. По конструкции высота таких колонн в 10…20 раз превышает их внутренний диаметр, который составляет 0,5…0,8 м.
Саломасы для маргариновой продукции получают, главным образом, непрерывным методом в батареях из 3-х реакторов с мешалками при давлении водорода 0,05…0,20 МПа. При этом используют суспендированный никель-кизельгуровый катализатор или смесь из 90…95 % никель-кизельгурового и 5…10 % никель-медного катализаторов. Доля катализатора в гидрируемом сырье составляет 0,1…0,4 %. Температура при переходе из одного реактора в другой повышается от 200 до 240 о С. Расход водорода на всю батарейную установку составляет 700…1000 м 3 /час.
Снижение степени ненасыщенности жирового сырья в установившемся режиме гидрирования сопровождается закономерным и взаимосвязанным изменением свойств получаемого саломаса. Это позволяет контролировать и регулировать ход процесса гидрирования по расходу водорода и по одному из качественных показателей гидрогенизата, например, по изменению температуры плавления или показателя преломления саломаса, величина которого пропорциональна йодному числу продукта. (При гидрировании температура плавления жира возрастает, а величина показателя преломления (йодное число) – снижается).
Саломас, выгружаемый из последнего реактора батарейной установки, охлаждается в теплообменнике до температуры 100…140 о С и направляется на фильтрование. Фильтрование проводится на фильтр-прессах, где происходит отделение саломаса от катализатора, который вновь возвращается в производство (оборотный катализатор). Для поддержания достаточной активности оборотного катализатора к нему добавляют свежий катализатор в соотношении 10 : 1 – 20 : 1.
http://himija-online.ru/organicheskaya-ximiya/zhiry/ximicheskie-svojstva-zhirov.html
http://nomnoms.info/gidrirovanie-gidrogenizatsiya-zhirov/