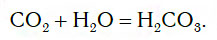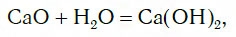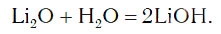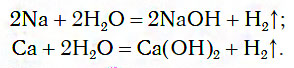Вода: строение и свойства
Вода — строение молекулы, химические и физические свойства. Взаимодействие с простыми веществами (металлами и неметаллами), и со сложными веществами.
Физические свойства
Молекулы воды связаны водородными связями: nH2O = (Н2O)n, поэтому вода жидкая в отличие от ее газообразных аналогов H2S, H2Se и Н2Те.
Химические свойства
1. Вода реагирует с металлами и неметаллами .
1.1. С активными металлами вода реагирует при комнатной температуре с образованием щелочей и водорода :
2Na + 2H2O → 2NaOH + H2
- с магнием реагирует при кипячении:
- алюминий не реагирует с водой, так как покрыт оксидной плёнкой. Алюминий, очищенный от оксидной плёнки, взаимодействует с водой, образуя гидроксид:
- металлы, расположенные в ряду активности от Al до Н , реагируют с водяным паром при высокой температуре, образуя оксиды и водород:
- металлы, расположенные в ряду активности от после Н , не реагируют с водой:
Ag + Н2O ≠
2. Вода реагирует с оксидами щелочных и щелочноземельных металлов , образуя щелочи (с оксидом магния – при кипячении):
3. Вода взаимодействует с кислотными оксидами (кроме SiO2):
4. Некоторые соли реагируют с с водой. Как правило, в таблице растворимости такие соли отмечены прочерком :
Например , сульфид алюминия разлагается водой:
5. Бинарные соединения металлов и неметаллов , которые не являются кислотами и основаниями, разлагаются водой.
Например , фосфид кальция разлагается водой:
6. Бинарные соединения неметаллов также гидролизуются водой.
Например , фосфид хлора (V) разлагается водой:
6. Некоторые органические вещества гидролизуются водой или вступают в реакции присоединения с водой (алкены, алкины, алкадиены, сложные эфиры и др.).
Урок 28. Химические свойства воды
В уроке 28 «Химические свойства воды» из курса «Химия для чайников» узнаем о взаимодействии воды с различными веществами.
При обычных условиях вода является достаточно активным веществом по отношению к другим веществам. Это означает, что со многими из них она вступает в химические реакции.
Взаимодействие с оксидами неметаллов
Если струю газообразного оксида углерода(IV) CO2 (углекислого газа) направить в воду, то часть его растворится в ней (рис. 109).
При этом в растворе протекает химическая реакция соединения, в результате которой образуется новое вещество — угольная кислота H2CO3:
На заметку: Собирая углекислый газ над водой, Дж. Пристли обнаружил, что часть газа растворяется в воде и придает ей приятный терпкий вкус. По сути дела, Пристли впервые получил напиток типа газированной, или содовой, воды.
Реакция соединения происходит также, если к воде прибавить твердый оксид фосфора(V) P2O5. При этом протекает химическая реакция с образованием фосфорной кислоты H3PO4 (рис. 110):
Испытаем растворы, полученные при взаимодействии CO2 и P2O5 с водой, индикатором метиловым оранжевым. Для этого прибавим по 1—2 капли раствора индикатора к полученным растворам. Цвет индикатора изменится с оранжевого на красный, что говорит о присутствии кислот в растворах. Значит, при взаимодействии CO2 и P2O5 с водой действительно образовались кислоты H2CO3 и H3PO4.
Оксиды, подобные CO2 и P2O5, которые при взаимодействии с водой образуют кислоты, относят к кислотным оксидам.
Кислотные оксиды — это оксиды, которым соответствуют кислоты.
Некоторые из кислотных оксидов и соответствующих им кислот приведены в таблице 11. Обратите внимание, что это оксиды элементов неметаллов. Как правило, оксиды неметаллов являются кислотными оксидами.
Взаимодействие с оксидами металлов
С оксидами металлов вода реагирует иначе, чем с оксидами неметаллов.
Исследуем взаимодействие оксида кальция CaO с водой. Для этого поместим в стакан с водой небольшое количество CaO и тщательно перемешаем. При этом протекает химическая реакция:
в результате которой образуется новое вещество Ca(OH)2, относящееся к классу оснований. Таким же образом реагируют с водой оксиды лития, натрия. При этом также образуются основания, например:
Подробнее с основаниями вы познакомитесь в следующем уроке. Оксиды металлов, которым соответствуют основания, называют основными оксидами.
Основные оксиды — это оксиды, которым соответствуют основания.
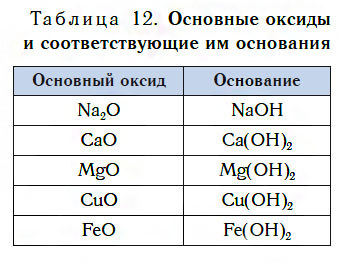
В таблице 12 приведены формулы некоторых основных оксидов и соответствующих им оснований. Заметьте, что, в отличие от кислотных оксидов, в состав основных оксидов входят атомы металлов. Большинство оксидов металлов — это основные оксиды.
Несмотря на то что каждому основному оксиду соответствует основание, не все основные оксиды взаимодействуют с водой, подобно CaO, образуя основания.
Взаимодействие с металлами
При обычных условиях активные металлы (K, Na, Ca, Ba и др.) бурно реагируют с водой:
В этих реакциях выделяется водород и образуются растворимые в воде основания.
Как химически активное вещество вода вступает в реакции со многими другими веществами, но об этом вы узнаете при дальнейшем изучении химии.
Краткие выводы урока:
- Вода — химически активное вещество. Она вступает в реакции с кислотными и основными оксидами, активными металлами.
- При взаимодействии воды с большинством кислотных оксидов образуются соответствующие кислоты.
- Некоторые основные оксиды при реакции с водой образуют растворимые основания.
- При обычных условиях вода реагирует с наиболее активными металлами. При этом образуются растворимые основания и водород.
Надеюсь урок 28 «Химические свойства воды» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Урок. Физические и химические свойства воды
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА ВОДЫ. ПРИМЕНЕНИЕ ВОДЫ
Тема. Физические и химические свойства воды. Применение воды.
— изучить физические и химические свойства воды;
— закрепить умение составлять уравнения реакций, характеризующих химические свойства воды;
— начать формировать представления о важнейших классах неорганических соединений – основаниях (гидроксидах металлов).
Основные вводимые понятия:
Основные виды деятельности учащихся:
— составлять уравнения реакций, характеризующих химические свойства воды;
— уметь определять тип реакции по химическому уравнению;
— уметь объяснить области применения воды;
— выступать с сообщениями, сопровождаемыми презентацией.
Демонстрация №5. Взаимодействие воды с натрием, кальцием, оксидом кальция, оксидом углерода ( IV ), оксидом фосфора ( V ) и испытание полученных растворов индикаторами.
II . Актуализация опорных знаний.
1. Проверка выполнения домашнего задания.
2. Химический диктант:
Молекулярная формула воды …
Формула оксида водорода …
Относительная молекулярная масса воды …
Молярная масса воды …
Температура кипения воды …
Температура замерзания воды …
III . Изучение нового материала.
1. Заслушивание сообщения с презентацией «Три агрегатных состояния воды».
— обучающиеся обсуждают и записывают физические свойства воды.
2. Химические свойства воды.
Химические свойства №1, №3 и №4 рассматриваются на основе демонстрации учителем взаимодействия воды с указанными веществами и испытания полученных растворов индикаторами.
1. Взаимодействие с активными металлами (Li, Na, K, Ca):
2 Na + 2 H 2 O = 2 NaOH + H 2
— вводится понятие «основания».
2. Взаимодействие с металлами средней активности ( Mg , Zn , Fe ):
Mg + H 2 O = MgO + H 2
3. Взаимодействие с оксидами активных металлов (Na 2 O, K 2 O , Ca O ):
— вводится понятие «основания».
4. Взаимодействие с оксидами неметаллов (CO 2 , P 2 O 5 )
— вводится понятие «кислота».
5. Разложение воды под действием электрического тока.
2 H 2 O = 2 H 2 
Задание 1. Определите тип каждой реакции.
Задание 2. Запишите уравнения реакций взаимодействия с водой веществ, указанных в скобках.
3. Применение воды.
Просмотр презентации «Области применения воды».
-обучающиеся составляют конспект после обсуждения рассмотренной информации.
IV . Закрепление изученного материала.
— Вставьте в предложение вместо точек пропущенные слова6
1. Температура замерзания воды равна …
2. Чистая вода — … жидкость.
3. … вода не проводит электрический ток.
4. При разложении воды образуются … и …
5. При взаимодействии активного металла с водой образуется гидроксид металла и …
6. При взаимодействии оксидов … с водой получают кислоты.
V . Подведение итогов урока. Домашнее задание.
Домашнее задание: §32 (с.107-109), тестовые задания 1, 2 (с.109), упр.1 (с. 109).
Краткое описание документа:
На данном уроке обучающиеся знакомятся с физическими и химическими свойствами воды. Проведение химического диктанта позволяет актуализировать важнейшие сведения о воде, изученные на предыдущих уроках.
Изучение нового материала начинается с просмотра презентации «Три агрегатных состояния воды». Затем рассматриваются химические свойства воды, взаимодействие воды с активными металлами, оксидами металлов и неметаллов демонстрируется учителем. обучающиеся по образцу записывают серию уравнений реакций воды с предложенными веществами.
На этапе закрепления учитель предлагает вставить в предложение пропущенные слова.
Курс повышения квалификации
Дистанционное обучение как современный формат преподавания
- Сейчас обучается 924 человека из 80 регионов
Курс повышения квалификации
Инструменты онлайн-обучения на примере программ Zoom, Skype, Microsoft Teams, Bandicam
- Курс добавлен 31.01.2022
- Сейчас обучается 20 человек из 11 регионов
Курс повышения квалификации
Педагогическая деятельность в контексте профессионального стандарта педагога и ФГОС
- Курс добавлен 23.11.2021
- Сейчас обучается 35 человек из 23 регионов
Ищем педагогов в команду «Инфоурок»
Дистанционные курсы для педагогов
«Взбодрись! Нейрогимнастика для успешной учёбы и комфортной жизни»
Свидетельство и скидка на обучение каждому участнику
Найдите материал к любому уроку, указав свой предмет (категорию), класс, учебник и тему:
5 579 152 материала в базе
Самые массовые международные дистанционные
Школьные Инфоконкурсы 2022
33 конкурса для учеников 1–11 классов и дошкольников от проекта «Инфоурок»
Другие материалы
- 25.02.2015
- 1240
- 0
- 25.02.2015
- 1950
- 0
- 25.02.2015
- 463
- 0
- 25.02.2015
- 555
- 0
- 25.02.2015
- 535
- 0
- 25.02.2015
- 816
- 0
- 25.02.2015
- 1021
- 0
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
Добавить в избранное
- 25.02.2015 2131
- DOCX 17.8 кбайт
- 44 скачивания
- Рейтинг: 5 из 5
- Оцените материал:
Настоящий материал опубликован пользователем Стулень Ольга Гавриловна. Инфоурок является информационным посредником и предоставляет пользователям возможность размещать на сайте методические материалы. Всю ответственность за опубликованные материалы, содержащиеся в них сведения, а также за соблюдение авторских прав несут пользователи, загрузившие материал на сайт
Если Вы считаете, что материал нарушает авторские права либо по каким-то другим причинам должен быть удален с сайта, Вы можете оставить жалобу на материал.
Автор материала
- На сайте: 6 лет и 11 месяцев
- Подписчики: 0
- Всего просмотров: 15617
- Всего материалов: 11
Московский институт профессиональной
переподготовки и повышения
квалификации педагогов
Дистанционные курсы
для педагогов
663 курса от 690 рублей
Выбрать курс со скидкой
Выдаём документы
установленного образца!
Учителя о ЕГЭ: секреты успешной подготовки
Время чтения: 11 минут
Полный перевод школ на дистанционное обучение не планируется
Время чтения: 1 минута
Тринадцатилетняя школьница из Индии разработала приложение против буллинга
Время чтения: 1 минута
Инфоурок стал резидентом Сколково
Время чтения: 2 минуты
Профессия педагога на третьем месте по популярности среди абитуриентов
Время чтения: 1 минута
ЕГЭ в 2022 году будут сдавать почти 737 тыс. человек
Время чтения: 2 минуты
В Ленобласти школьники 5-11-х классов вернутся к очному обучению с 21 февраля
Время чтения: 1 минута
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.
http://himi4ka.ru/arhiv-urokov/urok-28-himicheskie-svojstva-vody.html
http://infourok.ru/urok._fizicheskie_i_himicheskie_svoystva_vody-411002.htm