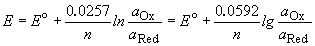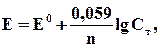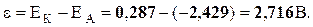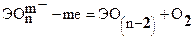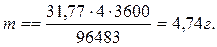Уравнения реакций протекающих в гальванических элементах
Для гальванического элемента принята следующая форма записи (на примере элемента Даниэля):
где вертикальная линия | обозначает границу раздела фаз, а двойная вертикальная линия || — солевой мостик. Электрод, на котором происходит окисление, называется анодом; электрод, на котором происходит восстановление, называется катодом. Гальванический элемент принято записывать так, чтобы анод находился слева.
Электродные полуреакции принято записывать как реакции восстановления (таблица 12.1), поэтому общая реакция в гальваническом элементе записывается как разность между реакциями на правом и левом электродах:
Правый электрод: Cu 2+ + 2e = Cu
Левый электрод: Zn 2+ + 2e = Zn
Общая реакция: Cu 2+ + Zn = Cu + Zn 2+
Потенциал E электрода рассчитывается по формуле Нернста:
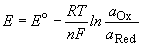
где aOx и aRed — активности окисленной и восстановленной форм вещества, участвующего в полуреакции; E o — стандартный потенциал электрода (при aOx = aRed =1); n — число электронов, участвующих в полуреакции; R — газовая постоянная; T — абсолютная температура; F — постоянная Фарадея. При 25 o C
Стандартные электродные потенциалы электродов измеряются относительно стандартного водородного электрода, потенциал которого принят равным нулю. Значения некоторых стандартных электродных потенциалов приведены в таблице 12.1.
Электродвижущая сила (ЭДС) элемента равна разности потенциалов правого и левого электродов:
Если ЭДС элемента положительна, то реакция (так, как она записана в элементе) протекает самопроизвольно. Если ЭДС отрицательна, то самопроизвольно протекает обратная реакция.
Стандартная ЭДС равна разности стандартных потенциалов:
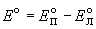
Для элемента Даниэля стандартная ЭДС равна
E o = E o (Cu 2+ /Cu) — E o (Zn 2+ /Zn) = +0.337 — (-0.763) = +1.100 В.
ЭДС элемента связана с 

Зная стандартную ЭДС, можно рассчитать константу равновесия протекающей в элементе реакции:
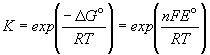
Константа равновесия реакции, протекающей в элементе Даниэля, равна
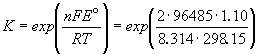
Зная температурный коэффициент ЭДС 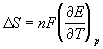




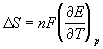
Таблица 12.1. Стандартные электродные потенциалы при 25 o С.
Электрод
Электродная реакция
E o , В
PbSO4 + 2H2O
Пример 12-1. Рассчитать стандартный электродный потенциал пары Cu 2+ /Cu + по данным таблицы 11.1 для пар Cu 2+ /Cu и Cu + /Cu.
Cu 2+ + 2e = Cu 
Cu + + e = Cu 
Cu 2+ + e = Cu + 
откуда E o = +0.153 В.
Пример 12-2. Составить схему гальванического элемента, в котором протекает реакция
Рассчитать стандартную ЭДС элемента при 25 o C, 
Ag | AgBr| Br — || Ag + | Ag
Правый электрод: Ag + + e = Ag E o = 0.7792 В
Левый электрод: AgBr + e = Ag + Br — E o = 0.0732 В
Общая реакция: Ag + + Br — = AgBr E o = 0.7260 В

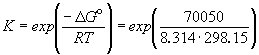
1/K= a(Ag + ) . a(Br — ) = m(Ag + ) . m(Br — ) . ( 



Отсюда, полагая 

Пример 12-3. 

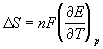



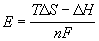
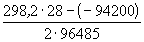
Ответ. 
12-1. Рассчитать стандартный электродный потенциал пары Fe 3+ /Fe по данным таблицы 12.1 для пар Fe 2+ /Fe и Fe 3+ /Fe 2+ . (ответ)
12-2. Рассчитать произведение растворимости и растворимость AgCl в воде при 25 o C по данным таблицы 12.1. (ответ)
12-3. Рассчитать произведение растворимости и растворимость Hg2Cl2 в воде при 25 o C по данным о стандартных электродных потенциалах. (ответ)
12-4. Рассчитать константу равновесия реакции диспропорционирования 2Cu + 
12-5. Рассчитать константу равновесия реакции ZnSO4 + Cd = CdSO4 + Zn при 25 o C по данным о стандартных электродных потенциалах. (ответ)
12-6. ЭДС элемента, в котором обратимо протекает реакция 0.5 Hg2Cl2 + Ag = AgCl + Hg, равна 0.456 В при 298 К и 0.439 В при 293 К. Рассчитать 


12-7. Вычислить тепловой эффект реакции Zn + 2AgCl = ZnCl2 + 2Ag, протекающей в гальваническом элементе при 273 К, если ЭДС элемента E= 1.015 В и температурный коэффициент ЭДС = — 4.02 . 10 -4 В . K -1 . (ответ)
12-8. В гальваническом элементе при температуре 298 К обратимо протекает реакция Cd + 2AgCl = CdCl2 + 2Ag. Рассчитать изменение энтропии реакции, если стандартная ЭДС элемента E o = 0.6753 В, а стандартные энтальпии образования CdCl2 и AgCl равны -389.7 и -126.9 кДж . моль -1 соответственно. (ответ)
12-9. ЭДС элемента Pt | H2 | HCl | AgCl | Ag при 25 o C равна 0.322 В. Чему равен pH раствора HCl . (ответ)
12-10. Растворимость Cu3(PO4)2 в воде при 25 o C равна 1.6 . 10 -8 моль . кг -1 . Рассчитать ЭДС элемента Pt | H2 | HCl (pH = 0) | Cu3(PO4)2 (насыщ. р-р) | Cu при 25 o C. (ответ)
12-11. Три гальванических элемента имеют стандартную ЭДС соответственно 0.01, 0.1 и 1.0 В при 25 o C. Рассчитать константы равновесия реакций, протекающих в этих элементах, если количество электронов для каждой реакции n = 1. (ответ)
12-12. ЭДС элемента Pt | H2 | HBr | AgBr | Ag в широком интервале температур описывается уравнением: E o (В) = 0.07131 — 4.99 . 10 -4 (T — 298) — 3.45 . 10 -6 (T — 298) 2 . Рассчитать 


12-13. Для измерения pH раствора можно применять хингидронный электрод. (Хингидрон, Q . QH2, представляет собой комплекс хинона, Q = C6H4O2, и гидрохинона, QH2 = C6H4O2H2). Электродная полуреакция записывается как Q + 2H + + 2e 
12-14. В гальваническом элементе обратимо протекает реакция CuSO4 + Zn = ZnSO4 + Cu. Рассчитать 

12-15. В элементе Вестона протекает реакция Cd + Hg2SO4 = Cd 2+ + 2Hg. Рассчитать ЭДС этого элемента при 303 K, если 

12-16. 


Сервер создается при поддержке Российского фонда фундаментальных исследований
Не разрешается копирование материалов и размещение на других Web-сайтах
Вебдизайн: Copyright (C) И. Миняйлова и В. Миняйлов
Copyright (C) Химический факультет МГУ
Написать письмо редактору
СХЕМА РАБОТЫ ГАЛЬВАНИЧЕСКОГО ЭЛЕМЕНТА И ТИПОВЫЕ ЗАДАЧИ
Фундаментальные законы физики и химии, и в том числе, закон сохранения массы и энергии вещества, находят свое подтверждение на уровне перемещения мельчайших частиц – электронов, массами которых в химии обычно пренебрегают.
Речь идет об окислительно-восстановительных процессах, сопровождающихся переходом электронов от одних веществ (восстановителей) к другим (окислителям). Причем вещества могут обмениваться электронами, непосредственно соприкасаясь друг с другом.
Однако существует множество случаев, когда прямого контакта веществ не происходит, а процесс окисления-восстановления все равно идет. А если он идет самопроизвольно, то при этом еще и энергия выделяется. Ее человек с успехом использует для выполнения электрической работы.
Реализуется такая возможность в гальваническом элементе, схема работы которого, а также расчеты, связанные с ним, рассматриваются в данной статье.
Простейший гальванический элемент: схема работы
Гальванический элемент – это прибор, позволяющий при посредстве химической реакции получить электрическую энергию.
Пластинка металла и вода: простые взаимоотношения
Давайте сначала разберемся, что происходит с пластинкой металла, если опустить ее в воду?
Процесс схож с диссоциацией соли: диполи воды ориентируются к ионам металла и извлекают их из пластины. Но почему же тогда не происходит растворения самой пластины в воде? Все дело в строении кристаллической решетки.
Кристаллы соли состоят из катионов и анионов, поэтому диполями воды извлекаются из решетки и те, и другие.
У металла же кристаллическая решетка представлена атомами-ионами. Внутри нее всегда происходит превращение атомов в катионы за счет отщепления валентных электронов и обратный процесс: катионы снова превращаются в атомы, присоединяя электроны. Электроны являются общими для всех ионов и атомов, присутствующих в кристаллической решетке металла.
Процессы внутри металлической кристаллической решетки в обобщенном виде можно показать так:
В итоге, вода, окружающая пластинку – это уже не собственно вода, а раствор, составленный из молекул воды и перешедших в нее из пластины ионов металла. На пластине же возникает избыток электронов, которые скапливаются у ее поверхности, так как сюда притягиваются гидратированные катионы металла.
Возникает так называемый двойной электрический слой.
Бесконечно катионы металла с пластины в раствор уходить не будут, поскольку существует и обратный процесс: переход катионов из раствора на пластину. И он будет идти до тех пор, пока не наступит динамическое равновесие:
На границе раздела «металлическая пластина – раствор» возникает разность потенциала, которая называется равновесным электродным потенциалом металла.
Пластинка металла и раствор его соли: к чему приводит такое соседство
А что произойдет, если металлическую пластинку поместить не в воду, а в раствор соли этого же металла, например, цинковую пластинку Zn в раствор сульфата цинка ZnSO4?
В растворе сульфата цинка уже присутствуют катионы цинка Zn 2+ . Таким образом, при погружении в него цинковой пластины возникнет избыточное количество этих катионов, и уже известное нам равновесие (см. выше) сместится влево. Все это приведет к тому, что отрицательный заряд на пластинке будет иметь меньшее значение, так как меньшее количество катионов с нее будет переходить в раствор. Как результат – более быстрое наступление равновесия и менее значительный скачок потенциала.
Потенциал металла в растворе его же соли в момент равновесия записывают так:
Металл, погруженный в раствор электролита, называют электродом, обратимым относительно катиона.
Цинк – достаточно активный металл. А если речь будет идти о медной пластинке Cu, погруженной в раствор, например, сульфата меди (II) CuSO4?
Медь – металл малоактивный. Двойной электрический слой, конечно же, появится и в этом случае. Но! Катионы из пластинки в раствор переходить не будут. Наоборот, катионы меди (II) Cu 2+ из раствора соли начнут встраиваться в кристаллическую решетку пластинки и создавать положительный заряд на ее поверхности. Сюда же подойдут сульфат-анионы SO4 2- и создадут вокруг нее отрицательный заряд. То есть распределение зарядов в данном случае будет совершенно противоположным, чем на цинковой пластинке.
Это общая закономерность: пластинки из малоактивных металлов при погружении в раствор их солей всегда заряжаются положительно.
Как устроен гальванический элемент Даниэля-Якоби, или Так где же все-таки электрический ток?
Известно, что электрический ток – это направленное движение заряженных частиц (электронов).
На активном металле скапливаются электроны, а поверхность малоактивного металла, заряжается положительно. Если соединить проводником (например, металлической проволокой) оба металла, то электроны с одного перейдут на другой, а двойной электрический слой перестанет существовать. Это будет означать возникновение электрического тока.
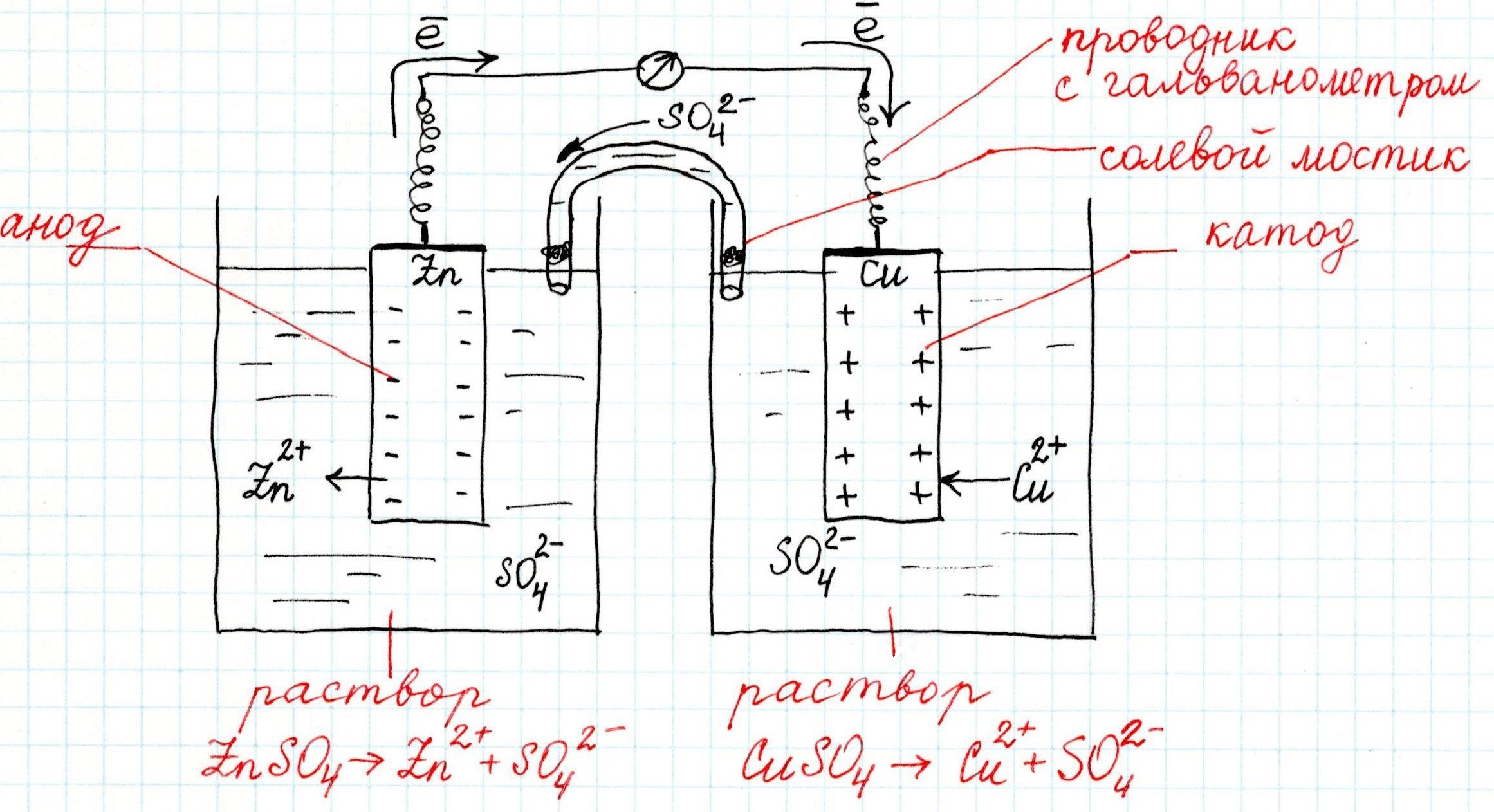
Причем, ток возникает за счет окислительно-восстановительного процесса: активный металл окисляется (так как отдает электроны малоактивному), а малоактивный металл восстанавливается (так как принимает электроны от активного). Металлы друг с другом не соприкасаются, а взаимодействуют через посредника: внешнего проводника. Данная схема и есть схема гальванического элемента. Именно так устроен и работает гальванический элемент Даниэля-Якоби:
В схеме элемента показан «солевой мостик». Он представляет собой трубку, в которой присутствует электролит, не способный взаимодействовать ни с электродами (катодом или анодом), ни с электролитами в пространствах у электродов. Например, это может быть раствор сульфата натрия Na2SO4. Подобный мостик нужен для того, чтобы уравновешивать (нейтрализовать) заряды, образующиеся в растворах гальванического элемента.
Таким образом, возникшая электрическая цепь замыкается: анод → проводник с гальванометром → катод → раствор в катодном пространстве → «солевой мостик» → раствор в анодном пространстве → анод.
Анод – электрод, на котором происходит окисление (цинковая пластинка):
Электроны цинка Zn отправляются по внешней цепи (то есть по проводнику) на катод.
Катод – электрод, на котором происходит восстановление (медная пластинка):
Катионы меди Cu 2+ , пришедшие на пластинку из раствора сульфата меди (II), получают электроны цинкового анода.
В общем виде весь процесс окисления-восстановления в гальваническом элементе выглядит так:
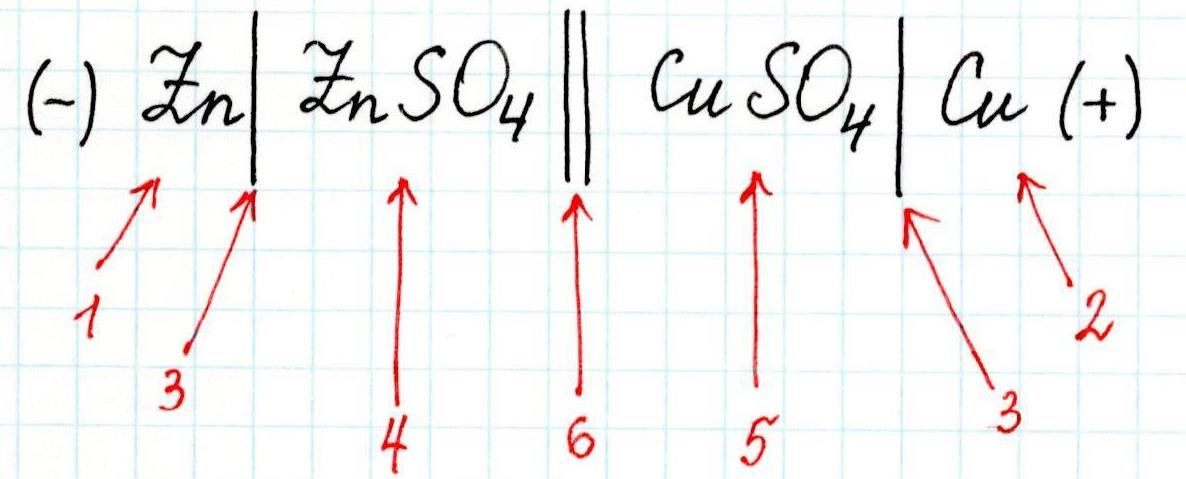
Для любого гальванического элемента можно составить запись в виде схемы. Например, для приведенного элемента Даниэля-Якоби она будет выглядеть так:
3 – скачок потенциала (граница раздела фаз);
4 – электролит в анодном пространстве;
5 – электролит в катодном пространстве;
6 – граница между растворами (солевой мостик).
Или сокращенно:
Типовые задачи на схему гальванического элемента: примеры решения
По вопросу, рассмотренному в данной статье, возможны два основных вида задач.
Задача 1. Составьте схему гальванического элемента, в котором протекает реакция:

Задача 2. Напишите электродные и суммарные уравнения реакций, протекающих в гальваническом элементе:

Итак, разобрав принцип работы гальванического элемента, мы научились записывать схему его работы и определять основные процессы на электродах.
Гальванический элемент
Гальванический элемент – это устройство, способное преобразовывать свободную энергию Гиббса окислительно-восстановительной реакции в электрическую.
Элемент состоит из двух электродов (например, цинк и медь), опущенных в растворы собственных солей (или другого электролита) и соединенных проводником.
Растворы солей также приведены в электрический контакт полупроницаемой мембраной или электролитическим ключом в виде стеклянной трубки, заполненной насыщенным раствором КСl.
При этом через проводник протекает электронный ток, а на электродах в растворе электролита протекают окислительно-восстановительные реакции. На внутреннем участке электрической цепи гальванического элемента (растворы солей и насыщенный раствор КСl) протекает ионный ток.
Например, для элемента Даниэля-Якоби:
– на аноде Zn 0 -2e=Zn 2+ – окисление;
– на катоде Cu 2+ +2e=Cu 0 – восстановление.
Уравнение токообразующей реакции:
Zn 0 + Cu 2+ =Zn 2+ +Cu 0 .
Схема гальванического элемента: 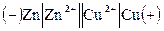
Электродвижущая сила (ЭДС) гальванического элемента (ε) выражается разностью установившихся электродных потенциалов катода и анода:
При стандартных условиях (при погружении металла в раствор собственного иона с одномоляльной концентрацией при температуре Т=25°С), электродный потенциал металла равен его стандартному электродному потенциалу (прил. 6).
В условиях, отличающихся от стандартных, электродный потенциал металла (Е) зависит от концентрации его ионов в растворе (при постоянной температуре), что выражается уравнением Нернста:
где Е 0 — стандартный электродный потенциал, В; n – число электронов, принимающих участие в процессе (заряд иона); Сm – моляльная концентрация (активность) гидратированных ионов металла в растворе, моль/кг Н2О.
Пример 1. Составьте схемы двух гальванических элементов, в одном из которых металл был бы катодом, а в другом – анодом. Напишите уравнения реакций, протекающих на электродах в гальванических элементах. Определите ЭДС элементов при температуре 298 К, если активность ионов обоих металлов в первом элементе равна 0,01 моль/кг Н2О, а в другом 1,0 моль/кг Н2О.
Решение.Металл – медь. Составим элемент, в котором медный электрод является катодом. Анодом можно выбрать любой металл, имеющий меньший электродный потенциал, например – магний.
Схема гальванического элемента: (-) Mg/ Mg 2+ //Cu 2+ /Cu (+).
Реакция на катоде: Cu 2+ (водн.) +2e=Cu(тв.)
Уравнение токообразующей реакции:
Значения потенциалов электродов рассчитаем по уравнению Нернста:
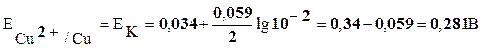
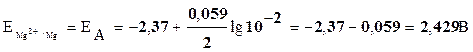
Составим элемент, в котором медный электрод является анодом. Катодом можно выбрать любой металл, имеющий больший электродный потенциал, например, ртуть:
(-)Cu / Cu 2+ //Hg 2+ / Hg (+).
Запишем уравнение реакций:
Так как активность ионов металла в растворах равна 1 моль/кг воды, то в данном элементе оба значения потенциалов – стандартные:
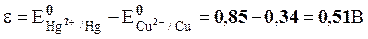
Электролиз
Электролизом называется процесс раздельного окисления и восстановления на электродах, опущенных в раствор электролита, осуществляемый за счет протекания тока от внешнего источника ЭДС. При этом на аноде происходит окисление, а на катоде – восстановление и выделение металла. При электролизе расплавов электролитов на катоде всегда протекает восстановление катионов:
На аноде – окисление соответствующих анионов:
Аn m— — me — = Аn 0
Как правило, анодный процесс сопровождается вторичными химическими реакциями – рекомбинацией атомов в молекулы:
либо распадом нейтральной сложной частицы на два вещества, одно из которых является простым:
Пример 1.Написать уравнения процессов, происходящих при электролизе расплава фторида алюминия AlF3 (материал катода – алюминий, материал анода – графит).
В расплаве AlF3 диссоциирует согласно уравнению:
Под действием электрического поля катионы Al 3+ движутся к катоду и принимают от него электроны:
Al 3+ + 3е — → Al 0 – процесс восстановления.
Анионы F — движутся к аноду и отдают электроны:
F — — е — → F 0 – процесс окисления,


|
В растворах электролитов электролиз осложняется возможностью участия молекул растворителя (например, воды) в электродных процессах. Если система, в которой проводят электролиз, содержит разные окислители, то на катоде будет восстанавливаться наиболее активный из них, т.е., окисленная форма той электрохимической системы, которой отвечает наибольшее значение электродного потенциала.
В зависимости от состава электролита на катоде могут протекать (в том числе и параллельно) следующие реакции:
1) восстановление катионов металла:
2) восстановление молекул воды:
Первая реакция исключительно протекает в растворах солей только тех металлов, которые в ряду напряжения находятся после водорода, то есть имеют больший, по сравнению с водородом электродный потенциал.
Вторая – только в растворах наиболее активных металлов, находящихся в начале ряда напряжений вплоть до алюминия. Их электродный потенциал значительно отрицательнее потенциала водородного электрода в нейтральной водной среде (-0,41 В). Для растворов солей металлов, имеющих электродный потенциал, близкий к -0,41 В, и составляющих середину ряда напряжений, характерно протекание обеих катодных реакций.
В растворах кислот на катоде протекает водородная реакция:
Следует отметить, что в качестве катода можно использовать любой токопроводящий материал, кроме наиболее активных щелочных и щелочноземельных металлов. Большинство других металлов, а также графит, устойчиво в любых электролитах при катодном заряжении.
Аналогично, при наличии в системе, подвергающейся электролизу, нескольких восстановителей, на аноде будет окисляться наиболее активный из них, т.е. восстановленная форма той электрохимической системы, которая характеризуется наименьшим значением электродного потенциала. На аноде может протекать несколько окислительных процессов:
1) растворение материала анода (кроме платины и графита):
2) окисление анионов соли или кислоты
Аn m— — me — = Аn 0
3) окисление молекул воды:
На нерастворимых анодах (платина, графит и некоторые металлы, образующие на своей поверхности защитную токопроводящую оксидную пленку, например, Pb в растворе Н2SО4 образует PbО2) конкурируют реакции 2 и 3. Для бескислородных кислот и их солей предпочтительнее реакция 2, например:
В растворах кислородных кислот и их солей, а также фторидов металлов протекает исключительно реакция окисления молекул воды.
В водных растворах щелочей на нерастворимых анодах протекает гидроксильная реакция:
Пример 2.Написать уравнения процессов, происходящих при электролизе раствора хлорида меди (анод – черновая медная пластина).
Решение.Если анод изготовлен из металла, способного окисляться в условиях электролиза, как в данном случае, ионы из раствора на аноде не окисляются.Медь окисляется на аноде (черновая медная пластина) с переходом ионов меди в раствор: Cu 0 -2e=Cu 2+ ,а на катоде выделяется чистая медь из раствора: Cu 2+ + 2e= Cu 0 . Суммарного уравнения электролиза, как правило, в этом случае не пишут.
Пример 3.Написать уравнения процессов, происходящих при электролизе водного раствора сульфата натрия (анод платиновый).
Решение.Стандартный электродный потенциал системы
Na + + е — → Na 0 (-2,71 В)
значительно отрицательнее потенциала водородного электрода в нейтральной водной среде (-0,41 В). Поэтому на катоде будет происходить электрохимическое восстановление воды, сопровождающееся выделением водорода:
а ионы Na + , приходящие к катоду, будут накапливаться в прилегающей к нему части раствора (катодное пространство)
На аноде будет происходить электрохимическое окисление воды, сопровождающееся выделением кислорода
поскольку отвечающий этой системе стандартный электродный потенциал (1,23В) значительно ниже, чем стандартный электродный потенциал (2,01 В), характеризующий систему
Ионы SО4 2- , движущиеся при электролизе к аноду, будут накапливаться в анодном пространстве.
Умножая уравнение катодного процесса на два и складывая с уравнением анодного процесса, получаем суммарное уравнение процесса:
 |  |





 |  |
 |

Количественно электролиз описывается двумя законами Фарадея:
1. Масса выделяющегося на электроде вещества пропорциональна количеству прошедшего электричества:
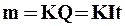
где Q – количество электричества (заряд); I – сила тока; t – время протекания тока.
Если Q=1Кл, то К=m. Масса вещества, выделяющаяся при прохождении 1 Кл электричества, называется электрохимическим эквивалентом.
2. Для выделения на электроде одного эквивалента любого вещества необходимо затратить одно и то же количество электричества, равное постоянной Фарадея F=96483 Кл/моль.
Обобщенное выражение законов Фарадея:
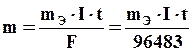
где m –масса вещества, г; mЭ– эквивалентная масса вещества, г/моль; I – сила тока, А; t – продолжительность электролиза, с.
Пример 4.Какая масса меди выделится на катоде при электролизе раствора CuSO4 в течение 1 ч, если сила тока равна 4 А?
Решение.Воспользуемся формулой (11.1). Эквивалентная масса mЭ меди в CuSO4 равна 63,54:2=31,77 г/моль; t=60*60=3600 c.
Подставив в формулу численные значения, получим
Пример 5.Вычислите эквивалентную массу металла, зная, что при электролизе раствора хлорида этого металла затрачено 38600 Кл электричества и на катоде выделилось 11,742 г металла.
Решение. Из формулы (11.1) имеем
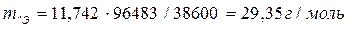
где m=11,742 г, I×t=Q=38600 Кл.
http://himzadacha.ru/sxema-raboty-galvanicheskogo-elementa-i-tipovye-zadachi/
http://helpiks.org/6-46278.html