Уравнения реакций взаимодействия металлов с растворами кислот
ОТНОШЕНИЕ МЕТАЛЛОВ К КИСЛОТАМ
Чаще всего в химической практике используются такие сильные кислоты как серная H 2 SO 4 , соляная HCl и азотная HNO 3 . Далее рассмотрим отношение различных металлов к перечисленным кислотам.
Соляная кислота – это техническое название хлороводородной кислоты. Получают ее путем растворения в воде газообразного хлороводорода – HCl . Ввиду невысокой его растворимости в воде, концентрация соляной кислоты при обычных условиях не превышает 38%. Поэтому независимо от концентрации соляной кислоты процесс диссоциации ее молекул в водном растворе протекает активно:
HCl 
Образующиеся в этом процессе ионы водорода H + выполняют роль окислителя, окисляя металлы, расположенные в ряду активности левее водорода. Взаимодействие протекает по схеме:
Me + HCl 
При этом соль представляет собой хлорид металла ( NiCl 2 , CaCl 2 , AlCl 3 ), в котором число хлорид-ионов соответствует степени окисления металла.
Соляная кислота является слабым окислителем, поэтому металлы с переменной валентностью окисляются ей до низших положительных степеней окисления:
2 Al + 6 HCl → 2 AlCl 3 + 3 H 2 ↑
2│ Al 0 – 3 e — → Al 3+ — окисление
3│2 H + + 2 e — → H 2 – восстановление
Соляная кислота пассивирует свинец ( Pb ). Пассивация свинца обусловлена образованием на его поверхности трудно растворимого в воде хлорида свинца ( II ), который защищает металл от дальнейшего воздействия кислоты:
В промышленности получают серную кислоту очень высокой концентрации (до 98%). Следует учитывать различие окислительных свойств разбавленного раствора и концентрированной серной кислоты по отношению к металлам.
Разбавленная серная кислота
В разбавленном водном растворе серной кислоты большинство ее молекул диссоциируют:
H2SO4 
HSO4 — 
Образующиеся ионы Н + выполняют функцию окислителя.
Как и соляная кислота, разбавленный раствор серной кислоты взаимодействует только с металлами активными и средней активности (расположенными в ряду активности до водорода).
Химическая реакция протекает по схеме:
1│2Al 0 – 6e — → 2Al 3+ — окисление
3│2 H + + 2 e — → H 2 – восстановление
Металлы с переменной валентностью окисляются разбавленным раствором серной кислоты до низших положительных степеней окисления:
Свинец ( Pb ) не растворяется в серной кислоте (если ее концентрация ниже 80%) , так как образующаяся соль PbSO 4 нерастворима и создает на поверхности металла защитную пленку.
Концентрированная серная кислота
В концентрированном растворе серной кислоты (выше 68%) большинство молекул находятся в недиссоциированном состоянии, поэтому функцию окислителя выполняет сера, находящаяся в высшей степени окисления ( S +6 ). Концентрированная H 2 SO 4 окисляет все металлы, стандартный электродный потенциал которых меньше потенциала окислителя – сульфат-иона SO 4 2- (0,36 В). В связи с этим, с концентрированной серной кислотой реагируют и некоторые малоактивные металлы.
Процесс взаимодействия металлов с концентрированной серной кислотой в большинстве случаев протекает по схеме:
Me + H 2 SO 4 (конц.) 
Продуктами восстановления серной кислоты могут быть следующие соединения серы:
Практика показала, что при взаимодействии металла с концентрированной серной кислотой выделяется смесь продуктов восстановления, состоящая из H 2 S , S и SO 2. Однако, один из этих продуктов образуется в преобладающем количестве. Природа основного продукта определяется активностью металла: чем выше активность, тем глубже процесс восстановления серы в серной кислоте.
Взаимодействие металлов различной активности с концентрированной серной кислотой можно представить схемой:
Алюминий ( Al ) и железо ( Fe ) не реагируют с холодной концентрированной H 2 SO 4 , покрываясь плотными оксидными пленками, однако при нагревании реакция протекает.
Концентрированная серная кислота является сильным окислителем, поэтому при взаимодействии с ней металлов, обладающих переменной валентностью, последние окисляются до более высоких степеней окисления, чем в случае с разбавленным раствором кислоты:
Химические свойства кислот
О чем эта статья:
8 класс, 9 класс, ЕГЭ/ОГЭ
Кислоты — это сложные химические вещества, состоящие из одного или нескольких атомов водорода, способных замещаться атомами металла, и кислотных остатков.
Рассмотрим подробнее общие свойства кислот.
Диссоциация
Кислоты — это электролиты, которые при диссоциации образуют катионы водорода и анионы кислотного остатка. Диссоциация кислот происходит ступенчато. По способности к диссоциации кислоты разделяют на две группы:
Хорошо диссоциирующие (сильные): H2SO4, HCl, HBr, HNO3, HClO4, HI.
Разложение
В результате реакций разложения кислородсодержащих кислот образуются кислотный оксид и вода. Бескислородные кислоты образуют простые вещества. Для разложения некоторых кислот необходимо нагревание или излучение (HCl, HNO3, H3PO4) другие же разлагаются самопроизвольно в момент образования (H2CO3, H2SO3, HNO2).
Взаимодействие кислот с металлами
Металл может вытеснять водород из кислоты только в том случае, если металл стоит левее водорода в ряду активности металлов. Продукты реакции — соль и водород.
При взаимодействии с кислотами-окислителями, например, азотной, образуется продукт восстановления кислоты, хотя протекание реакции также неоднозначно.
Высокая окислительная способность серной и азотной кислот позволяет им вступать в реакции с металлами. Продукты реакции будут зависеть от активности металла и от концентрации кислот.
Таблица: химические свойства кислот-окислителей
На холоду — пассивация
На холоду — пассивация
Реакция не проходит
На холоду — пассивация
На холоду — пассивация
Взаимодействие кислот с основаниями
Кислоты реагируют с основаниями и амфотерными гидроксидами, в результате образуются соль и вода. Взаимодействие кислот с основаниями называют реакцией нейтрализации.
NaOH + HCl = NaCl + H2O
Взаимодействие кислот с солями
Сильные кислоты вытесняют слабые из растворов их солей, при этом образуются новая соль и новая кислота. Условие протекания реакции кислот с солями — одним из продуктов реакции должны быть нерастворимая соль или слабая кислота, вода, газ.
Взаимодействие кислот с основными и амфотерными оксидами
Кислоты вступают в реакцию с основными и амфотерными оксидами (последние ведут себя как основные оксиды). В результате реакции образуется соль и вода.
Восстановительные свойства бескислородных кислот
Бескислородные кислоты (кроме HF) проявляют восстановительные свойства за счет химического элемента, который входит в состав аниона, при действии на них различных окислителей.
Например, в качестве окислителей для всех галогеноводородных кислот выступают диоксид марганца MnO2, перманганат калия KMnO4, дихромат калия K2Cr2O7.
Результат этих реакций — образование свободных галогенов.
Из галогеноводородных кислот наибольшая восстановительная активность — у йодоводородной. Ее могут окислять оксид железа (III) и соль трехвалентного железа.
Высокая восстановительная активность характерна для сероводородной кислоты, она может быть окислена диоксидом серы.
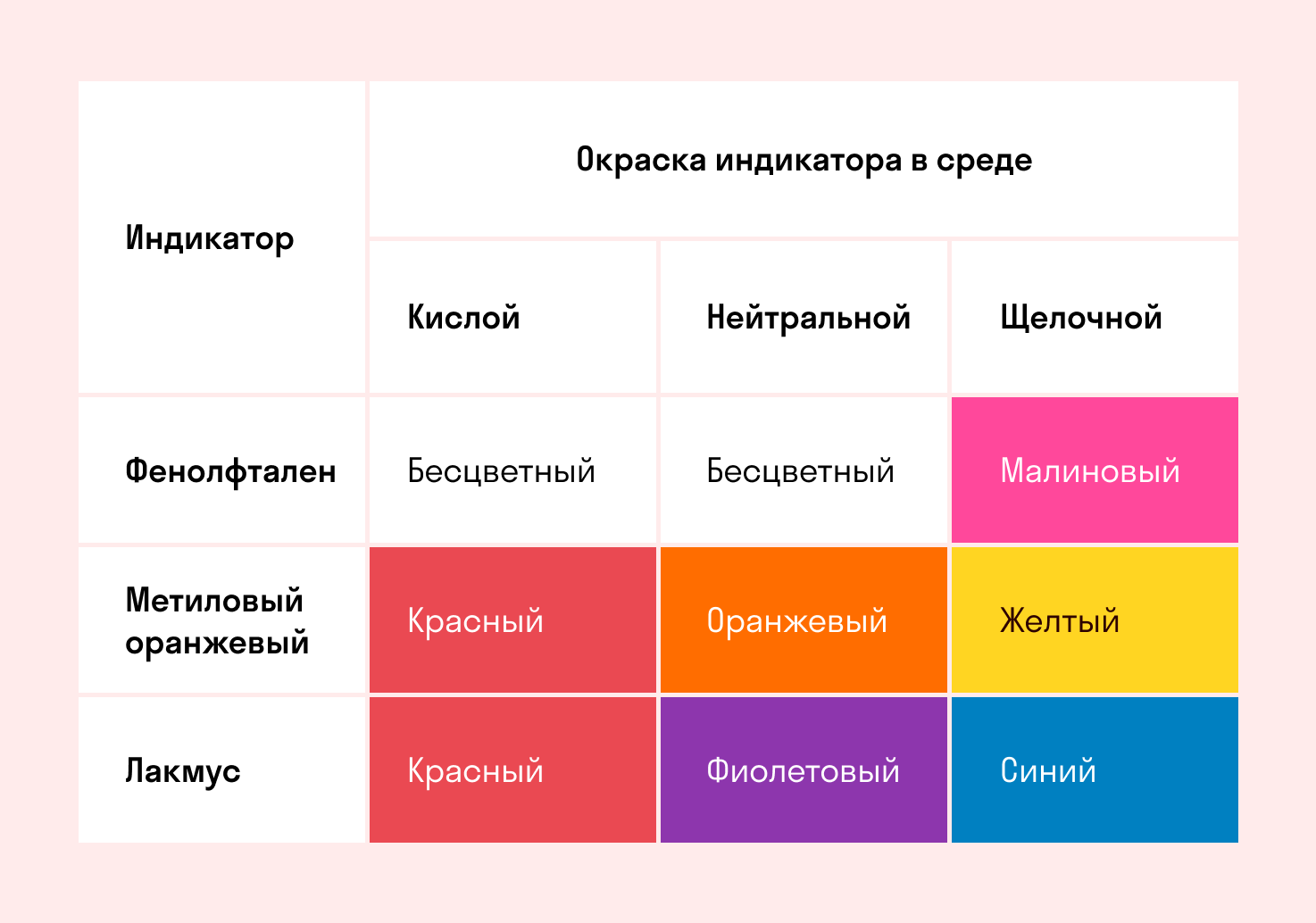
Способность окрашивать индикаторы
Индикаторы кислот — это специальные вещества, при помощи которых определяют наличие кислот в растворе.
Вопросы для самоконтроля
С чем реагируют кислоты?
При каких условиях кислоты взаимодействуют с солями? Приведите пример.
Составьте уравнения реакций и назовите продукты реакций:
Разбавленный раствор серной кислоты реагирует с: медью, хлоридом меди, сульфатом меди, цинком?
Соляная кислота вступает в реакцию с каждым из двух веществ:
Взаимодействие металлов с кислотами
ХИМИЯ МЕТАЛЛОВ
Целью данной работы является рассмотрение связи физико-химических свойств металлов с ЭЛЕКТРОННЫМ строением атомов, строением кристаллической структуры, изучение химических свойств металлов (взаимодействие с простыми и сложными окислителями; водой, кислотами, щелочами, их смесями) для понимания физико-химических процессов при химических методах обработки металлов и сплавов.
Основные понятия темы
Металлы — простые вещества, обладающие характерными свойствами; высокой электропроводностью и теплопроводностью, отрицательным температурным коэффициентом электропроводности, способностью хорошо отражать электромагнитные волны (блеск и непрозрачность), пластичностью.
По химическим свойствам металлы — восстановители, так как легко отдаю: свои валентные электроны:
Металлы — это элементы, атомы которых имеют минимальное количество электронов на внешнем энергетическом уровне. Степень окисления определяется числом неспаренных электронов в нормальном и возбужденном состояниях.
Восстановительную активность атома элемента определяют потенциалом ионизации валентных электронов. Химическая активность металла как простого вещества, имеющего кристаллическое строение, характеризуется термодинамическими величинами (знтальпией ΔН и энергией Гиббса ΔG). Для суждения о возможности реакции металла с водой, кислотами, щелочами необходимо также определение величины ΔG химической реакции, Так как эти реакции являются окислительно-восстановительными, где металл выступает в качестве восстановителя, а ион водорода H + (гидроксоний H2O) либо анион кислоты в виде окислителя.
При условии, что φокисл > φвост, реакция между металлом и водой, кислотой, щелочью, растворами солей возможна
Взаимодействие металлов с простыми окислителями
Простые окислители — это кислород О:, галогены. Наиболее часто встречается реакция окисления металлов кислородом воздуха:
Возможность данной реакции при нормальных условиях определяется
величиной ΔG 0 298 реакции.
При окисления металлов кислородом образуются оксиды. Для металлов, имеющих большое число степеней окисления, низшие оксиды металлов обладают основными свойствами (если степень окисления от 1 до 2), высшие оксиды (оксиды с максимальными степенями окисления) -кислотными (степень окисления > 4), Оксиды, где степень окисления +3, +4 — амфотерны.
7.1.2. Взаимодействие металлов с водой
Металлы взаимодействуют с водой по реакции
Так как эта реакция является окислительно-восстановительной, то возможность данной реакции определяется по величине энергии Гиббса.
Наряду с термодинамическим расчетом необходимо учитывать, что многие металлы покрыты оксидными пленками.
Взаимодействие металлов с кислотами
Для очистки металлов от поверхностных слоев перед нанесением покрытий всегда, когда нужно иметь дело с чистой поверхностью металла, используют кислотное травление. Травление бывает технологическое и структурное
Технологическое травление используют для обработки и изменения формы поверхности металла, структурное травление — для выявления структуры поверхности кристаллических материалов,
Химическое фрезерование проводится для получения нужного рисунка — придания профиля поверхности детали, Согласно чертежу, на отдельные участки поверхности заносится химически стойкий слой, а свободные участка травятся при воздействии смесей кислот.
Химическое травление используется для выявления дефектов в кристаллах: малоугловых и двойниковых границ, дислокаций и дефектов упаковки
Для металлов, химическое травление которых затруднено (Ti, Mo, W, жаропрочные сплавы), используется электрохимическое травление.
Кислоты — вещества, содержащие водород и диссоциирующие с образованием Н + .
Различают бескислородные и кислородсодержащие кислоты.
Бескислородные кислоты — растворы галогеноводородов в воде: соляная (НС1), плавиковая (HF), бромоводородная (НВг), йодоводородная (HI), сероводородная (H-S),
Кислородсодержащие кислоты: азотная, серная, фосфорная, хлорная и другие.
План выполнения эксперимента
Запишите предполагаемое уравнение реакции взаимодействия исследуемого металла с раствором электролита. По уравнениям (7.6-7.9; 7.22-7.24), значениям электродных потенциалов и перенапряжений определите термодинамическую вероятность протекания этих реакций. Для взаимодействия типа Me + <Г получите также эту информацию, пользуясь диаграммой Пурбе.
Опустите в пробирки стружки металла и прилейте 1 -2 мл электролита С концентрированными растворами работайте в вытяжном шкафу. Опишите характер протекания реакции, окраску, запах выделяющихся продуктов. Если реакция не идет при комнатной температуре, нагревайте раствор на спиртовке
В отчете приведите уравнения химических реакций, расчет термодинамической вероятности протекания реакции, экспериментальные наблюдения и сопоставьте данные расчета и эксперимента.
Реакция взаимодействия с водой
Положили в пробирку кусочек цинка, налили воды и подогрели на спиртовке. Довели воду до кипения. Наглядных проявлений хода реакции не наблюдалось.
Zn 0 – 2e → Zn 2+ φвост(Zn 2+ /Zn) = -0.763 В φокисл (2H2O/2OH 2- H2) = -0.414 В
E = φокисл – φвост = -0,414 + 0,763 = 0,349 В
ΔG = -zFE = -2*26.8*0.349 = -18.706
т. к. ΔG 0 — 2e → Zn 2+ (восстановитель)
NO3 — + H + + 3e → NO + H2O (окислитель)
уравняем левую и правую части

2 NO3 — + 4H + + 3e → NO + 2H2O (окислитель)
3Zn 0 + 8H + → 3Zn 2+ + 2NO +4H2O
φвост(Zn 2+ /Zn) = -0.763 В φокисл (NO3 — /NO) = 0.96 В
E = φокисл – φвост = 0,96 + 0,763 = 1,723 В
ΔG = -zFE = -2*26,8*1,723 = -92,35 , т. к. ΔG 0 — 2e → Zn 2+ (восстановитель)
HSO4 — +7H + + 6e → S + 4H2O (окислитель)
φвост(Zn 2+ /Zn) = -0.763 В φокисл = +0.351 В
E = φокисл – φвост = 0.351 +0.763 = 1.114 В
ΔG = -zFE = -2*26,8*1,114 = -59,7 , т. к. ΔG 0 — 2e → Zn 2+ (восстановитель)
2H + + 2e → H2 (окислитель)
φвост(Zn 2+ /Zn) = -0.763 В φокисл = 0, т. к. Ph соляной кислоты = 0
E = φокисл – φвост = 0 + 0,763 = 0,763 В
ΔG = -zFE = -2*26,8*0,763 = -40,9 , т. к. ΔG 0 — 2e → Zn 2+ (восстановитель)
2H2O + 2e → 2OH — + H2 (окислитель)
φвост(Zn 2+ /Zn) = -0.763 В φокисл = -0.82 В
E = φокисл – φвост = -0,82 + 0,763 = -0,057 В
ΔG = zFE = -2*26,8*0,057 = -3,05 , т. к. ΔG
http://skysmart.ru/articles/chemistry/himicheskie-svojstva-kislot
http://poisk-ru.ru/s9054t3.html