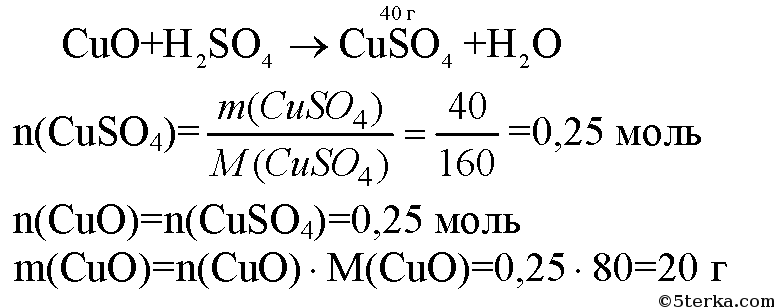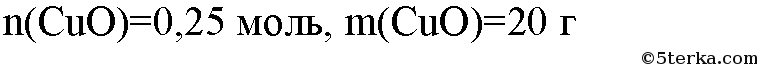Используя метод электронного баланса, составьте уравнение реакции Mg + H2SO4 → MgSO4 + H2S + H2O Определите окислитель и восстановитель
Ваш ответ
решение вопроса
Похожие вопросы
- Все категории
- экономические 43,300
- гуманитарные 33,630
- юридические 17,900
- школьный раздел 607,282
- разное 16,837
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Тема III. Работа 2. Свойства кислот. Соли. Вариант 4
Вопросы:
1. Допишите уравнения реакций получения солей: а) Mg + H2SO4 = б) Fe2O3 + HCl = в) BaO + HNO3 =
Расставьте коэффициенты и назовите образующиеся соли.
2. Перечислите общие химические свойства кислот.
3. При взаимодействии оксида меди(II) с серной кислотой образовалось 40 г сульфата меди(II). Рассчитайте массу и количество вещества оксида меди(II), вступившего в реакцию.
Решения и ответы:
2. Кислоты реагируют с металлами, основными оксидами, основаниями, солями.

задача №4
к главе «Тема III. Водород. Кислоты. Соли. Работа 2. Свойства кислот. Соли».
Тесты по теме ХИМИЧЕСКИЕ РЕАКЦИИ (4 варианта)
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
Дисциплина «Химия» Критерии оценки:
Тема: «Химические реакции» «5» — 13 баллов
Тест 1-2 уровня «4» — 11 баллов
Какие из следующих реакций являются окислительно-восстановительными:
А) КОН + CuCl 2 → КС l + Cu ( OH ) 2
Б) К Br + Cl 2 → KCl + Br 2
Перепишите приведенные схемы химических реакций, расставьте коэффициенты и укажите, к какому типу можно отнести каждую из них:
Б ) MgCl 2 + NaOH → Mg(OH) 2 ↓ + NaCl
Укажите тип каждой из следующих ОВР:
А) K С l О 3 → K С l + K С l О 4
Укажите уравнение реакции замещения:
А) BaO + H 2 O = Ba(OH) 2
Б) CuO + H 2 = Cu + H 2 O
В) 3 KOH + H 3 PO 4 = K 3 PO 4 + 3 H 2 O
По данной левой части уравнения CuO + H 2 SO 4 = … восстановите его правую часть.
А) CuSO 4 + H 2 O
Б) CuSO 4 + 2 H 2 O
В) CuSO 4 + H 2
Восстановите пропущенную запись и укажите тип химической реакции:
А) ? + 2 HCl = FeCl 2 + H 2
Б) 2 Al + ? = 2 AlCl 3
Из нескольких простых или сложных веществ образуется одно более сложное вещество в реакции:
А) замещение
Б) обмена
В) разложение
Г) соединение
Расставьте коэффициенты в схемах и укажите типы химических реакций:
А) Al 2 O 3 + H 2 SO 4 
Б) H 2 + Cl 2 
Составьте уравнение ОВР, которая протекает по следующей схеме:
KMnO 4 + К Br + H 2 SO 4 
Химическое явление – это:
А) плавление олова
Б) горение магния
В) замерзание воды
Дисциплина «Химия» Критерии оценки:
Тема: «Химические реакции» «5» — 13 баллов
Тест 1-2 уровня «4» — 11 баллов
Уравнение реакции обмена:
А) CaO + SiO 2 = CaSiO 3
Б) FeS + 2 HCl = FeCl 2 + H 2 S 
В) 2 KClO 3 = 2 KCl + 3O 2
Расставьте коэффициенты в схемах и укажите типы химических реакций:
А) Li + O 2 
Б) Fe 2 O 3 + Al 
Уравнение реакции разложения:
А) CaO + SiO 2 = CaSiO 3
Б) FeS + 2 HCl = FeCl 2 + H 2 S
В) 2 KNO 3 = 2 KNO 2 + O 2
Из одного сложного вещества образуется два или более новых веществ в реакции:
А) замещение
Б) обмена
В) разложение
Г) соединение
По данной правой части уравнения … = CuCl 2 + 2 H 2 O восстановите его левую часть.
А) Cu + 2 HCl
Б) Cu(OH) 2 + 2 HCl
В) CuO + 2 HCl
Восстановите пропущенную запись, укажите тип химической реакции:
А) ? + H 2 SO 4 = ZnSO 4 + H 2
Б) 4 Al + ? = 2 Al 2 O 3
Расставьте коэффициенты в схемах и укажите типы химических реакций:
А) CuO + HCl 
Б) NH 3 
Физическое явление – это:
А) испарение воды
Б) горение керосина
В) скисание молока.
Составьте уравнение ОВР, которая протекает по следующей схеме:
Приведите примеры реакций соединения, в результате которых образуются следующие вещества: а) FeS б) Fe 2 O 3 в) FeCl 3
Дисциплина «Химия» Критерии оценки:
Тема: «Химические реакции» «5» — 13 баллов
Тест 1-2 уровня «4» — 11 баллов
Расставьте коэффициенты в схемах и укажите типы химических реакций:
а) Fe 2 O 3 + HCl 
б) NO + O 2 
Химическое явление – это:
а) плавление олова
б) горение магния
в) замерзание воды
Уравнение реакции замещения:
а) BaO + H 2 O = Ba(OH) 2
б) CuO + H 2 = Cu + H 2 O
в) 3 KOH + H 3 PO 4 = K 3 PO 4 + 3 H 2 O
Сумма коэффициентов в уравнении реакции:
А) 10; Б) 11; В) 12; Г) 13;
По данной левой части уравнения ZnO + 2 HCl =… восстановите его правую часть.
а) ZnCl 2 + H 2 O
б) ZnCl 2 + 2 H 2 O
в) ZnCl 2 + H 2
Восстановите пропущенную запись, укажите тип химической реакции:
а) Mg + 2 HCl = ? + H 2
б) 2 Na + ? = 2 NaCl
Расставьте коэффициенты в схемах и укажите типы химических реакций:
а) Al 2 O 3 + H 2 SO 4 
б) H 2 + Cl 2 
Физическое явление – это:
А) испарение воды
Б) горение керосина
В) скисание молока
Методом электронного баланса c оставьте уравнение ОВР, которая протекает по следующей схеме:
Приведите примеры реакций соединения, в результате которых образуются следующие вещества: а) CO 2 б) SO 2 в) P 2 O 5
Дисциплина «Химия» Критерии оценки:
Тема: «Химические реакции» «5» — 13 баллов
Тест 1-2 уровня «4» — 11 баллов
Какое уравнение соответствует реакции разложения:
А ) Zn + CuSO 4 = ZnSO 4 + Cu
Сумма коэффициентов в уравнении реакции FeCl 3 + Ca(OH) 2 = Fe(OH) 3 + CaCl 2 равна:
А) 10 Б) 11 В) 12 13
Расставьте коэффициенты в схемах и укажите типы химических реакций:
Какое из приведенных уравнений соответствует реакции нейтрализации?
В ) CaCl 2 + Na 2 CO 3 = CaCO3 + 2 NaCl
Допишите уравнения реакций. Назовите тип химической реакции.
В уравнении ОВР Cu + HNO 3 (разб.) = Cu ( NO 3 ) 2 + NO + H 2 O коэффициент перед окислителем равен
А) 8 Б) 10 В) 6 Г) 4
ОВР реакцией является реакция, уравнение которой
В) CuCl 2 + Fe = FeCl 2 + Cu
Реакции, в результате которых выделяется определенное количество теплоты, называются
Методом электронного баланса c оставьте уравнение ОВР, которая протекает по следующей схеме:
Приведите примеры реакций соединения, в результате которых образуются следующие вещества: а) Сг S б) CuCl 2 в) CuO
Курс повышения квалификации
Дистанционное обучение как современный формат преподавания
- Сейчас обучается 930 человек из 80 регионов
Курс повышения квалификации
Инструменты онлайн-обучения на примере программ Zoom, Skype, Microsoft Teams, Bandicam
- Курс добавлен 31.01.2022
- Сейчас обучается 26 человек из 18 регионов
Курс повышения квалификации
Педагогическая деятельность в контексте профессионального стандарта педагога и ФГОС
- Сейчас обучается 36 человек из 23 регионов
Ищем педагогов в команду «Инфоурок»
Дистанционные курсы для педагогов
«Взбодрись! Нейрогимнастика для успешной учёбы и комфортной жизни»
Свидетельство и скидка на обучение каждому участнику
Найдите материал к любому уроку, указав свой предмет (категорию), класс, учебник и тему:
5 594 350 материалов в базе
Самые массовые международные дистанционные
Школьные Инфоконкурсы 2022
33 конкурса для учеников 1–11 классов и дошкольников от проекта «Инфоурок»
«Психологические методы развития навыков эффективного общения и чтения на английском языке у младших школьников»
Свидетельство и скидка на обучение каждому участнику
Другие материалы
- 24.09.2015
- 6114
- 10
- 24.09.2015
- 746
- 2
- 24.09.2015
- 2844
- 8
- 24.09.2015
- 748
- 0
- 24.09.2015
- 2210
- 0
- 24.09.2015
- 2920
- 2
- 24.09.2015
- 428
- 0
Вам будут интересны эти курсы:
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
Добавить в избранное
- 24.09.2015 26718
- DOCX 34.8 кбайт
- 32 скачивания
- Рейтинг: 3 из 5
- Оцените материал:
Настоящий материал опубликован пользователем Кондакова Лилия Николаевна. Инфоурок является информационным посредником и предоставляет пользователям возможность размещать на сайте методические материалы. Всю ответственность за опубликованные материалы, содержащиеся в них сведения, а также за соблюдение авторских прав несут пользователи, загрузившие материал на сайт
Если Вы считаете, что материал нарушает авторские права либо по каким-то другим причинам должен быть удален с сайта, Вы можете оставить жалобу на материал.
Автор материала
- На сайте: 6 лет и 7 месяцев
- Подписчики: 5
- Всего просмотров: 192305
- Всего материалов: 6
Московский институт профессиональной
переподготовки и повышения
квалификации педагогов
Дистанционные курсы
для педагогов
663 курса от 690 рублей
Выбрать курс со скидкой
Выдаём документы
установленного образца!
Учителя о ЕГЭ: секреты успешной подготовки
Время чтения: 11 минут
Минпросвещения России подготовит учителей для обучения детей из Донбасса
Время чтения: 1 минута
Школьник из Сочи выиграл международный турнир по шахматам в Сербии
Время чтения: 1 минута
РДШ организовало сбор гуманитарной помощи для детей из ДНР
Время чтения: 1 минута
Ленобласть распределит в школы прибывающих из Донбасса детей
Время чтения: 1 минута
В Белгородской области отменяют занятия в школах и детсадах на границе с Украиной
Время чтения: 0 минут
Минобрнауки и Минпросвещения запустили горячие линии по оказанию психологической помощи
Время чтения: 1 минута
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.
http://5terka.com/node/11284
http://infourok.ru/testi-po-teme-himicheskie-reakcii-varianta-434604.html