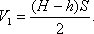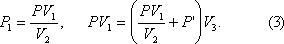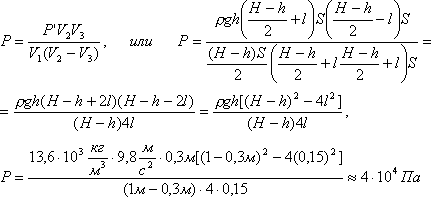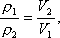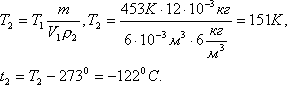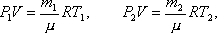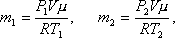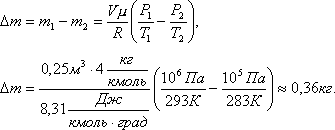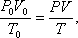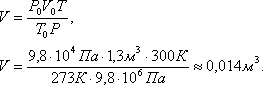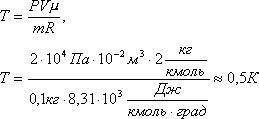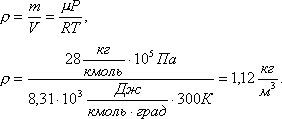Алгоритм решения задач на уравнение Менделеева — Клайперона
Разделы: Физика
Алгоритм решения задач на применение уравнения Менделеева Клайперона.
Многократное (до 7 и более раз) воспроизведение учащимися логически выверенных строго последовательных пошаговых действий дает возможность глубоко и прочно усвоить учебный материал. Представленный алгоритм апробирован. Он позволяет:
1) научить использовать уравнение МенделееваКлайперона (его варианты);
2) продолжить формирование навыков работы в международной системе единиц “СИ” и культуры оформления решения задач;
3) осуществляет межпредметную связь с алгеброй и химией;
4) воспитывает точность, аккуратность, пунктуальность.
| № шага | Алгоритм | Выполнение |
| 1 | Внимательно прочитайте текст задачи. | Баллон содержит 50 л кислорода, температура которого 27° С, а давление 2МПа. Найдите массу кислорода. |
| 2 | Запишите в “Дано” буквенное обозначение и числовое значение известных по тексту физических величин. Необходимо знать нормальные условия: р=10 5 Па, t°=0° С | Дано: p=2 МПа |
| 3 | Запишите химическую формулу и молярную массу газообразного вещества в “ Дано”, используя систему СИ. М Воздух= 0,029 кг/моль. | О2 М=32•10 3 кг/моль |
| 4 | Под горизонтальной чертой запишите буквенное обозначение неизвестной величины, знак = и? | m= ? |
| 5 | Под словом “ Решение” напишите уравнение МенделееваКлайперона или его вариант: | |
| 6 | Проделайте алгебраические преобразования так, чтобы по одну сторону знака = стояла неизвестная величина, а по другую все известные. | |
| 7 | Проверьте, все ли величины выражены в системе СИ, учитывая, что 1л= 10 3 м 3 , Т=t° +273 , 1 мм рт. ст.= 133 Па | 50 л = 5• 10 2 м 3 Т = 300 К |
| 8 | Подставьте числовые значения вместе с единицами измерения, проведите расчет и работу с единицами измерения, учитывая, что 1 Дж=1 Н? м, 1 Па=1Н/м 2 , 1 Н=1кг? м/с 2 |  |
| 9 | Запишите ответ: | Ответ: m=1,3 кг |
Задачи для закрепления:
1) Определите массу водорода, находящегося в баллоне емкостью 20 л при давлении 830 кПа, если температура газа равна 17° С.
2) Сосуд вместимостью 40 л содержит 1,98 кг углекислого газа и выдерживает давление не выше 3 МПа. При какой температуре возникает опасность взрыва?
3) Определите плотность азота при нормальных условиях.
4) Какое количество вещества содержится в газе при давлении 200 кПа и температуре 240 К, если его объем 40 л?
5) Какой объем занимает воздух массой 2,9 кг при давлении 750 мм рт.ст. и температуре 3° С?
6) Каково давление азота в сосуде объемом 0,25 м 3 при температуре 32° С? Масса газа 300 г.
Таблицу алгоритма и примеры решения задач на закрепление учитель, исходя из методических потребностей, может размещать как на одной, так и на разных сторонах листа формата А4, раздать ученикам для использования на уроке и дома.
1) 0,014 г;
2) 48° С;
3) 1,23 кг/м 3 ;
4) 4 моль;
5) 2,25 м 3 ;
6) 108624 Па.
Урок решения задач по теме «Уравнение Менделеева — Клапейрона»
Данный урок по физике для учащихся 10 класса по теме «Уравнение Менделеева — Клапейрона»
Просмотр содержимого документа
«Урок решения задач по теме «Уравнение Менделеева — Клапейрона»»
Тема урока: Решение задач на уравнение Менделеева-Клапейрона
Цели урока: продолжить формирование умения решать качественные, вычислительные и графические задачи на применение уравнения Менделеева-Клапейрона и газовых законов;
развить познавательный интерес к физике;
воспитывать активность и целеустремленность при решении задач.
Тип урока: закрепление материала
Форма урока: Урок – тренинг.
Актуализация знаний учащихся
1. Сформулируйте и экспериментально обоснуйте:
А) закон Бойля – Мариотта;
Б) закон Гей – Люссака
2. Постройте изотерму в осях координат: (P,V), (P, T), (V,T).
3, Постройте изобару в осях координат: (V,T); (P, T); (P, V)
4 Постройте изохору в осях координат: (P, T); (V, T); (V, P).
3. Решите качественные задачи.
А) Почему пузырьки воздуха, поднимаясь в воде вверх, увеличиваются в объеме?
Б) Плавательный пузырь выходит через рот наружу, если глубоководную рыбу вынуть из воды. Почему это происходит?
Г) Почему с горящих поленьев с треском слетают искры?
Д) Почему из стеклянной бутылки вылетает пробка, если в нее налить газированную воду, а потом поставить в теплое место?
4. Вычислительные задачи.
Задача 1. При сжатии газа его объем уменьшился на 2 л, а давление увеличилось в 2 раза. Найти первоначальный объем газа V1.
Обозначим ΔV изменение объема газа, P1 и P2 – давления газа до и после сжатия.
Решение. Судя по условию задачи, здесь процесс изотермический. Правда следовало бы добавить, что процесс сжатия происходит медленно, потому что, если бы он происходил быстро, то это был уже адиабатный процесс, при котором температура газа тоже меняется. Но, как правило, при условии задач на газовые процессы об этом упомянуть забывают, поэтому мы и обратили на этот момент внимание.
Произведем вычисления V1= 2·2л=4л
Задача 2. В узкой откачанной и запаянной с двух концов горизонтальной трубке посредине находится столбик ртути длиной 0,3 м. Если трубку поставить вертикально, столбик ртути сместится на 15 см. Определить давление в трубке до того как из нее откачали воздух, если ее длина 1м, а плотность ртути13,6·10 3 кг/м 3 .
Решение. По условию задачи температура газа остается постоянной, поэтому при решении задачи можно применить закон Бойля-Мариотта. Состояние воздуха в трубке в горизонтальном положении определялось параметрами: объемом V1 и давлением P. Выразим объем через поперечное сечение трубки S и высоту воздушного столбика 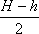
При вертикальном положении трубки состояние газа в верхней части трубки определялось параметрами: объемом 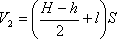
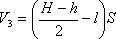
Запишем закон Бойля-Мариотта для состояния газа в верхней части трубки
и для нижней части трубки
Выражение P1, полученное из (1), подставим в (2)
В равенство (3) подставим значения
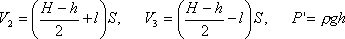
Задача 3. Газ массой 12·10 -3 кг занимает объем 6·10 -3 м 3 при температуре 180 0 С. При какой температуре плотность этого газа будет равна 6 кг/м 3 .
Решение: Плотность газа при постоянном давлении и массе обратно пропорциональна объему, то есть
но при постоянном давлении объем прямо пропорционален абсолютной температуре 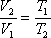

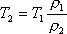
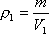
Задача 4. Определить на сколько изменилась масса гелия, находящегося в баллоне объемом 0,25 м 3 под давлением 10 6 Па при температуре 20 0 С, если из баллона была выпущена часть массы газа, после чего давление понизилось до 10 5 Па, а температура уменьшилась до 10 0 С.
Решение. До того как часть газа была выпущена из баллона его состояние определялось такими параметрами: давление Р1, объем V, масса m1, температура Т1. После того как часть газа была выпущена из баллона, состояние газа стало определяться параметрами: Р2, V, m2, T2.Запишем уравнение Менделеева-Клапейрона для первого и второго состояния газа
где V – объем газа, который по условию задачи остается неизменным; μ – молекулярный вес гелия. Выразим из этих уравнений m1 и m2 и найдем их разность Δm
Задача 5. Определить объем баллона со сжатым углекислым газом, находящимся под давлением в 100 атмосфер при температуре 27 0 С, если при нормальных условиях то же количество углекислого газа занимает объем 1,3 м 3 .
Решение. При нормальных условиях состояние газа определяется параметрами: Т0, P0, V0. При данных условиях – параметрами Т, P, V. Так как масса газа не изменялась, то для решения задачи можно воспользоваться уравнением объединенного газового закона:
Задача 6. При какой температуре находилось 100 г водорода в баллоне объемом 10 л, если давление при этом было 2 . 10 4 Па?
Решение. Из уравнения Менделеева-Клапейрона PV= m /µ·RT находим температуру:
Задача 7. Со дна водоема всплывает пузырек воздуха. На глубине 6 м он имел объем 10 мм³. Найти чему будет равен объем пузырька около поверхности воды.
Решение. P₁ V₁ = P₂ V₂; P₁ = ρ·g·h + P₀; P₂ = P₀; где Р₀ – атмосферное давление.
(ρ g h + P₀)V₁ = P₀V₂; V₂ = (ρ g h + P₀) V₁/ P₀; V₂ = 16 (мм³)
Задача 1. Определить плотность азота при температуре 27 0 С и давлении 760 мм рт. ст.
Решение. Из уравнения Менделеева-Клапейрона найдем плотность азота PV= m /µ·RT откуда
Ответ: 1,12 кг/м 3 .
Задача 2.. Найдите первоначальный объем, если давление газа увеличилось в 1,5 раза, а объем его уменьшился при этом на 30 мм.
Решение. P₁V₁ = P₂V₂; ΔV = V₁ – V₂; V₂ = V₁ – ΔV; P ₁V₁ = P₂(V₁ – ΔV); V₁ (P₂ – P₁) = P₂·ΔV;
Урок по физике «Решение задач на применение Уравнение Менделеева-Клапейрона».
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
Раздел дисциплины: Молекулярная физика.
Тема урока: «Решение задач на применение Уравнение Менделеева-Клапейрона».
Тип урока: урок структуризации полученных знаний ( общеметодологической направленности).
Вид урока: комбинированный (дискуссия с постановкой проблемных ситуаций, практическая работа, самостоятельная работа).
1. Образовательная – продолжить формирование умения решать количественные задачи на применение уравнения Менделеева-Клапейрона; расширить знания в области молекулярной физики.
2. Развивающая – способствовать формированию умений анализировать, обобщать факты, применять полученные знания при решении задач.
3. Воспитательная – формирование сознательного отношения к процессу обучения, стремления к самостоятельной деятельности; продолжить формирование основ научного мировоззрения обучающихся.
Метод проведения урока: проблемно-поисковый.
Время реализации урока: 45 мин
Химия ( количество вещества или число моль, молярная масса).
Атомная физика (строение атома, масса и заряд элементарных частиц).
Microsoft Windows XP (Microsoft Word, Microsoft Office Power Р oint).
Карточки (15 штук) Приложение.
Дополнение к практической работе.
Мякишев Г.Я., Буховцев Б.Б. Учебник.Физика 10 класс. – М.: Просвещение,2013
Рымкевич А.П.Физика.Задачник.10-11 класс. – М.:Дрофа,2014
1) Организационный момент. Формулирование темы.
Преподаватель проверяет присутствие обучающихся и их готовность к уроку.
Создание деловой и доброжелательной обстановки.
Формулирование темы и цели урока.
Преподаватель рассказывает об общем ходе занятия.
2) Актуализация имеющихся знаний, умений и навыков.
Какой газ называют идеальным?
Назовите микроскопические параметры идеального газа.
Как объяснить давление газа с точки зрения МКТ?
Каким прибором измеряется давление газа?
Запишите основное уравнение МКТ идеального газа.
От чего зависит средняя кинетическая энергия молекул идеального газа?
От каких величин зависит средняя квадратичная скорость молекул идеального газа?
Что такое температура и что она характеризует? С какими микроскопическими параметрами связана температура?
Запишите формулу, устанавливающую взаимосвязь температуры по шкале Кельвина и Цельсия.
Запишите формулу, показывающую зависимость средней кинетической энергии поступательного движения молекул от температуры.
Для того чтобы описать состояние идеального газа используют три термодинамических параметра. Какие?
Запишите уравнение состояния идеального газа.
Решение задачи у доски с помощью преподавателя
Баллон с предохранительным клапаном (газгольдер) содержит водород при 



Пояснение решения задачи:
C начала состояние газа описывалось уравнением:
Масса газа в баллоне была, соответственно:
После установления нового равновесия масса газа в баллоне станет:
По условию задачи 

Откуда объем сосуда равен:
Подставим числа, переведем температуры в шкалу Кельвина:


Ответ: V = 1011 м 
3) Закрепление навыков
Практическая работа — самостоятельная работа обучающихся
Методические рекомендации к самостоятельной работе:
Самостоятельная работа представлена в трех вариантах и имеет дифференцированный характер.
Вариант №3 следует предлагать самым сильным обучающимся.
Задание № 3 для 1 варианта и задания №2 для 2 и 3 вариантов подается на экране.
Самостоятельная работа
1) Температуру идеального газа увеличили в 4 раза. При этом средняя квадратичная скорость его молекул:
А) увеличилась в 4 раза
В) увеличилась в 2 раза
С) уменьшилась в 4 раза
2) В таблице приведены значения некоторых параметров состояния газа. Определить недостающий параметр.
3) Определить массу воздуха в помещении №1 (Задание на экране)
1) Сравнить давления водорода и кислорода при одинаковых концентрациях молекул и равных средних квадратичных скоростях их движения. М 1 = 2 г/моль, М 2 = 32 г/моль. Р 2 / Р 1 = А) 1/16 В) 16 С) 64
2) Определить массу воздуха в помещении №2 (Задание на экране)
3) Найти формулу некоторого соединения углерода с водородом, если известно, что это вещество массой m = 0,66 г в газообразном состоянии при температуре t = 27 0 C в объеме 1 дм 3 создает давление Р = 10 5 Па?
1) В результате нагревания давление газа в закрытом сосуде увеличилось в 4 раза. Во сколько раз изменилась средняя квадратичная скорость молекул газа? / 1 = А) 2 В) 4 С) 8
2) Определить массу воздуха в помещении №3 (Задание на экране)
3) До какой температуры Т 1 при постоянном давлении Р = 10 5 Па надо нагреть кислород, чтобы его плотность стала равна плотности водорода при том же давлении и температуре Т 2 = 200 К ?
Содержание заданий № 3 для 1 варианта и задания №2 для 2 и 3 вариантов
Дан план квартиры. Определить массу воздуха в помещениях №1 – 1 вариант, №2 – 2 вариант, №3 – 3 вариант при нормальном атмосферном давлении ( P = 100 кПа; M = 29·10 -3 кг/моль – молярная масса воздуха).
Принимаются следующие условия:
— Температура в помещениях 22 0 С
— Высота потолка в квартире 2 м 70 см
Методические рекомендации по организации самостоятельной работы.
Карточка самостоятельной работы дана в приложении.
Задание № 3 для 1 варианта и задания №2 для 2 и 3 вариантов подается на экране с помощью Microsoft Office Power Р oint (дополнение к практической работе).
Пояснение решения задачи №3 для 2 варианта:
Согласно уравнению Менделеева-Клапейрона
Молярная масса вещества равна:
В формулу подставлена абсолютная температура Т = t +273, Т = 300 К ; объем выражен в м 3 .
М = 16 • 10 -3 кг/моль, или 16 г/моль, или молекулярная масса равна 16 а.е.м. – то есть в состав соединения войдет атом углерода с молекулярной массой 12 а.е.м. и 4 атома водорода с молекулярной массой 1 а.е.м. – формула соединения СН 4 .
Пояснение решения задачи №3 для 3 варианта:
Согласно уравнению Менделеева-Клапейрона
Плотность – это масса некоторого объема: 

Молярная масса вещества равна:
Тогда плотность газа:
Ответ: Т 1 = 3200 К
Критерии выставления оценки за работу обучающихся:
4) Подведение итогов урока. Рефлексия.
Преподаватель совместно с обучающимися подводит итоги урока.
Обучающиеся отвечают на вопросы:
Что нового узнали сегодня на занятии?
Что на уроке показалось трудным?
Преподаватель выставляет оценки обучающимся за работу на занятии.
§ 70; вопросы стр 191 [1] ;
задачи 479, 480 [2]
Спасибо за работу!
Самостоятельная работа
1) Температуру идеального газа увеличили в 4 раза. При этом средняя квадратичная скорость его молекул:
А) увеличилась в 4 раза
В) увеличилась в 2 раза
С) уменьшилась в 4 раза
2) В таблице приведены значения некоторых параметров состояния газа. Определить недостающий параметр.
3) Определить массу воздуха в помещении №1 (Задание на экране)
1) Сравнить давления водорода и кислорода при одинаковых концентрациях молекул и равных средних квадратичных скоростях их движения. М 1 = 2 г/моль, М 2 = 32 г/моль. Р 2 / Р 1 = А) 1/16 В) 16 С) 64
2) Определить массу воздуха в помещении №2 (Задание на экране)
3) Найти формулу некоторого соединения углерода с водородом, если известно, что это вещество массой m = 0,66 г в газообразном состоянии при температуре t = 27 0 C в объеме 1 дм 3 создает давление Р = 10 5 Па?
1) В результате нагревания давление газа в закрытом сосуде увеличилось в 4 раза. Во сколько раз изменилась средняя квадратичная скорость молекул газа? / 1 = А) 2 В) 4 С) 8
2) Определить массу воздуха в помещении №3 (Задание на экране)
3) До какой температуры Т 1 при постоянном давлении Р = 10 5 Па надо нагреть кислород, чтобы его плотность стала равна плотности водорода при том же давлении и температуре Т 2 = 200 К ?
Дополнение к практической работе
Курс повышения квалификации
Дистанционное обучение как современный формат преподавания
- Сейчас обучается 932 человека из 80 регионов
Курс повышения квалификации
Педагогическая деятельность в контексте профессионального стандарта педагога и ФГОС
- Курс добавлен 23.11.2021
- Сейчас обучается 40 человек из 25 регионов
Курс повышения квалификации
Инструменты онлайн-обучения на примере программ Zoom, Skype, Microsoft Teams, Bandicam
- Курс добавлен 31.01.2022
- Сейчас обучается 26 человек из 16 регионов
Ищем педагогов в команду «Инфоурок»
Дистанционные курсы для педагогов
«Взбодрись! Нейрогимнастика для успешной учёбы и комфортной жизни»
Свидетельство и скидка на обучение каждому участнику
Найдите материал к любому уроку, указав свой предмет (категорию), класс, учебник и тему:
5 575 521 материал в базе
Материал подходит для УМК
«Физика. Базовый и углубленный уровни (в 2 частях) », Генденштейн Л.Э., Дик Ю.И.
4. Уравнение Клапейрона
Самые массовые международные дистанционные
Школьные Инфоконкурсы 2022
33 конкурса для учеников 1–11 классов и дошкольников от проекта «Инфоурок»
Другие материалы
- 30.06.2018
- 347
- 0
- 30.06.2018
- 846
- 0
- 30.06.2018
- 796
- 1
- 30.06.2018
- 701
- 7
- 30.06.2018
- 577
- 0
- 30.06.2018
- 308
- 0
- 29.06.2018
- 869
- 0
- 23.06.2018
- 774
- 0
Вам будут интересны эти курсы:
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
Добавить в избранное
- 06.07.2018 2900
- DOCX 407 кбайт
- 51 скачивание
- Оцените материал:
Настоящий материал опубликован пользователем Киселева Елена Николаевна. Инфоурок является информационным посредником и предоставляет пользователям возможность размещать на сайте методические материалы. Всю ответственность за опубликованные материалы, содержащиеся в них сведения, а также за соблюдение авторских прав несут пользователи, загрузившие материал на сайт
Если Вы считаете, что материал нарушает авторские права либо по каким-то другим причинам должен быть удален с сайта, Вы можете оставить жалобу на материал.
Автор материала
- На сайте: 3 года и 7 месяцев
- Подписчики: 1
- Всего просмотров: 7264
- Всего материалов: 5
Московский институт профессиональной
переподготовки и повышения
квалификации педагогов
Дистанционные курсы
для педагогов
663 курса от 690 рублей
Выбрать курс со скидкой
Выдаём документы
установленного образца!
Учителя о ЕГЭ: секреты успешной подготовки
Время чтения: 11 минут
Онлайн-конференция о создании школьных служб примирения
Время чтения: 3 минуты
В России действуют более 3,5 тысячи студенческих отрядов
Время чтения: 2 минуты
Приемная кампания в вузах начнется 20 июня
Время чтения: 1 минута
Минпросвещения подключит студотряды к обновлению школьной инфраструктуры
Время чтения: 1 минута
Полный перевод школ на дистанционное обучение не планируется
Время чтения: 1 минута
Тринадцатилетняя школьница из Индии разработала приложение против буллинга
Время чтения: 1 минута
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.
http://multiurok.ru/files/urok-rieshieniia-zadach-po-tiemie-uravnieniie-mien.html
http://infourok.ru/urok-po-fizike-reshenie-zadach-na-primenenie-uravnenie-mendeleevaklapeyrona-3153762.html