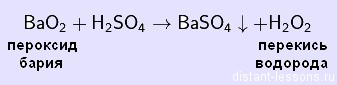Все химические уравнения с пероксидом водорода
Добро пожаловать, Гость!
Готовимся к сдаче ЕГЭ по химии
Пероксид водорода
Пероксид водорода (перекись водорода), H2O2
— простейший представитель пероксидов. Бесцветная жидкость с «металлическим» вкусом, неограниченно растворимая в воде, спирте и эфире. Концентрированные водные растворы взрывоопасны. Пероксид водорода является хорошим растворителем. Из воды выделяется в виде неустойчивого кристаллогидрата H2O2 • 2H2O.
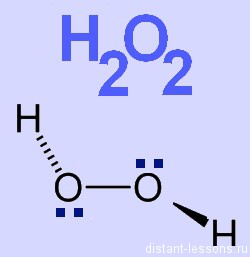
Строение молекулы
Молекула Н2O2 содержит в своем составе пероксидный анион O2 -2 . Каждый атом кислорода образует 2 ковалентные связи, но имеет степень окисления, равную -1. В упрощенном виде строение молекулы отражает графическая формула:
H +1 -O -1 -O -1 -H +1
Физические свойства
В чистом безводном виде Н2O2 — бесцв. сиропообразная жидкость с плотностью 1,45 г/см 3 (т. пл. -0,41°С, т. кип. 150,2°С). Смешивается с водой в любых соотношениях, растворяется также в спирте, эфире. 30%-ный р-р Н2O2 называют пергидролем. Подобно воде, Н2O2 — хороший полярный растворитель, в котором вещества с ионной и полярной ковалентной связью диссоциируют на ионы.
Химические свойства
Разложение Н2O2 (диспропорционирование)
2O -1 — 2e — → O2 0
При Т > 90° С пероксид водорода разлагается практически полностью. Причиной непрочности молекул Н2O2 является неустойчивость атома кислорода в степепени окисления -1.
Молекулы Н2O2 в незначительной степени диссоциируют в водном растворе по схеме:
(Кдисс = 1,5 * 10 -12 при 20°С)
Кислотные свойства проявляются в реакциях со щелочами с образованием солей — средних (пероксидов) и кислых (гидропероксидов), например:
Гидролиз пероксидов металлов
Хотя по составу пероксиды напоминают оксиды, они на самом деле обладают свойствами солей. В водных растворах полностью гидролизуются с выделением Н2O2:
Получение Н2O2 из пероксидов металлов
Так как Н2O2 — очень слабая кислота, то она вытесняется из своих солей как сильными кислотами, так и слабыми, например:
Атомы кислорода, находящиеся в неустойчивой степени окисления -1, стремятся приобрести еще один электрон для перехода в устойчивое состояние. Поэтому пероксид водорода проявляет очень сильные окислительные свойства, особенно в кислой среде:
Правила составления окислительно-восстановительных реакций
Окислительно-восстановительные свойства пероксида водорода
Потренироваться составлять реакции онлайн можно тут .
H2O2 — голубоватая жидкость со слабыми кислотными свойствами.
Пероксид водорода может принимать как окислительные, так и восстановительные свойства, но окислительные свойства сильнее. В окислительно-восстановительных реакциях необходимо сравнивать чьи окислительные свойства сильнее, чтобы правильно написать продукты реакции. В следующей таблице приведены примеры соединений с более сильными и более слабыми окислительными свойствами и примеры соответствующих реакций.
1. H2O2 — окислитель (восстанавливается с образованием H2O) в реакциях со следующими соединениями:
KI (йодиды), KNO2 (нитриты), PbS (сульфиды), Na2SO3 (сульфиты), NH3, соединения Cr +3 .
Примеры реакций:
2KI + H2O2 → I2 + 2KOH
KNO2 + H2O2 → KNO3 + H2O
Na2S + 4H2O2 → Na2SO4 + 4H2O
PbS + 4H2O2 → PbSO4 + 4H2O
Na2SO3 + H2O2 → Na2SO4 + H2O
2NH3 + 3H2O2  → N2 + 6H2O
Соединения Cr +3 в щелочной среде:
Cr2O3 + 3H2O2 + 4NaOH → 2Na2CrO4 + 5H2O
Cr2(SO4)3 + 3H2O2 + 10NaOH → 2Na2CrO4 + 3Na2SO4 + 8H2O
2Cr(OH)3 + 3H2O2 + 4NaOH → 2Na2CrO4 + 8H2O
2NaCrO2 + 3H2O2 + 2NaOH → 2Na2CrO4 + 4H2O
2K3[Cr(OH)6] + 3H2O2 → 2K2CrO4 + 2KOH + 8H2O
2. H2O2 — восстановитель (окисляется с образованием O2) в реакциях со следующими соединениями:
KMnO4, K2Cr2O7, Cl2 (галогены), соединения Au +3 , KNO3 (нитраты), KClO3 (хлораты).
Примеры реакций:
5H2O2 + KMnO4 + 3H2SO4 → 2MnSO4 + K2SO4 + 5O2 + 8H2O
3H2O2 + K2Cr2O7 + 4H2SO4 → Cr2(SO4)3 + 3O2 + K2SO4 + 7H2O
H2O2 + Br2 + 2KOH → 2NaBr + O2 + 2H2O
H2O2 + Cl2 → O2 + 2HCl
3H2O2 + KClO3 → KCl + 3O2 + 3H2O
3H2O2 + 2KNO3 + H2SO4 → K2SO4 + 2NO + 3O2 + 4H2O.
Химия, Биология, подготовка к ГИА и ЕГЭ
Это вещество продается во всех аптеках, т.е. его может приобрести любой человек. Химик Л. Ж. Тенар считается первооткрывателем «окисленной воды»
Давайте подробно разберем
свойства перекиси водорода
Строение молекулы
- валентность O = 2
- степень окисления O = -1
- молекула полярна
Физические свойства перекиси водорода
жидкое бесцветное вещество без запаха; с «металлическим» привкусом
очень хорошо растворимо в воде, точнее, перекись может смешиваться с H2O в любых соотношениях;
хорошо растворяется в полярных (органических) растворителях).
Химические свойства перекиси водорода
- Часто можно наблюдать, как капелька перекиси водорода «пузырит» — вещество очень легко разлагается на свету — образуется вода и выделяется кислород:
Поэтому перекись нельзя держать открытой на воздухе — со временем в склянке останется только вода.
пероксид водорода проявляет свойства очень слабой кислоты (слабее угольной):
с.о. -1 делает возможным и окислительные — восстановление до O(-2), и восстановительные — окисление до O2, свойства:
Окислительные свойства перекиси водорода
Восстановительные свойства перекиси водорода
В кислой среде H2O2 восстанавливается до H2O:
В щелочной или нейтральной — до OH-:
Если реакция идет с сильными окислителями, то образуется кислород:
Если реакция идет с сильными окислителями, то образуется кислород:
Биологические свойства перекиси водорода
— безвредное для организма противомикробное средство, дезинфицирующее средство
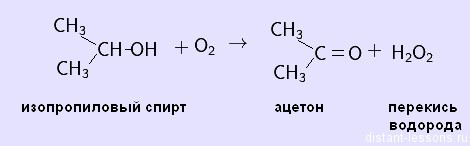
Методы получения:
Благодаря своим сильным окислительным свойствам пероксид водорода нашёл широкое применение в быту и в промышленности, где используется, например, как отбеливатель, в аналитической химии, в медицине — как антисептик, в производстве дезинфицирующих и отбеливающих средств.
Перекись водорода применяется также для обесцвечивания волос (пергидроль) и отбеливания зубов, однако эффект в обоих случаях основан на окислении, а следовательно, разрушении тканей, и потому такое применение (особенно в отношении зубов) не рекомендуется специалистами.
http://chemrise.ru/theory/inorganic_11/rules_hydrogen_peroxide_11
http://distant-lessons.ru/svojstva-perekisi-vodoroda.html