Выражение для кинетического уравнения реакции i го порядка
ФИЗИЧЕСКАЯ И КОЛЛОИДНАЯ ХИМИЯ
Конспект лекций для студентов биофака ЮФУ (РГУ)
2.1 СКОРОСТЬ ХИМИЧЕСКОЙ РЕАКЦИИ
2.1.1 Кинетическое уравнение химической реакции. Порядок реакции.
Одной из задач, стоящих перед химической кинетикой, является определение состава реакционной смеси (т.е. концентраций всех реагентов) в любой момент времени, для чего необходимо знать зависимость скорости реакции от концентраций. В общем случае, чем больше концентрации реагирующих веществ, тем больше скорость химической реакции. В основе химической кинетики лежит т. н. основной постулат химической кинетики :
Скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ, взятых в некоторых степенях.
Т. е. для реакции
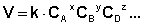
Коэффициент пропорциональности k есть константа скорости химической реакции . Константа скорости численно равна скорости реакции при концентрациях всех реагирующих веществ, равных 1 моль/л.
Зависимость скорости реакции от концентраций реагирующих веществ определяется экспериментально и называется кинетическим уравнением химической реакции. Очевидно, что для того, чтобы записать кинетическое уравнение, необходимо экспериментально определить величину константы скорости и показателей степени при концентрациях реагирующих веществ. Показатель степени при концентрации каждого из реагирующих веществ в кинетическом уравнении химической реакции (в уравнении (II.4) соответственно x, y и z) есть частный порядок реакции по данному компоненту. Сумма показателей степени в кинетическом уравнении химической реакции (x + y + z) представляет собой общий порядок реакции . Следует подчеркнуть, что порядок реакции определяется только из экспериментальных данных и не связан со стехиометрическими коэффициентами при реагентах в уравнении реакции. Стехиометрическое уравнение реакции представляет собой уравнение материального баланса и никоим образом не может определять характера протекания этой реакции во времени.
В химической кинетике принято классифицировать реакции по величине общего порядка реакции. Рассмотрим зависимость концентрации реагирующих веществ от времени для необратимых (односторонних) реакций нулевого, первого и второго порядков.
2.1.2 Реакции нулевого порядка
Для реакций нулевого порядка кинетическое уравнение имеет следующий вид:
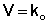
Скорость реакции нулевого порядка постоянна во времени и не зависит от концентраций реагирующих веществ; это характерно для многих гетерогенных (идущих на поверхности раздела фаз) реакций в том случае, когда скорость диффузии реагентов к поверхности меньше скорости их химического превращения.
2.1.3 Реакции первого порядка
Рассмотрим зависимость от времени концентрации исходного вещества А для случая реакции первого порядка А ––> В. Реакции первого порядка характеризуются кинетическим уравнением вида (II.6). Подставим в него выражение (II.2):
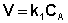
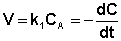
После интегрирования выражения (II.7) получаем:
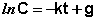
Константу интегрирования g определим из начальных условий: в момент времени t = 0 концентрация С равна начальной концентрации Со. Отсюда следует, что g = ln Со. Получаем:
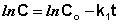
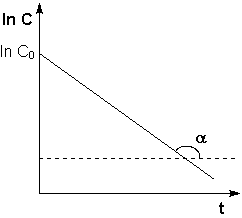
Рис. 2.3 Зависимость логарифма концентрации от времени для реакций
первого порядка
Т.о., логарифм концентрации для реакции первого порядка линейно зависит от времени (рис. 2.3) и константа скорости численно равна тангенсу угла наклона прямой к оси времени.
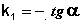
Из уравнения (II.9) легко получить выражение для константы скорости односторонней реакции первого порядка:
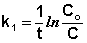
Еще одной кинетической характеристикой реакции является период полупревращения t1/2 – время, за которое концентрация исходного вещества уменьшается вдвое по сравнению с исходной. Выразим t1/2 для реакции первого порядка, учитывая, что С = ½Со:
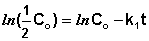
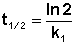
Как видно из полученного выражения, период полупревращения реакции первого порядка не зависит от начальной концентрации исходного вещества.
2.1.4 Реакции второго порядка
Для реакций второго порядка кинетическое уравнение имеет следующий вид:
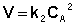
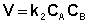
Рассмотрим простейший случай, когда кинетическое уравнение имеет вид (II.14) или, что то же самое, в уравнении вида (II.15) концентрации исходных веществ одинаковы; уравнение (II.14) в этом случае можно переписать следующим образом:
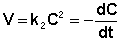
После разделения переменных и интегрирования получаем:
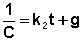
Постоянную интегрирования g, как и в предыдущем случае, определим из начальных условий. Получим:
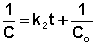
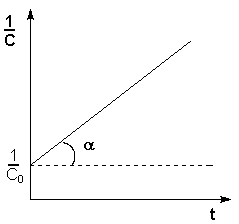
Т.о., для реакций второго порядка, имеющих кинетическое уравнение вида (II.14), характерна линейная зависимость обратной концентрации от времени (рис. 2.4) и константа скорости равна тангенсу угла наклона прямой к оси времени:
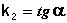
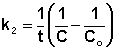
Рис. 2.4 Зависимость обратной концентрации от времени для реакций
второго порядка
Если начальные концентрации реагирующих веществ Cо,А и Cо,В различны, то константу скорости реакции находят интегрированием уравнения (II.21), в котором CА и CВ – концентрации реагирующих веществ в момент времени t от начала реакции:
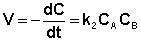
В этом случае для константы скорости получаем выражение
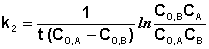
Порядок химической реакции есть формально-кинетическое понятие, физический смысл которого для элементарных (одностадийных) реакций заключается в следующем: порядок реакции равен числу одновременно изменяющихся концентраций. В случае элементарных реакций порядок реакции может быть равен сумме коэффициентов в стехиометрическом уравнении реакции; однако в общем случае порядок реакции определяется только из экспериментальных данных и зависит от условий проведения реакции. Рассмотрим в качестве примера элементарную реакцию гидролиза этилового эфира уксусной кислоты (этилацетата), кинетика которой изучается в лабораторном практикуме по физической химии:
Если проводить эту реакцию при близких концентрациях этилацетата и воды, то общий порядок реакции равен двум и кинетическое уравнение имеет следующий вид:
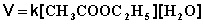
При проведении этой же реакции в условиях большого избытка одного из реагентов (воды или этилацетата) концентрация вещества, находящегося в избытке, практически не изменяется и может быть включена в константу скорости; кинетическое уравнение для двух возможных случаев принимает следующий вид:
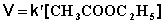
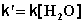
2) Избыток этилацетата:
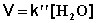
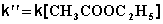
В этих случаях мы имеем дело с т.н. реакцией псевдопервого порядка . Проведение реакции при большом избытке одного из исходных веществ используется для определения частных порядков реакции.
Copyright © С. И. Левченков, 1996 — 2005.
Кинетические уравнения 1-, 2- и 0-го порядка
ТЕОРЕТИЧЕСКИЕ ОСНОВЫ РАБОТЫ
Скорость химической реакции определяется как изменение концентрации одного из реагирующих веществ или продуктов реакции в единицу времени. Среднюю скорость реакции в промежутке времени от t1 до t2 рассчитывают следующим образом:

где с1 и с2 – концентрация вещества в моменты времени t1 и t2 соответственно.
Знак плюс берется при расчете скорости по продукту реакции, в ходе реакции концентрация продукта возрастает, с2 > с1, Dс>0. Знак минус берется при расчете скорости по одному из исходных реагентов, концентрация его при протекании реакции убывает, с2 3 либо в моль/дм 3 (моль/л), время – в секундах, минутах, часах.
Скорость химической реакции зависит от природы реагирующих веществ, концентрации, температуры и присутствия в системе катализатора.
Для всякой химической реакции зависимость скорости реакции от концентраций реагирующих веществ выражается законом действующих масс: скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ в соответствующих степенях

где ci – концентрация i-го реагента. Показатель степени при концентрации называется порядком реакции по i-му веществу. Сумма показателей степеней при концентрациях в законе действия равна суммарному порядку реакции. Для простых реакций показатель степени совпадает со стехиометрическим коэффициентом в уравнении реакции. Коэффициент пропорциональности k в законе действующих масс называется константой скорости. Величина k численно равна скорости химической реакции при концентрациях реагирующих веществ, равных единице. Константа скорости химической реакции является характеристикой каждой конкретной реакции, зависит от температуры и не зависит от концентраций.
Уравнения, связывающие скорость химической реакции с концентрациями, а также выражающие зависимость концентраций от времени, называются кинетическими уравнениями (см. таблицу 1).
Таблица 1
Кинетические уравнения 1-, 2- и 0-го порядка
| Порядок реакции | Выражение закона действующих масс | Единица измерения константы скорости | Кинетическое уравнение | Зависимость периода полураспад от начальной концентрации |
 | с -1 |  |  | |
 | л×моль -1 ×с -1 |  | 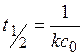 | |
 | моль×л -1 ×с -1 |  |  |
Для определения численного значения константы скорости необходимо тем или иным методом определить концентрацию реагирующего вещества в различные моменты времени и подставить эти значения в выражение для константы скорости (см. таблицу). Константу скорости можно также найти графически.
Изучаемая в данной работе реакция окисления иодид-ионов пероксидом водорода в водном растворе в кислой среде протекает по уравнению:
Механизм реакции сложный, включает несколько стадий. В целом в реакции участвуют три вида частиц, и в реакционной смеси могут изменяться концентрации всех этих частиц, влияя на скорость реакции. При избытке кислоты (ионов H + ) концентрация [H + ] может считаться постоянной. Концентрацию иодид-ионов [I – ] можно поддерживать постоянной. Для этого в ходе опыта к реакционной смеси периодически добавляют одинаковые количества тиосульфата натрия Na2S2O3. Тиосульфат реагирует с выделяющимся при реакции (1) иодом по уравнению
Таким образом, пероксид водорода расходуется в реакции, а концентрация иодид-ионов остается практически постоянной. Кинетическое уравнение реакции окисления v = k [H + ][I – ] n [H2O2] = kэксп [H2O2], где kэксп = k [H + ][I – ] n есть величина постоянная при соблюдении вышеуказанных условий, n – порядок реакции по I – . kэксп – экспериментально наблюдаемая константа скорости реакции первого порядка по пероксиду водорода.
Определить константу скорости реакции окисления иодид-ионов пероксидом водорода в кислой среде.
Ø раствор KI, 0,4 %-ный
Ø раствор крахмала 0,5 %-ный (индикатор)
Ø раствор молибдата аммония (NH4)2MoO4 (катализатор)
Ø Коническая колба на 250 мл
Ø Пипетки на 100 мл, 10 мл, 5 мл
Ø Бюретка 25 мл
1. В коническую колбу наливают мерной колбой 100 мл раствора KI и пипеткой 5 мл раствора H2SO4.
2. Бюретку заполняют раствором тиосульфата натрия. В течение опыта раствор тиосульфата в бюретку не добавляют!
3. В колбу с подкисленным раствором иодида из бюретки добавляют точно 1 мл раствора тиосульфата. Приливают 5 капель раствора крахмала.
4. В эту же колбу наливают пипеткой 10 мл пероксида водорода, тщательно перемешивают и ставят под бюретку с тиосульфатом.
5. В момент окрашивания реакционной смеси в синий цвет включают секундомер. Немедленно добавляют еще 1 мл тиосульфата и перемешивают, окраска раствора исчезает.
6. Отмечают момент следующего окрашивания раствора (секундомер не выключают!), сразу добавляют следующий мл раствора тиосульфата. Записывают время появления окрашивания по секундомеру.
7. Продолжают наблюдение, производят 6-7 таких отсчетов по секундомеру, соответствующих окрашиванию реакционной смеси, каждый раз приливая по 1 мл раствора тиосульфата.
Затем добавляют 3-5 капель раствора молибдата аммония в качестве катализатора. Реакция проходит до конца, т.е. весь пероксид водорода вступает в нее. Выделившийся при этом иод оттитровывают тиосульфатом до исчезновения окраски. Записывают окончательный (общий) объем тиосульфата V0. Общее количество Na2S2O3 эквивалентно начальному количеству H2O2.
По ходу опыта результаты измерений заносят в таблицу 2.
Условия проведения опыта: t = °C.
| Объем раствора Vt Na2S2O3, вступившего в реакцию к моменту времени t, мл | Момент появления окраски, t |  |
| По секундомеру | Перевод в секунды | |
| V0 |
Обработка результатов.
1. Рассчитывают константу скорости изучаемой реакции по формуле, приводят три значащих цифры.
2. Рассчитывают среднее значение К по данным таблицы и указывают его в выводе.
3. Строят график зависимости ln(V0-Vt) от времени и определяют по нему значение константы скорости. Указывают значение К в выводе.
Контрольные вопросы и задания.
1. Дайте определения следующим понятиям: химическая кинетика, скорость реакции, средняя и истинная скорость, порядок, молекулярность реакции. В каких единицах может измеряться скорость химической реакции?
2. Какие факторы влияют на скорость химической реакции, на значение константы скорости химической реакции?
3. Сформулируйте закон действия масс. Запишите его математическое выражение. Что называется общим порядком реакции, порядком реакции по веществу?
4. Запишите кинетическое уравнение реакции нулевого, первого, второго порядков. Как экспериментально можно определить константу скорости реакции первого порядка?
5. Что называется временем полупревращения (периодом полураспада)?
6. Какие уравнения описывают зависимость скорости реакции от температуры?
7. Дайте понятие энергии активации реакции.
8. Приведите химизм процесса, протекающего в данном опыте.
9. Какого порядка эта реакция и как это определить?
10. Взаимодействие оксида углерода (II) с хлором выражается уравнением:
концентрация оксида углерода (II) равно 0,3 моль/л, а хлора – 0,2 моль/л. как изменится скорость прямой реакции, если увеличить концентрацию оксида углерода (II) до 1,2 моль/л, а концентрацию хлора до 0,6 моль/л? считать, что это реакция второго порядка.
11. При помощи правила Вант-Гоффа вычислите, при какой температуре реакция закончится через 28 мин, если при 20 о С на это требуется 1,5 ч. температурный коэффициент скорости равен 2,5.
12. Для реакции C12H22O11 + H2O ↔ C6H12O6 + C6H12O6 константа скорости при температуре 298,2 к равна 0,765 л/(моль. мин), а при температуре 328,2 к — 35,5 л/(моль. мин). найдите энергию активации этой реакции и константу скорости при температуре 304,5 К.
13. Константа скорости рекомбинации ионов H + и ФГ — (фенилглиоксинат) в молекулу нфг при 298 К равна K = 1011.59 л/(моль. с). рассчитайте время, в течение которого реакция прошла на 70%, если исходные концентрации обоих ионов равны 0.001 моль/л.
Выражение для кинетического уравнения реакции i го порядка
Из уравнений (4) и (5) видно, что критериями первого порядка реакции по реагенту А является линейная зависимость ln [ A ] – t или ln 
В тоже время по тангенсам углов наклона линейных зависимостей можно определить константы скорости.
Другой тест правильности выбранного первого порядка является постоянство константы скорости реакции, вытекающее из уравнения (5)
Размерность константы скорости первого порядка dim < k >= [1/ c ], [1/мин] или соответственно с -1 , мин -1
Третий тест основан на концентрационной зависимости времени полупревращения. Условие полупревращения [ A ] = 0,5[ A ]0 , тогда в соответствии с уравнением (5)
Можно видеть, что критерием первого порядка реакции является независимость времени полупревращения t ½ от начальной концентрации реагента [ A ]0.
Примерами подобных реакций первого порядка являются реакции изомеризации, а также реакции разложения некоторых сложных молекул в газовой фазе.
и в жидкой фазе, например, гидролиз трет-бутилбромида.
Для реакции A + B → C + D можно записать уравнение скорости
Обозначим [ A ]0 и [ B ]0 – начальными концентрациями реагентов А и В, а Х – количество прореагировавших А и В, тогда уравнение (1) приобретет вид
Разделяя переменные, имеем
Проинтегрируем левую часть этого уравнения методом неопределенных коэффициентов, для чего представим дробь
в виде суммы дробей
Решая совместно эти уравнения, имеем

Подставляя значения α и β в уравнение (3) и (4) и интегрируя полученные уравнения в соответствующих пределах
Из уравнения (5) видно, что критерием правильности выбранного второго порядка реакции является линейность зависимости

По тангенсу угла наклона этой зависимости можно определить константу скорости реакции. Другим критерием правильности выбранного второго порядка является постоянство значений k , вычисленных в соответствии с уравнением (5):
во всем диапазоне пар значений τ – х.
Размерность константы скорости второго порядка

Если вещества А и В взяты в равных количествах или реакция идет с участием одного вещества, например
то при постоянстве объема удобно использовать в качестве переменной концентрацию одного из исходных веществ
тогда кинетическое уравнение будет иметь вид
Интегрируя это уравнение в соответствующих пределах
приходим к выражению
Из уравнений (7) и (8) следует, что критериями правильности выбранного второго порядка являются линейный характер зависимости 1/[ A ] от t и постоянство значения k , вычисленных для различных пар значений [ A ] – t по формуле
Третий критерий правильности второго порядка основан на определении времени полупревращения t ½ . Так как [ A ] = 0.5[ A ]0, то в соответствии с уравнением (7)

Можно видеть, что критерием второго порядка является обратно пропорциональная зависимость между t ½ и начальной концентрацией реагента. В соответствии с выражениями (7) и (8) константы скорости второго порядка можно определить по тангенсу угла наклона зависимостей 

Имеется множество реакций протекающих по кинетике второго порядка:
и простой случай, соответствующий равенству исходных и текущих концентраций реагентов
Разделяя переменные и интегрируя
Из уравнения (3) видно, что критериями правильности выбранного третьего порядка является линейность зависимостей 

для всех пар значений t и [ A ] и обратно пропорциональная зависимость между временем полупревращения и квадратом начальной концентрации реагента
В соответствии с уравнением (3) константа скорости третьего порядка может быть определена по тангенсу угла наклона зависимости 

Интегрирование уравнения (1)
приводит к выражениям
Из уравнений (2) и (3) следует, что критериями нулевого порядка по реагенту А являются линейный характер зависимости [ A ] от t , постоянство k , вычисленного по формуле

Из уравнений (2) и (3) следует, что константа скорости нулевого порядка может быть определена по тангенсу угла наклона зависимостей [ A ]0 – [ A ] или [ A ] от времени
Сложные реакции представляют собой совокупность простых реакций. К сложным реакциям относятся обратимые реакции.
При кинетическом анализе сложных реакций руководствуются принципом независимости простых реакций, согласно которому каждая простая реакция, входящая в сложную ведет себя кинетически так, как если бы она была единственная.
в начальный момент времени концентрация реагента A составляет [ A ]0, а [ B ] = 0, то уравнение этой реакции запишется как
Выражая r через концентрацию [A] имеем


где X – количество молей вещества A в единице объеме, которое прореагировало к моменту τ и соответственно количество молей вещества B в единице объеме, которое образовалось к этому моменту. Преобразуя правую часть уравнения (2)

В условиях равновесия
При τ ® ¥ X стремится к своему равновесному значению X ® X ¥ . Тогда
где
Тогда кинетическое уравнение (3) примет вид
Интегрируя это уравнение в соответствующих пределах
и
В соответствии с выражениями (6) и (7) кинетические зависимости для A и B будут иметь следующий вид
Пользуясь интегральной формой кинетического уравнения (5) и соотношением 
Так, в соответствии с (5)
так как 
Подставляя последнее выражение в уравнение (8), имеем
Подставляя выражение (10) в уравнение (8), имеем
Рассмотрим систему параллельных реакций первого порядка
В соответствии с ранее принятыми обозначениями суммарная скорость расходования реагента A выразится уравнением
По форме уравнение (1) подобно кинетическому уравнению необратимой реакции первого порядка, поэтому его интегральная форма имеет вид.
Разрешая уравнение (2) относительно [ A ] имеем
Для определения констант k 1 и k 2 рассмотрим уравнения конкурирующих параллельных реакций.
Поделив почленно, левые и правые части уравнений (5) и (6), имеем уравнение 
Разделяя, левые и правые части уравнений (5) и (1), (6) и (7), приходим к очевидным равенствам

интегрирование которых дает уравнения:

Подставляя в последние уравнения выражение (4) приходим к равенствам
Уравнения (2) и (8) являются основой для определения абсолютных значений констант скорости конкурирующих реакций k 1 и k 2 . На первом этапе можно определить сумму констант скоростей k 1 + k 2 , пользуясь уравнением (2). Затем на основе линейных зависимостей между XB и X , а также XC и X определяют брутто константы 

Нетрудно показать, что для трех параллельных реакций первого порядка


Этот случай более сложен по сравнению с предыдущим. Рассмотрим систему параллельных реакций
Уравнение скорости расхода A в этой системе реакций с учетом его количества, прореагировавшего к моменту времени t (Х) имеет вид:
или с учетом преобразований
обозначая 
Разделяя переменные, приходим к выражению
Интегрируем левую часть уравнения (3) методом неопределенных коэффициентов, для чего представим левую её часть в виде суммы дробей.

так как 

Тогда 
Откуда 

С учетом (4) возвращаемся к уравнению (3)
Интегрирование уравнения (5) приводит к выражению
Откуда
или
Возвращаясь к соотношению 
Рассмотрим систему двух последовательных реакций первого порядка
В силу принципа независимости скорости расходования реагента A выражается уравнением скорости необратимой реакции первого порядка
Решение которого дается в виде


Уравнение скорости изменения концентрации промежуточных продуктов
Разделим почленно левые и правые части уравнений (3) и (1)
Уравнение (4) имеет признаки однородного уравнения первого порядка. Для его решения вводим обозначение
Подставляя последнее выражение в уравнение (4), имеем:
Разделяем переменные и интегрируем
и
тогда
и
или
Так как 
В тоже время в соответствии с уравнением (2)
Тогда уравнение (5) можно преобразовать в форму
Выведенные зависимости показывают, что в случае необратимых последовательных реакций уравнение для первого промежуточного продукта связано с характеристиками лишь первых двух стадий, оставаясь одинаковым при любом числе и характеристиках последующих стадий. При этом независимо от начальной концентрации реагента A , значение второй характеристики материального баланса 
Используя уравнение (5) можно найти 
Из анализа уравнения (6) следует, что при XA = 0 и XA = 1 

откуда
и значение максимума
Из выражений (8) и (9) видно, что положение и величина максимума промежуточного продукта в необратимых реакциях первого порядка зависит только от соотношения констант скоростей первых двух стадий. При этом, чем больше величина 

Уравнение образования продукта C :
Максимальная скорость 
Легко видеть, что это условие соответствует одновременно условию максимума концентрации B , определяемого уравнениями(8) и (9). Качественно проанализированные зависимости могут быть представлены графически.
Неэлементарные реакции состоят из ряда элементарных стадий, составляющих их механизм. Кинетика таких реакций определяется последовательностью элементарных стадий, их характером (обратимые, необратимые), природой реагентов, интермедиатов и продуктов реакции. При кинетическом анализе неэлементарных реакций возникает задача определения концентраций интермедиатов, играющих ключевую роль в образовании продуктов или расходовании реагентов. В качестве инструмента такого определения используется принцип квазистационарных концентраций Боденштейна – Семенова. Согласно этому принципу скорость изменения концентраций нестабильных интермедиатов пренебрежимо мала по сравнению со скоростью изменения концентраций реагентов и продуктов реакции и её можно считать равной нулю. Применение принципа стационарных концентраций к неэлементарным реакциям, протекающим по сложному механизму, позволяет исключить из кинетического описания процессов неизвестные концентрации интермедиатов и получить одно или некоторый минимум дифференциальных уравнений скорости, выраженных через подлежащие измерению концентрации реагентов и продуктов реакции.
Рассмотрим пример неэлементарной реакции, описываемой стехиометрией
и протекающей через образование интермедиата Q
Скорость реакции можно приравнять к скорости образования продукта B
В соответствии с принципом квазистационарных концентраций
откуда
Подставляя последнее выражение в уравнение (1) приходим к уравнению скорости реакции
Если экспериментально возможно непосредственно измерить скорость реакции, то обработку кинетических данных можно провести, преобразуя уравнение (3) как:
Последнее уравнение приводится к виду
Обрабатывая зависимость (4) в координатах 

http://allrefrs.ru/5-28618.html
http://www.trotted.narod.ru/physchem/26.htm