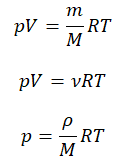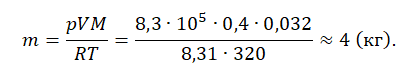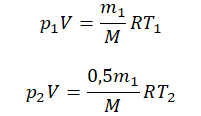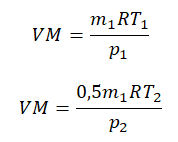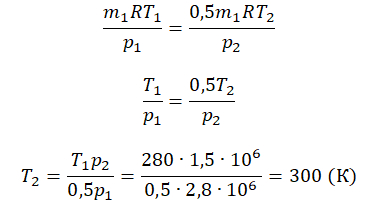Уравнение состояния идеального газа
теория по физике 🧲 молекулярная физика, МКТ, газовые законы
Уравнение состояния идеального газа было открыто экспериментально. Оно носит название уравнения Клапейрона — Менделеева. Это уравнение устанавливает математическую зависимость между параметрами идеального газа, находящегося в одном состоянии. Математически его можно записать следующими способами:
Уравнение состояния идеального газа
Внимание! При решении задач важно все единицы измерения переводить в СИ.
Пример №1. Кислород находится в сосуде вместимостью 0,4 м 3 под давлением 8,3∙10 5 Па и при температуре 320 К. Чему равна масса кислорода? Молярная масса кислорода равна 0,032 кг/моль.
Из основного уравнения состояния идеального газа выразим массу:
Уравнение состояния идеального газа следует использовать, если газ переходит из одного состояния в другое и при этом изменяется его масса (количество вещества, число молекул) или молярная масса. В этом случае необходимо составить уравнение Клапейрона — Менделеева отдельно для каждого состояния. Решая систему уравнений, легко найти недостающий параметр.
Подсказки к задачам
| Давление возросло на 15% | p2 = 1,15p1 |
| Объем увеличился на 2% | V2 = 1,02V1 |
| Масса увеличилась в 3 раза | m2 = 3m1 |
| Газ нагрелся до 25 о С | T2 = 25 + 273 = 298 (К) |
| Температура уменьшилась на 15 К (15 о С) | T2 = T1 – 15 |
| Температура уменьшилась в 2 раза | 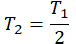 |
| Масса уменьшилась на 20% | m2 = 0,8m1 |
| Выпущено 0,7 начальной массы | |
| Какую массу следует удалить из баллона? | Нужно найти разность начальной и конечной массы: |
| Газ потерял половину молекул | 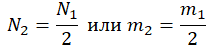 |
| Молекулы двухатомного газа (например, водорода), диссоциируют на атомы | 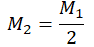 |
| Озон (трехатомный кислород) при нагревании превращается в кислород (двухатомный газ) | M (O3) = 3Ar (O)∙10 –3 кг/моль M (O2) = 2Ar (O)∙10 –3 кг/моль |
| Открытый сосуд | Объем V и атмосферное давление pатм остаются постоянными |
| Закрытый сосуд | Масса m, молярная масса M, количество вещества ν, объем V, число N и концентрация n частиц, плотность ρ— постоянные величины |
| Нормальные условия | Температура T0 = 273 К Давление p0 = 10 5 Па |
| Единицы измерения давления | 1 атм = 10 5 Па |
Пример №2. В баллоне содержится газ под давлением 2,8 МПа при температуре 280 К. Удалив половину молекул, баллон перенесли в помещение с другой температурой. Определите конечную температуру газа, если давление уменьшилось до 1,5 МПа.
2,8 МПа = 2,8∙10 6 Па
1,5 МПа = 1,5∙10 6 Па
Так как половина молекул была выпущена, m2 = 0,5m1. Объем остается постоянным, как и молярная масса. Учитывая это, запишем уравнение состояния идеального газа для начального и конечного случая:
Преобразим уравнения и получим:
Приравняем правые части и выразим искомую величину:

Алгоритм решения
Решение
График построен в координатах (V;Ek). Процесс 1–2 представляет собой прямую линию, исходящую из начала координат. Это значит, что при увеличении объема растет средняя кинетическая энергия молекул. Но из основного уравнения МКТ идеального газа следует, что мерой кинетической энергии молекул является температура:
Следовательно, когда кинетическая энергия молекул растет, температура тоже растет.
Запишем уравнение Менделеева — Клапейрона:
Так как количество вещества одинаковое для обоих состояния 1 и 2, запишем:
ν R = p 1 V 1 T 1 . . = p 2 V 2 T 2 . .
Мы уже выяснили, что объем и температура увеличиваются пропорционально. Следовательно, давление в состояниях 1 и 2 равны. Поэтому процесс 1–2 является изобарным, давление во время него не меняется.
Процесс 2–3 имеет график в виде прямой линии, перпендикулярной кинетической энергии. Так как температуры прямо пропорциональна кинетической энергии, она остается постоянной вместе с этой энергией. Следовательно, процесс 2–3 является изотермическим, температура во время него не меняется. Мы видим, что объем при этом процессе уменьшается. Но так как объем и давление — обратно пропорциональные величины, то давление на участке 2–3 увеличивается.
pазбирался: Алиса Никитина | обсудить разбор | оценить
На высоте 200 км давление воздуха составляет примерно 10 –9 от нормального атмосферного давления, а температура воздуха Т – примерно 1200 К. Оцените плотность воздуха на этой высоте.
Уравнение состояния. Для определения многих физических свойств природных газов используется уравнение состояния.
Для определения многих физических свойств природных газов используется уравнение состояния.
Уравнением состояния называется аналитическая зависимость между параметрами, описывающими изменение состояние вещества. В качестве таких параметров используется давление, температура, объём.
Состояние газа при нормальных и стандартных условиях описывается уравнением Менделеева–Клапейрона:
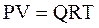
где Р – абсолютное давление, Па;
Q – количество вещества, кмоль;
Т – абсолютная температура, К;
R – универсальная газовая постоянная, Па×м 3 /(кмоль×град).
На основе уравнения состояния газа можно рассчитать много параметров для системы нефтяного газа: плотность, мольный объём, количество молекул, число молекул, парциальные давления и др., если рассматривать уравнение состояния газа для 1 моля, т.е., Q = 1 моль. С учетом этого, уравнение состояния газа можно преобразовать следующим образом:
При ∑N = 1 моль, следует, что: P·V = R·T. Зная, что масса (m) одного моля идеального газа равна его молекулярной массе (М), умножив левую и правую части на молекулярную массу и массу газа, соответственно получим:
Поделив обе части на V·R·T: и преобразовав 2.19, получим выражение для расчета плотности:
P·M / R·T = m / V, m / V = M·P / R·T, r = M·P / R·T. (2.20)
Рассмотрим пример. Дан один моль метана CH4.
Найти его плотность?
Решение. Зная, что молекулярная масса метана равна 16 г/моль и метан занимает объём при н.у. = 22,414 л, а при с.у. = 24,055 л, найдем:
Плотность смеси газовых компонентов рассчитывают с учетом средней молекулярной массы смеси газа (Mсм), как отношение его молекулярной массы к его мольному объёму (Vм). Например, при нормальных условиях (н.у.) она будет рассчитываться по выражению:
Из расчетов и из выражений 2.20, 2.21 следует, что плотность газа с возрастанием температуры будет уменьшаться, а с возрастанием давления (2.20) будет расти.
Рассмотрим другой пример. Определить плотность метана СН4 при избыточном давлении, например при давлении 3,5 атм и температуре 0°С. Решение. В этом случае общее давление в системе будет равно:
Р = (3,5 + 1) = 4 (атм).
Зная, что молекулярная масса метана = 16 г/моль, универсальная газовая постоянная (R) = 0,08206 атм•л/(К•моль), а температура (T) = 273,15 К, найдем плотность метана:
rCH4 = Р·М / R·T = (3,5 + 1)·16 /0,08206 ·273,15 = 3,21 (г/л).
Относительная плотность газов рассчитывается по отношению к плотности воздуха, определенного при тех же условиях:
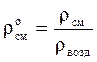
При нормальных условий (н.у.) плотность воздуха (ρвозд) » 1,293; при стандартных условий (с.у.) — ρвозд » 1,205.
Если плотность газа (ρо) задана при атмосферном давлении = 0,1013 МПа, то пересчёт её на другое давление (Р) при той же температуре для идеального газа производится по формуле:
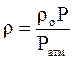
Рассмотрим пример. Для условий задачи, рассмотренной выше (см. пример раздела 2.2) можно рассчитать абсолютные (r) и относительные (ρ о см) плотности смеси, используя правое выражение (2.16) для расчета молекулярной массы:
Мсм = 100 / (36,5 / 16 +17,2 / 30 +19,8 / 44 +14,7 / 58 +11,8 / 72)
rcv = 26,874 / 22,41 = 1,119 (кг/м 3 );
ρ о см (н.у.) = 1,119 / 1,293 = 0,927.
Аналогично из (2.20) находится и выражение для мольного объёма:
Отсюда, мольный объём при давлениях равному 1 атм или близких к атмосферному и для физических процессов, когда не происходит изменения числа молей в системе оценивается соотношением:
где R – универсальна газовая постоянная, R = 0,08206 атм·л/(К·моль);
Т – температура, К;
Рассмотрим пример. Найти вид зависимости изменения мольного объёма газа от температуры V = f(T).
Решение. Воспользуемся выражением 2.25 и получим объём, занимаемый одним молем идеального газа при условиях задачи:
Vн.у. = 0,08206•273,15 = 22,414 (л),
Vс.у. = 0,08206•293,15 = 24,055 (л).
Любой газ при нормальных условиях (н.у. Þ Т = 0 о С и Р = 760 мм рт. ст.) занимает объём равный 22,414 м 3 , а при стандартных (с.у. Þ Т = 20 о С и Р = 760 мм рт. ст.) объём равный 24,055 м 3 .
С увеличением температуры мольный объём газа увеличивается. Мольный объём газов с возрастанием температуры будет расти, а с возрастанием давления (см. 2.24) уменьшаться.
У этого уравнения есть свои граничные условия. Оно справедливо для описания поведения газов при давлениях близких к атмосферному (от 1 до 10–12 атм) и при температурах до 20 о С. При повышенном давлении газ сжимается и его состояние отличается от поведения идеальных газов.
Дата добавления: 2015-08-08 ; просмотров: 1477 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Определение плотности газа по результатам измерения давления и температуры датчиками Arduino
Введение
Задача измерения параметров газовой смеси широко распространена в промышленности и торговле. Проблема получения достоверной информации при измерении параметров состояния газовой среды и её характеристик с помощью технических средств разрешается принятыми в стандартах методиками выполнения измерений (МВИ), например, при измерении расхода и количества газов с помощью стандартных сужающих устройств [1], или с помощью турбинных, ротационных и вихревых расходомеров и счётчиков [2].
Периодический газовый анализ позволяет установить соответствие между реальной анализируемой смесью и её моделью, по которой в МВИ учитываются физико-химические параметры газа: состав газовой смеси и плотность газа при стандартных условиях.
Также в МВИ учитываются теплофизические характеристики газа: плотность при рабочих условиях (давление и температура газа, при которых выполняют измерение его расхода или объёма), вязкость, фактор и коэффициент сжимаемости.
К измеряемым в реальном режиме времени параметрам состояния газа относятся: давление (перепад давлений), температура, плотность. Для измерения этих параметров применяются соответственно средства измерительной техники: манометры (дифманометры), термометры, плотномеры. Измерение плотности газовой среды допускается измерять прямым или косвенным методами измерения. Результаты как прямых, так и косвенных методов измерения зависят от погрешности средств измерения и методической погрешности. В рабочих условиях, сигналы измерительной информации могут быть подвержены влиянию значительного шума, среднее квадратичное отклонение которого может превышать инструментальную погрешность. В этом случае, актуальной задачей является эффективная фильтрация сигналов измерительной информации.
В данной статье рассматривается методика косвенного измерения плотности газа при рабочих и стандартных условиях c применением фильтра Калмана.
Математическая модель определения плотности газа
Обратимся к классике и вспомним уравнение состояния идеального газа [3]. Имеем:
1. Уравнение Менделеева-Клапейрона:



R — универсальная газовая постоянная,

T — абсолютная температура, T=273.16 К.
2. Два измеряемых параметра:
p – давление газа, Па
t – температура газа, °С.
Известно, что молярный объём 


Также известно, что

где: m – масса газа, M – молярная масса газа.
Учитывая (2) и (3) перепишем (1) в виде:

Как известно, плотность вещества


Из (4) и (5) выведем уравнение для плотности газа


и введём обозначение параметра


Если состав газовой смеси не меняется, то параметр k является константой.
Итак, для расчёта плотности газа необходимо рассчитать молярную массу газовой смеси.
Молярную массу смеси веществ определяем, как среднее арифметическое взвешенное молярной массы массовых долей, входящих в смесь индивидуальных веществ.
Примем известным состав веществ в газовой смеси – в воздухе, который состоит из:
- 23 % по весу из молекул кислорода
- 76 % по весу из молекул азота
- 1 % по весу из атомов аргона
Молярные массы этих веществ воздуха будут соответственно равны:

Вычисляем молярную массу воздуха, как среднее арифметическое взвешенное:
Теперь, зная значение константы


Приведение плотности газа к нормальным, стандартным условиям
Практически, измерения свойств газов проводят в различных физических условиях, и для обеспечения сопоставления между различными наборами данных должны быть установлены стандартные наборы условий [4].
Стандартные условия для температуры и давления – это установленные стандартом физические условия, с которыми соотносят свойства веществ, зависящие от этих условий.
Различные организации устанавливают свои стандартные условия, например: Международный союз чистой и прикладной химии (IUPAC), установил в области химии определение стандартной температуры и давления (STP): температура 0 °C (273.15 K), абсолютное давление 1 бар ( Па); Национальный институт стандартов и технологий (NIST) устанавливает температуру 20 °C (293,15 K) и абсолютное давление 1 атм (101.325 кПа), и этот стандарт называют нормальной температурой и давлением (NTP); Международная организация по стандартизации (ISO) устанавливает стандартные условия для природного газа (ISO 13443: 1996, подтверждённый в 2013 году): температура 15.00 °С и абсолютное давление 101.325 кПа.
Поэтому, в промышленности и торговле необходимо указывать стандартные условия для температуры и давления, относительно которых и проводить необходимые расчёты.
Плотность воздуха мы рассчитываем по уравнению (8) в рабочих условиях температуры и давления. В соответствии с (6) запишем уравнение для плотности воздуха в стандартных условиях: температура 


Делаем расчёт плотности воздуха, приведенной к стандартным условиям. Разделим уравнение (9) на уравнение (6) и запишем это отношение для 

Подобным образом, получим уравнение для расчёта плотности воздуха, приведенной к нормальным условиям: температура 


В уравнениях (10) и (11) используем значения параметров воздуха 
Реализация измерительного канала давления и температуры
Для решения многих задач получения информации, в зависимости от их сложности, удобно создавать прототип будущей системы на базе одной из микроконтроллерных платформ типа Arduino, Nucleo, Teensy, и др.
Что может быть проще? Давайте сделаем микроконтроллерную платформу для решения конкретной задачи – создание системы измерения давления и температуры, затрачивая меньше, возможно, средств, и используя все преимущества разработки программного обеспечения в среде Arduino Software (IDE).
Для этого, на аппаратном уровне, нам понадобятся компоненты:
- Arduino (Uno, …) – используем как программатор;
- микроконтроллер ATmega328P-PU – микроконтроллер будущей платформы;
- кварцевый резонатор на 16 МГц и пара керамических конденсаторов на 12-22 пФ каждый (по рекомендациям фирмы-изготовителя);
- тактовая кнопка на перезагрузку микроконтроллера и подтягивающий плюс питания к выводу RESET микроконтроллера резистор на 1 кОм;
- BMP180 — измерительный преобразователь температуры и давления с интерфейсом I2C;
- преобразователь интерфейсов TTL/USB;
- расходные материалы – провода, припой, монтажная плата, и др.
Принципиальная схема платформы, с учетом необходимых интерфейсов: стандартного последовательного интерфейса, I2C, и ничего более, представлена на рис. 1.

Рис. 1 — Принципиальная схема микроконтроллерной платформы для реализации системы измерения давления и температуры
Теперь рассмотрим этапы осуществления нашей задачи.
1. Прежде, нам нужен программатор. Подключаем Arduino (Uno, …) к компьютеру. В среде Arduno Software из меню по пути Файл->Примеры->11. ArdunoISP добираемся до программы программатора ArduinoISP, которую зашиваем в Arduino. Предварительно из меню Инструменты выбираем соответственно Плату, Процессор, Загрузчик, Порт. После Загрузки программы ArduinoISP в плату, наша Arduino превращается в программатор и готова к использованию по назначению. Для этого в среде Arduno Software в меню Инструменты выбираем пункт Программатор: “Arduino as ISP”.
2. Подключаем по интерфейсу SPI ведомый микроконтроллер ATmega328P к ведущему программатору Arduino (Uno, …), рис. 2. Следует заметить, что предварительно биты регистра Low Fuse Byte микроконтроллера ATmega328P были установлены в незапрограммированное состояние. Переходим в среду Arduno Software и из меню Инструменты выбираем пункт Записать Загрузчик. Прошиваем микроконтроллер ATmega328P.

Рис. 2 – Схема подключения микроконтроллера к программатору
3. После успешной прошивки, микроконтроллер ATmega328P готов к установке на разработанную микроконтроллерную платформу (рис. 3), которую программируем также, как и полноценную Arduino (Uno, …). Программа опроса измерительного преобразователя давления и температуры представлена на листинге 1.

Рис. 3 Система измерения давления и температуры
Программа Python для фильтрации по каналам температуры и давления, и получение результатов
Программа Python методики определения плотности газа по результатам измерений давления и температуры представлена на листинге 2. Информация из измерительной системы выводится в реальном режиме времени.
Результаты расчёта представлены листингом и рис. 4, 5, 6.

Рис. 4 – результаты измерения (красный) и фильтрации (синий) давления

Рис. 5 – результаты измерения (красный) и фильтрации (синий) температуры

Рис. 6 – результаты расчёта плотности воздуха, приведенной к стандартным условиям (температура 273.15 К; абсолютное давление 101.325 кПа)
Выводы
Разработана методика определения плотности газа по результатам измерения давления и температуры с применением датчиков Arduino и программных средств Python.
http://helpiks.org/4-56994.html
http://habr.com/ru/post/412915/