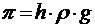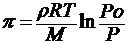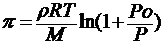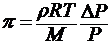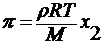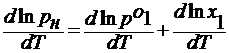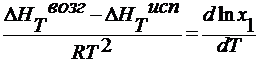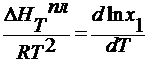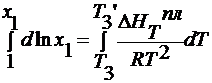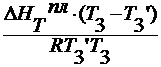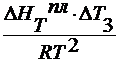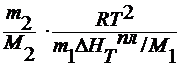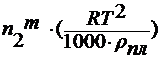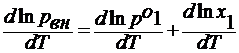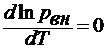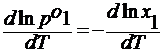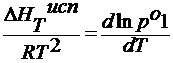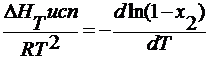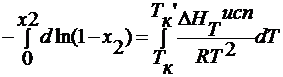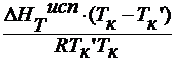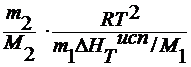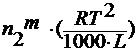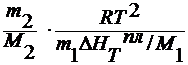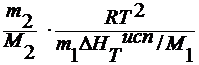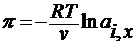Вывод уравнения вант гоффа для осмотического давления
65. Осмос. Определение осмотического давления и уравнения его вычисления.
Осмос – это самопроизвольный переход растворителя в раствор через полупроницаемую перегородку. Избыточное давление, которое необходимо приложить к раствору на высоте h = 0, чтобы воспрепятствовать проникновению растворителя в раствор, называют осмотическим давлением. Величина этого давления равна весу столба жидкости в трубке высотою h .
Осмотическое давление может быть рассчитано по выражению
где ρ — плотность раствора,
g – сила земного притяжения,
h – вес столба жидкости.
Величина осмотического давления зависит от концентрации раствора. Вант-Гофф установил, что осмотическое давление растворов прямолинейно меняется с изменением их концентрации, а произведение их осмотического давления на объём раствора, содержащего 1 моль растворенного вещества, есть величина постоянная и равна
π ∙ ν = 22,9 Дж/моль
Осмотическое давление равно такому давлению, которое развивало бы растворенное вещество в заданном объёме раствора, если бы оно находилось в идеальном газообразном состоянии и занимало бы объём указанного раствора.
Растворы, обладающие одинаковыми осмотическими давлениями, называют изоосмотическими. Для растворов одинакового объёма осмотическое давление прямо пропорционально температуре:
для разбавленных растворов неэлектролитов : π ∙ ν / T = R
учитывая, что ν = 1/ C , получаем уравнение Вант-Гоффа :
66. Термодинамический вывод уравнения Вант-Гоффа осмотического давления.
Пусть в заданном сосуде давление, развиваемое 1 молем пара от Ро до Р, производит работу за счёт изменения величины потенциальной энергии, которую можно определить по выражению 1-го закона термодинамики при Т= const в таком виде:
знак минус определяет затраченную системой работу. Для идеального газа v = RT / p , откуда получим
интегрируем в пределах от Ро до Р:
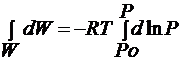
1 моль вещества можно механически перенести на высоту h , затрачивая работу
W = Mgh , где М – молекулярная масса растворителя.
Тогда Mgh = RT ln Po / P
Откуда h =
Для разбавленного раствора давление насыщенного пара над чистой жидкостью po = p + ∆ p
Для разбавленных растворов ∆ p / р
допуская ρ = n 1 / v и М=М1, получим
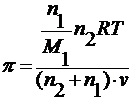
67. Связь осмотического давления с понижением давления для разбавленных растворов.
Осмометр термостатирован . В нём через некоторое время устанавливается динамическое равновесие, которое характеризуется равенством скоростей обмена жидкостью между раствором и растворителем через пленку.
В равновесном состоянии системы давление пара над поверхностью чистой жидкости будет равно Ро , а над поверхностью раствора на высоте h – P = P ’. Давление пара Ро над уровнем чистой жидкости будет выше, чем давление над раствором на высоте h на величину ∆Р = Ро – Р. Условие равенства Р = Р’ над раствором на высоте h доказывается невозможностью построения вечного двигателя при Т = const , в равновесной изолированной системе. Этот двигатель невозможно построить и в открытых системах.
где ρ — плотность раствора, кг/м 3 ;
g – сила земного притяжения, м/ c 2 ;
В этом случае π имеет размерность н /м 2 . Изменение давления насыщенного пара растворителя с изменением высоты h можно определить по формуле Лапласа
h = 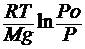
Для разбавленного раствора давление насыщенного пара над чистой жидкостью po = p + ∆ p
Для разбавленных растворов ∆ p / р
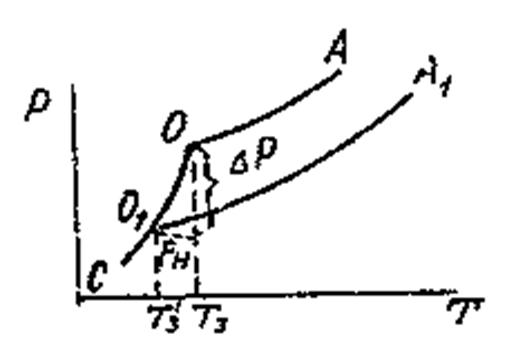
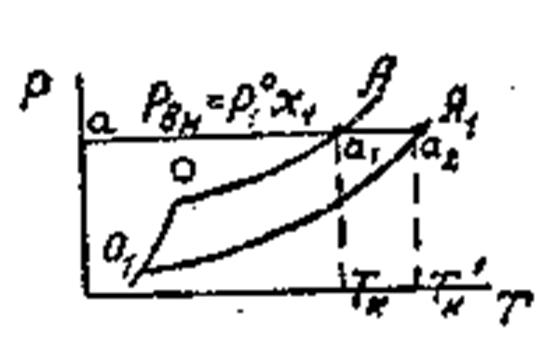
Жидкость замерзает при условии, что давление насыщенного пара над нею равно давлению над твёрдым телом. На рис. Это условие выполняется в точке пересечения кривых СО и ОА, при температуре Т3. Раствор также замерзает, когда давление пара над ним будет равно давлению насыщенного пара над твёрдым растворителем, что определяется точкой О1 от пересечения кривых О1А1 и СО1. В этой точке давление ниже, чем в точке О, поэтому раствор замерзает при более низкой температуре, чем чистая жидкость, то есть при Т3’. Давление над разбавленным раствором снижается согласно закону Рауля
где рн , р1 о – давление над твёрдым телом в растворе и чистым растворителем.
∆ HT возг , ∆ HT исп – мольные теплоты возгонки и испарения Дж/моль.
для разбавленных растворов Т3 — Т3’ мала, поэтому ∆ HT пл = const :
lnx 1 = 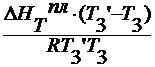
— ln (1- x 2 )=
для разбавленных растворов Т3 ≈ Т3’ , x 2
x 2 =
для разбавленных растворов n 1 >> n 2, тогда x 2 = 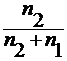
x 2 =
∆ T 3 =
∆ HT пл / M 1 = ρ пл – удельная теплота плавления
∆ T 3 =
∆ T 3 = 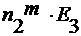
где n 2 m – моляльность раствора;
E 3 – эбулиоскопическая константа.
69. Термодинамический вывод уравнения, связывающего повышение температуры кипения раствора с его моляльностью .
На рис. кривые ОА и О1А1 определяют изменение давления насыщенного пара над чистой жидкостью и над раствором. Для определения условий, при которых закипают жидкости, проводим изобару внешнего давления, которая пересекает кривые в точках а1 и а2. Эти точки определяют Ткип чистой жидкости и раствора. Жидкость закипает при условии, что давление пара её равно внешнему давлению. Над раствором давление пара ниже, чем над чистой жидкостью, на величину∆р , поэтому для закипания раствора его необходимо дополнительно нагреть до Тк ’, причем
Формула закона Рауля для растворителя
∆ HT исп – молекулярная теплота испарения жидкости, Дж/моль.
для бинарной смеси х1 = 1- х2
— ln (1- x 2 )=
для разбавленных растворов x 2
x 2 =
n 1 >> n 2, тогда x 2 = 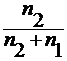
x 2 =
∆ T к =
∆ HT исп / M 1 = L – удельная теплота испарения
∆ T к =
∆ T к = 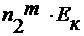
где n 2 m – моляльность раствора;
E к – эбулиоскопическая константа.
70. Свойства разбавленных растворов электролитов и методы их вычисления. Изотонический коэффициент.
Разбавленные растворы электролитов – солей, оснований, кислот в воде – показывают систематические отклонения от свойств идеальных растворов. Эти отклонения связаны с тем, что молекулы электролита в водном растворе распадаются на ионы, и в единице объёма раствора будет содержаться большее число частиц, чем в исходной загрузке соли, кислоты, основания.
Для расчета свойств разбавленных растворов электролитов необходимо уравнения законов идеальных растворов исправить, введя в них коэффициент, учитывающий изменение числа частиц в растворе вследствие диссоциации или ассоциации растворенного вещества. Этот коэффициент обозначают i и называют изотоническим коэффициентом. Он показывает отношение числа частиц, образующихся в растворе, к числу частиц в исходной порции вещества. Для электролитов:
N 1 – число образовавшихся ионов или распавшихся молекул
N(1-α) – число нераспавшихся молекул
Σ Ni = N — Nα + Nα + Nα i = Σ Ni / N = 1+ α
если исходные молекулы распадаются на ν новых частиц, то
Σ Ni = N [1+ α ( ν -1)] i = Σ Ni / N = 1+ α ( ν -1)
если α =0, то i =1, если α =1, то i = ν .
Для раствора, в котором молекулы растворенных веществ ассоциируют друг с другом:
Nα / n – число ассоциированных молекул
N (1- α ) – число исходных молекул
Σ Ni = N — Nα + Nα /n i = Σ Ni/N = 1+α(1/n -1)
С учетом этой поправки законы разбавленных растворов электролитов запишутся:
71. Определение молекулярной массы растворенного вещества по понижению температуры замерзания раствора, по повышению температуры кипения раствора и по осмотическому давлению.
1 . по понижению температуры замерзания раствора
x 2 =
для разбавленных растворов n 1 >> n 2, тогда x 2 = 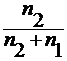
x 2 = 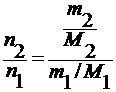
∆ HT пл / M 1 = ρ пл – удельная теплота плавления
M2 = 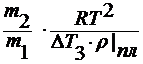
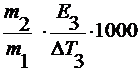
где ∆ T 3 – понижение температуры замерзания раствора;
E 3 – эбулиоскопическая константа.
2. по повышению температуры кипения раствора
x 2 = 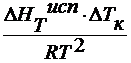
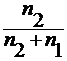
x 2 = 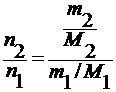
∆ HT исп / M 1 = L – удельная теплота испарения
M2 = 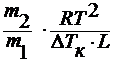
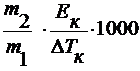
где ∆ Тк – повышению температуры кипения раствора;
E к – эбулиоскопическая константа.
3. по осмотическому давлению
уравнение Вант-Гоффа : π = cRT
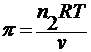
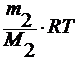
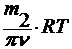
где π – осмотическое давление.
72. Методы расчета активностей и коэффициентов активности растворителя и растворенного вещества по давлению насыщенного пара, осмотическому давлению, по повышению температуры кипения и понижению температуры замерзания растворов.
1. по давлению насыщенного пара
2. по осмотическому давлению
3. по повышению температуры кипения
∆ T к = 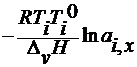
4. по понижению температуры замерзания растворов
∆ T 3 = 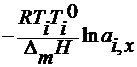
Коллигативные свойства растворов
Любому раствору характерны те или иные физические свойства, к которым относятся и коллигативные свойства растворов. Это такие свойства, на которые не оказывает влияние природа растворенного вещества, а зависят они исключительно от количества частиц этого растворенного вещества.
К коллигативным свойствам растворов относятся:
- Понижение давление паров
- Повышение температуры кипения
- Понижение температуры затвердевания (кристаллизации)
- Осмотическое давление раствора.
Рассмотрим подробнее каждое из перечисленных свойств.
Понижение давления паров
Давление насыщенного пара (т.е. пара, который пребывает в состоянии равновесия с жидкостью) над чистым растворителем называется давлением или упругостью насыщенного пара чистого растворителя.
Если в некотором растворителе растворить нелетучее вещество, то равновесное давление паров растворителя при этом понижается, т.к. присутствие какого – либо вещества, растворенного в этом растворителе, затрудняет переход частиц растворителя в паровую фазу.
Экспериментально доказано, что такое понижение давления паров напрямую зависит от количества растворенного вещества. В 1887 г. Ф.М. Рауль описал количественные закономерности коллигативных свойств растворов.
Первый закон Рауля
Первый закон Рауля заключается в следующем:
Давление пара раствора, содержащего нелетучее растворенное вещество, прямо пропорционально мольной доле растворителя в данном растворе:
p — давление пара над раствором, Па;
p0 — давление пара над чистым растворителем, Па;
χр-ль — мольная доля растворителя.
nв-ва и nр-ля – соответственно количество растворенного вещества и растворителя, моль.
Иногда Первому закону Рауля дают другую формулировку:
относительное понижение давления насыщенного пара растворителя над раствором равно мольной доле растворенного вещества:
При этом принимаем, что χв-ва + χр-ль= 1
Изотонический коэффициент Вант-Гоффа
Для растворов электролитов данное уравнение приобретает несколько иной вид, в его состав входит изотонический коэффициент i:
Δp — изменение давления паров раствора по сравнению с чистым растворителем;
i – изотонический коэффициент.
Изотонический коэффициент (или фактор Вант-Гоффа) — это параметр, не имеющий размерности, который характеризует поведение какого – либо вещества в растворе.
То есть, изотонический коэффициент показывает, разницу содержания частиц в растворе электролита по сравнению с раствором неэлектролита такой же концентрации. Он тесно связан связан с процессом диссоциации, точнее, со степенью диссоциации и выражается следующим выражением:
n – количество ионов, на которые диссоциирует вещество.
α – степень диссоциации.
Повышение температуры кипения или понижение температуры затвердевания (кристаллизации). Второй закон Рауля
Равновесное давление паров жидкости имеет тенденцию к увеличению с ростом температуры, жидкость начинает кипеть, при уравнивании давления ее паров и внешнего давления.
При наличии нелетучего вещества, давление паров раствора снижается, и раствор будет закипать при более высокой температуре, по сравнению с температурой кипения чистого растворителя.
Температура замерзания жидкости также определяется той температурой, при которой давления паров жидкой и твердой фаз уравниваются.
Ф.М. Рауль доказал, что повышение температуры кипения, так же как и понижение температуры замерзания разбавленных растворов нелетучих веществ, прямо пропорционально моляльной концентрации раствора и не зависит от природы растворённого вещества. Это правило известно как Второй закон Рауля:
K — криоскопическая константа,
mв-ва — моляльность вещества в растворе.
Растворы электролитов не подчиняются Законам Рауля. Но для учёта всех несоответствий Вант-Гофф предложил ввести в приведённые уравнения поправку в виде изотонического коэффициента i, учитывающего процесс распада на ионы молекул растворённого вещества:
Осмотическое давление раствора
Некоторые материалы имеют способность к полупроницаемости, т.е. им свойственно пропускать частицы определенного вида и не пропускать частицы другого вида.
Перемещение молекул растворителя (но не растворенного, в нем вещества), через полупроницаемую мембрану в раствор с большей концентрацией из более разбавленного представляет собой такое явление как осмос.
Представим два таких раствора, которые разделены полупроницаемой мембраной, как показано на рисунке выше. Растворы стремятся к выравниванию концентраций, поэтому вода будет проникать в раствор, тем самым уменьшая его концентрацию.
Для того, чтобы осмос приостановить, необходимо приложить внешнее давление к раствору. Такое давление, которое требуется приложить, называется осмотическим давлением.
Осмотическое давление и концентрацию раствора неэлектролита позволяет связать уравнение Вант — Гоффа, которое напоминает уравнение идеального газа Клапейрона – Менделеева:
где C — молярная концентрация раствора, моль/м 3 ,
R — универсальная газовая постоянная (8,314 Дж/моль·К);
T — абсолютная температура раствора.
Преобразуем уравнение следующим образом:
C = n/V = m/(M·V)
π = т·R·T / M·V или
Для растворов электролитов осмотическое давление определяется уравнением, в которое входит изотонический коэффициент:
где i — изотонический коэффициент раствора.
Для растворов электролитов i > 1, а для растворов неэлектролитов i = 1.
Если полупроницаемой перегородкой разделены два раствора, имеющие одинаковое осмотическое давление, то перемещение растворителя через перегородку отсутствует. Такие растворы называются изотоническими.
Раствор, с меньшим осмотическим давлением, по сравнению с более концентрированным раствором, называют гипотоническим, а раствор с большей концентрацией – гипертоническим.
Осмос. Осмотическое давление. Закон Вант-Гоффа
Если привести в соприкосновение два раствора с разными концентрациями, то молекулы растворителя и растворенного вещества будут диффундировать в противоположных направлениях, преимущественно в том направлении, где их концентрация ниже. Такая двусторонняя диффузия приведет к выравниванию концентраций (С1=С2).
Рассмотрим особый случай односторонней диффузии, когда на границе между раствором и растворителем или между двумя растворами различной концентрации находится перегородка, проницаемая для молекул растворителя и задерживающая частицы растворенного вещества.
Представим себе, что в сосуд с водой опущен цилиндр с раствором, нижняя часть которого изготовлена из материала, пропускающего растворитель, но не пропускающего частицы растворенного вещества (полупроницаемая перегородка). Получается неравновесная система, т.к. если в воде N1=1, то в растворе мольная доля растворителя – воды N1
Осмотическое давление Росм зависит от температуры раствора и его концентрации и не зависит от природы растворителя и растворенного вещества. В 1886 г. голландский химик Вант-Гофф показал, что для разбавленных растворовнеэлектролитов зависимость осмотического давления от температуры и концентрации выражается уравнением (закон Вант-Гоффа):

где Росм – осмотическое давление раствора, кПа; С – молярная концентрация растворенного неэлектролита, моль/л; Т – абсолютная температура, К.
Заменим величину С отношением 


Формально уравнение Вант-Гоффа аналогично уравнению состояния идеального газа и выражает сходство в поведении разбавленных растворов неэлектролитов с идеальными газами. Из вышеприведенного уравнения выразим величину М:

Данное выражение позволяет определить молекулярную массу растворенного вещества, измерив осмотическое давление в осмометре.
Явление осмоса играет важную роль в жизни растений, животных и человека. Стенки растительных клеток живых организмов представляют собой полупроницаемые мембраны, через которые свободно проходят молекулы воды, но почти полностью задерживаются вещества, растворенные в клеточном соке. Поэтому осмос служит причиной тургора (состояние напряжения) и плазмолиза (сморщивание) клеток. С ним связаны процессы усвоения пищи и обмена веществ. У высших животных и человека осмотическое давление в разных органах и тканях несколько меньше 8 атм и постоянно. Осмотическое давление широко встречается в природе, например, в скважинах осмотическое давление рвет породы и т.д.
Растворы электролитов
Свойства растворов электролитов. При изучении свойств водных растворов кислот, щелочей и солей, относящихся к электролитам, было установлено, что они не подчиняются законам Рауля и Вант-Гоффа. Они имеют бо́льшие, чем вычисленные по соответствующим формулам, понижениедавления насыщенного пара растворителя над раствором ( 




Изотонический коэффициент показывает, во сколько раз экспериментальные величины 




Коэффициент i показывает меру отклонения растворов электролитов от закономерностей для неэлектролитов;он всегда больше единицы (i>1), стремится к целому числу.
Электролитическая диссоциация.Наблюдаемые отклонения для растворов электролитов, а также их способность проводить электрический ток были объяснены на основе теории электролитической диссоциации, созданной шведским ученым Аррениусом (1883 г.).
Основные положения теории электролитической диссоциации:
1.Электролитическая диссоциация – распад молекул электролитов на ионы в среде растворителя.
2. Электролиты при растворении в воде распадаются (диссоциируют) на положительно и отрицательно заряженные ионы.
3. Под действием электрического тока положительно заряженные ионы движутся к катоду, отрицательно заряженные – к аноду. Поэтому первые называют катионами, вторые – анионами.
4. Сумма положительных зарядов в растворе равна сумме отрицательных зарядов, поэтому раствор в целом электронейтрален.
5. Ионы представляются как точечные заряды, взаимодействия между которыми отсутствуют (подобны идеальным газовым смесям).
6. Диссоциация – процесс обратимый, поскольку одновременно протекают процесс распада молекул на ионы (диссоциация) и процесс соединения ионов в молекулы (ассоциация). Например, уравнение диссоциации молекулы электролита КА на катион К + и анион Аˉ записывается так:
КА D К + + 
Согласно теории Аррениуса, вследствие диссоциации электролитов на ионы, с одной стороны, увеличивается общее число частиц в растворе, а следовательно, возрастают понижение давления пара и изменение температуры кипения и замерзания, с другой стороны – ионы обусловливают способность раствора проводить электрический ток.
Физический смысл изотонического коэффициента i состоит в увеличении общего числа частиц в растворе за счет диссоциации растворенного вещества на ионы.
Однако теория Аррениуса рассматривала ионы как свободные не зависимые от молекул растворителя частицы, не учитывала всей сложности явлений в растворах. Теории Аррениуса противостояла химическая, или гидратная, теория растворов Менделеева, в основе которой лежало представление о взаимодействии растворенного вещества с растворителем. В преодолении кажущегося противоречия обеих теорий большая заслуга принадлежит русскому ученому И. А. Каблукову, впервые высказавшему предположение о гидратации ионов. Развитие этой идеи привело в дальнейшем к объединению теории Аррениуса и Менделеева.
В создании современной физико-химической теории растворов большую роль сыграли работы русских ученых Д. И. Менделеева, И. А. Каблукова, Д.П. Коновалова, В. А. Кистяковского и др.
Сольватация (гидратация). По современным представлениям причиной электролитической диссоциации является физико-химическое взаимодействие между полярными молекулами и ионами растворяемого вещества и полярными молекулами растворителя (сольватация), приводящее к образованию соединений сольватов (комплексов). В случае, если вода – растворитель, говорят о гидратации и образовании гидратов.
Взаимодействие между молекулами и ионами растворяемого вещества и молекулами воды может состоять из нескольких процессов, протекающих последовательно или одновременно: молекулярной диссоциации, образования сольватов, ионизации и электролитической диссоциации. В зависимости от типа растворяющихся веществ число стадий может изменяться. Так, в случае ионных кристаллов стадии образования гидратов и электролитическая диссоциация совмещены.
В случае ассоциированных веществ первой стадией является молекулярная диссоциация растворенного вещества. Процесс молекулярной диссоциации происходит вследствие химического взаимодействия между молекулами растворяемого вещества КА, (m+n) молекулами воды с образованием гидратированной молекулы КА(m+n)Н2О:
Образующийся гидрат диссоциирует на гидратированные ионы (стадия электролитической диссоциации):
КА(m+n)Н2О D К + ·mН2О + А – ·nН2О. (б) Схематично процесс гидратации, на примере реакций (а) и (б), представлен

Процесс гидратации может остановиться на любой стадии. Если процесс гидратации останавливается на стадии (а), то система представляет собой раствор неэлектролита. Она характеризуется отсутствием ионов в растворе и соответственно не обладает ионной электрической проводимостью. Если процесс гидратации протекает до стадии (б), то система является раствором электролита, т.е. имеет место электролитическая диссоциация с образованием ионов. Уравнение электролитической диссоциации можно записать, опустив промежуточные стадии, указав лишь начальные и конечные продукты реакции:
Особенностью гидратов (сольватов) как химических соединений является то, что коэффициенты n и m меняются с изменением концентрации, температуры и других параметров раствора. Поэтому приведенные формулы гидратов (сольватов) не отражают их истинного стехиометрического состава, и в уравнениях химических реакций гидратированные ионы обычно записывают, например, К + ·aq, А – · aq.
Однако часто в подобных уравнениях опускают молекулы растворителя, записывая их в таком виде:
Электролитическая диссоциация протекает самопроизвольно (∆G + + SО4 2- .
К сильным электролитам в водных растворах относятся почти все соли, основания щелочных и щелочноземельных металлов, кислоты: H2SO4, HNO3, HCl, HBr, HI, HСlO4, HClO3, HBrO4, HBrO3, HIO3, H2SeO4, HMnO4, H2MnO4 и т.д.
К слабым электролитам относятся электролиты, степень диссоциации которых в растворах меньше единицы (α + + ОН —
К слабым электролитам относят воду, почти все органические кислоты (муравьиную, уксусную, бензойную и т.д.), ряд неорганических кислот (H2SO3, HNO2, H2CO3, H3AsO4, H3AsO3, H3BO3, H3PO4, H2SiO3, H2S, H2Se, H2Te, HF, HCN, HCNS), основания p-, d-, f- элементов (Al(OH)3, Cu(OH)2, Fe(OH)2 и т.д.), гидроксид аммония, гидроксиды магния и бериллия, некоторые соли (CdI2, CdCl2, HgCl2, Hg(CN)2, Fe(CNS)3 и т.д.).
Численное значение степени электролитической диссоциации зависит от различных факторов:
1. Природа растворителя.
Это связано с величиной диэлектрической проницаемости растворителя ε. Как следует из закона Кулона, сила (f) электростатического притяжения двух разноименно заряженных частиц зависит не только от величины их зарядов (q1 и q2), расстояния между ними r, но и от природы среды, в которой взаимодействуют заряженные частицы, т.е. от ε:

Например, при 298 К ε(Н2О) = 78,25, а ε(С6Н6) = 2,27. Такие соли, как KCl, LiCl, NaCl и др., в воде полностью диссоциированы на ионы, т.е. ведут себя как сильные электролиты; в бензоле эти соли диссоциируют лишь частично, т.е. являются слабыми электролитами. Таким образом, одни и те же вещества могут проявлять различную способность к диссоциации в зависимости от природы растворителя.
У сильных электролитов с повышением температуры степень диссоциации уменьшается, у слабых – при повышении температуры до 60°С α увеличивается, а затем начинает уменьшаться.
3. Концентрация раствора.
Если рассматривать диссоциацию как равновесный химический процесс, то в соответствии с принципом Ле Шателье добавление растворителя (разбавление водой), как правило, увеличивает количество продиссоциированных молекул, что приводит к увеличению α. Процесс образования молекул из ионов в результате разбавления затрудняется: для образования молекулы должно произойти столкновение ионов, вероятность которого с разбавлением уменьшается.
4. Наличие одноименных ионов.
Добавление одноименных ионов уменьшает степень диссоциации, что также согласуется с принципом Ле Шателье. Например, в растворе слабой азотистой кислоты при электролитической диссоциации устанавливается равновесие между недиссоциированными молекулами и ионами:
При введении в раствор азотистой кислоты нитрит-ионов NO2ˉ (прибавлением раствора нитрита калия КNО2) равновесие сместится влево, следовательно, степень диссоциации α уменьшится. Аналогичный эффект даст и введение в раствор ионов Н + .
Необходимо отметить, что не следует путать понятия «сильный электролит» и «хорошая растворимость». Например, растворимость СН3СООН в Н2О неограниченная, однако уксусная кислота относится к слабым электролитам ( 
http://zadachi-po-khimii.ru/obshaya-himiya/kolligativnye-svojstva-rastvorov.html
http://megaobuchalka.ru/5/14723.html