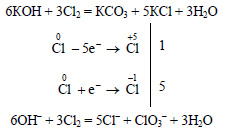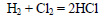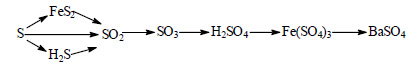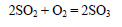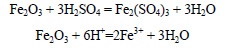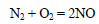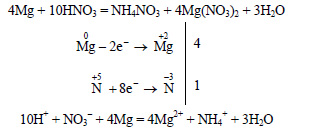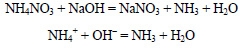Хлорид калия: способы получения и химические свойства
Хлорид калия KCl — соль щелочного металла калия и хлороводородной кислоты. Белое вещество, плавится и кипит без разложения. Умеренно растворяется в воде.
Относительная молекулярная масса Mr = 74,55; относительная плотность для тв. и ж. состояния d = 1, 984; tпл = 770º C; tкип = 1430º C;
Способ получения
1. Хлорид калия можно получить путем взаимодействия калия и разбавленной хлороводородной кислоты, образуются хлорид калия и газ водород:
2K + 2HCl = 2KCl + H2↑.
2. При комнатной температуре, в результате взаимодействия калия и хлора, образуется хлорид калия:
2K + Cl2 = 2KCl
3. Концентрированный раствор гидроксида калия реагирует с концентрированным раствором хлорида аммония при кипении. При этом образуются хлорид калия, газ аммиак и вода:
4. Разбавленная хлороводородная кислота реагирует с гидроксидом калия . Взаимодействие хлороводородной кислоты с гидроксидом калия приводит к образованию хлорида калия и воды:
KOH + HCl = KCl + H2O
5. В результате взаимодействия сульфата калия и хлорида бария образуется сульфат бария и хлорид калия:
6. Карбонат калия взаимодействует с разбавленной соляной кислотой , образуя хлорид калия, углекислый газ и воду:
Качественная реакция
Качественная реакция на хлорид калия — взаимодействие его с нитратом серебра, в результате реакции происходит образование белого творожного осадка:
1. При взаимодействии с нитратом серебра , хлорид калия образует нитрат калия и осадок хлорид серебра:
KCl + AgNO3 = KNO3 + AgCl↓
Химические свойства
1. Хлорид калия вступает в реакцию со многими сложными веществами :
1.1. Хлорид калия взаимодействует с кислотами :
Хлорид калия в твердом состоянии при кипении реагирует с концентрированной серной кислотой с образованием сульфата калия и газа хлороводорода:
1.2. Хлорид калия способен вступать в реакцию с многими солями :
1.2.1. Твердый хлорид калия реагирует с концентрированной и горячей серной кислотой и твердым перманганатом калия . Взаимодействие хлорида калия с перманганатом калия и серной кислотой приводит к образованию сульфата марганца, сульфата калия, газа хлора и воды:
1.2.2. Хлорид калия взаимодействует с гидросульфатом калия при температуре 450–700º C . При этом образуются сульфат калия и хлороводородная кислота:
1.2.3. При взаимодействии концентрированного раствора хлорида калия и насыщенного перхлората натрия выделяются перхлорат калия и хлорид натрия:
KCl + NaClO4 = KClO4↓ + NaCl
Please wait.
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 6e0a808e9aab0099 • Your IP : 85.95.188.35 • Performance & security by Cloudflare
Составьте уравнения реакций, при помощи которых молено осуществить следующие превращения:
Уравнения реакций, если это возможно, составьте в полном и сокращенном ионном виде
Ответ:
а) При реакции хлора с гидроксидом кальция образуется смесь хлорида кальция и гипохлорита кальция:
При реакции хлора с горячим раствором гидроксида калия образуется хлорат калия:
Хлорат калия является сильным окислителем, при его реакции с соляной кислотой выделяется хлор:
Хлор реагирует с водородом с образованием хлороводорода:
При реакции хлороводорода с гидроксидом кальция образуется хлорид кальция:
При реакции раствора хлорида кальция с раствором нитрата серебра в осадок выпадает хлорид серебра:
При реакции хлора с железом при нагревании образуется хлорид железа (III):
При реакции раствора хлорида железа (III) с раствором гексацианоферрата (II) калия (желтая кровяная соль) образуется осадок гексацианоферрата (II) железа (III), так называемая берлинская лазурь:
При реакции серы с железом при нагревании можно получить дисульфид железа FeS2:
Сера реагирует при нагревании с водородом с образованием сероводорода:
При окислении дисульфида железа образуется оксид серы (IV):
Оксид серы (IV) образуется также при сжигании серы или сероводорода:
При окислении оксида серы (IV) кислородом в присутствии катализатора и при повышенной температуре образуется оксид серы (VI) (триоксид серы, серный ангидрид):
Триоксид серы бурно реагирует с водой с образованием серной кислоты:
При реакции серной кислоты с оксидом железа (111) образуется сульфат железа (III):
При реакции сульфата железа (III) с хлоридом бария выпадает осадок сульфата бария:
Азот реагирует с кислородом в условиях электрического разряда с образованием оксида азота (II):
В присутствии катализатора азот реагирует с водородом с образованием аммиака:
При окислении аммиака кислородом в присутствии катализатора образуется оксид азота (II):
Оксид азота (II) окисляется кислородом в оксид азота (IV):
Оксид азота (IV) реагирует в присутствии кислорода с водой с образованием азотной кислоты:
При реакции 30%-ной азотной кислоты с медью выделяется оксид азота (II):
При реакции разбавленной (15%-ной) азотной кислоты с цинком выделяется оксид азота (I):
При реакции сильно разбавленной (5%-ной) азотной кислоты с магнием образуется нитрат аммония:
При действии щелочи на нитрат аммония выделяется аммиак:

задача №11
к главе «Глава VI. Неметаллы».
http://gomolog.ru/reshebniki/1-kurs/shimanovich-2014/381.html
http://5terka.com/node/161