Взаимодействие кислот с оксидами металлов
Разделы: Химия
Цель урока:
- Знакомство учащихся еще с одним свойством кислот — взаимодействие их с оксидами металлов:
а) значение реакции обмена между кислотами и оксидами
б) очистка поверхности металла от ржавчины - Проверить и закрепить полученные знания и умения:
а) типы химических реакций
б) свойства кислот - Обобщение полученных знаний.
- Закрепление знаний учащихся .
- Подготовка к практической работе.
Методы работы:
Беседа. Демонстрация опыта: взаимодействие серной кислоты с оксидом меди(II) . Лабораторные опыты. Взаимодействие соляной кислоты с оксидом магния. Демонстрация опыта. Пропускание оксида углерода (IV) через раствор серной кислоты. Обобщение и наблюдение.
- Какие известные вам кислоты?
- Сравните свойства серной и соляной кислот.
- Какое правило нужно соблюдать при использовании серной кислоты в воде?
- Назовите общие свойства кислот. Ответ поясните примерами.
- Перед вами две кислоты:
а) обратите внимание на их признаки;
б) по этим признакам назовите каждую;
в) запишите их формулы. - Приводятся формулы различных веществ:
а) выпишите из них формулы кислот и назовите их.
б) подчеркните формулы бескислородных кислот: Cu (OH)₂‚ HCl‚ CO₂‚ P₂O₅‚ H₃PO₄‚ KOH‚ H₂SO₄‚H₂S‚ Al₂O₃‚ H₂SO₃‚ CuSO₄‚ HNO₃.
в) определите валентность кислотных остатков. - Пойдут ли реакции:
а) между медью и соляной кислотой;
б) между цинком и соляной кислотой;
в) между железом и разбавленной серной кислотой?
Какой этот тип химической реакции? - Какие известны еще типы химических реакции? Приведите примеры.
Урок начинается с постановки «проблем».
- Взаимодействуют ли кислоты с оксидами металлов, неметаллов?
- Как получить соль металла, не вытесняющего водород из кислоты? Объяснить на примере получения сульфата меди (II).
Решаем первый вопрос: будут ли реагировать кислоты с оксидами металлов? Демонстрация опыта. Взаимодействие оксида меди с серной кислотой.
Показать оксид меди, серную кислоту и предложить учащимся описать их свойства. Затем учитель наливает в стакан объемом 150-200мл. 20-25мл. серной кислоты(1:5), высыпает ложку оксида меди (II), перемешивает. Происходят ли какие изменения? Заметных изменений нет. Нагреваем. Что наблюдаем?
Раствор становится голубым, черный порошок на дне стакана растворился. Добавляем еще немного оксида и перемешиваем до полного его растворения. Добавление оксида меди прекращаем до того, когда новая порция не остается на дне стакана не растворившейся. И только тогда приливаем немного воды.
Что представляет собой раствор голубого цвета? Как выделить образовавшееся вещество из раствора?
- Показать фильтрование горячего раствора:
а) приготовление фильтра.
б) правила фильтрования. - Выпаривание филтрата в фарфоровой чашке.
Обратить внимание на некоторые трудности выпаривания – соль разлетается, чтобы этого избежать, нужно особенно подчеркивать, что раствор надо перемешивать и выпаривать только до появления первых кристаллов, а не досуха.
На доске записываем уравнение реакции:
CuO+H₂SO₄= CuSO₄ + H₂O
Можно ли отнести эту реакцию к одному из известных вам типов?
Атомы меди и водорода поменялись местами. Это реакция обмена. Реакцией обмена называются реакции между двумя сложными веществами, при которых они обмениваются своими составными частями.
Вывод учащихся: при взаимодействии серной кислоты с оксидом меди, получается соль и вода.
Могут ли другие кислоты реагировать с оксидами?
Учащиеся выполняют лабораторные опыты:
- Взаимодействие соляной кислоты с оксидом железа (III).(оксид железа должен быть в виде буро-красного порошка. Темно-серая кристаллическая модификация почти не растворятся в кислотах).
- Взаимодействие оксида магния с соляной кислотой.
Химические свойства кислот
О чем эта статья:
8 класс, 9 класс, ЕГЭ/ОГЭ
Кислоты — это сложные химические вещества, состоящие из одного или нескольких атомов водорода, способных замещаться атомами металла, и кислотных остатков.
Рассмотрим подробнее общие свойства кислот.
Диссоциация
Кислоты — это электролиты, которые при диссоциации образуют катионы водорода и анионы кислотного остатка. Диссоциация кислот происходит ступенчато. По способности к диссоциации кислоты разделяют на две группы:
Хорошо диссоциирующие (сильные): H2SO4, HCl, HBr, HNO3, HClO4, HI.
Разложение
В результате реакций разложения кислородсодержащих кислот образуются кислотный оксид и вода. Бескислородные кислоты образуют простые вещества. Для разложения некоторых кислот необходимо нагревание или излучение (HCl, HNO3, H3PO4) другие же разлагаются самопроизвольно в момент образования (H2CO3, H2SO3, HNO2).
Взаимодействие кислот с металлами
Металл может вытеснять водород из кислоты только в том случае, если металл стоит левее водорода в ряду активности металлов. Продукты реакции — соль и водород.
При взаимодействии с кислотами-окислителями, например, азотной, образуется продукт восстановления кислоты, хотя протекание реакции также неоднозначно.
Высокая окислительная способность серной и азотной кислот позволяет им вступать в реакции с металлами. Продукты реакции будут зависеть от активности металла и от концентрации кислот.
Таблица: химические свойства кислот-окислителей
На холоду — пассивация
На холоду — пассивация
Реакция не проходит
На холоду — пассивация
На холоду — пассивация
Взаимодействие кислот с основаниями
Кислоты реагируют с основаниями и амфотерными гидроксидами, в результате образуются соль и вода. Взаимодействие кислот с основаниями называют реакцией нейтрализации.
NaOH + HCl = NaCl + H2O
Взаимодействие кислот с солями
Сильные кислоты вытесняют слабые из растворов их солей, при этом образуются новая соль и новая кислота. Условие протекания реакции кислот с солями — одним из продуктов реакции должны быть нерастворимая соль или слабая кислота, вода, газ.
Взаимодействие кислот с основными и амфотерными оксидами
Кислоты вступают в реакцию с основными и амфотерными оксидами (последние ведут себя как основные оксиды). В результате реакции образуется соль и вода.
Восстановительные свойства бескислородных кислот
Бескислородные кислоты (кроме HF) проявляют восстановительные свойства за счет химического элемента, который входит в состав аниона, при действии на них различных окислителей.
Например, в качестве окислителей для всех галогеноводородных кислот выступают диоксид марганца MnO2, перманганат калия KMnO4, дихромат калия K2Cr2O7.
Результат этих реакций — образование свободных галогенов.
Из галогеноводородных кислот наибольшая восстановительная активность — у йодоводородной. Ее могут окислять оксид железа (III) и соль трехвалентного железа.
Высокая восстановительная активность характерна для сероводородной кислоты, она может быть окислена диоксидом серы.
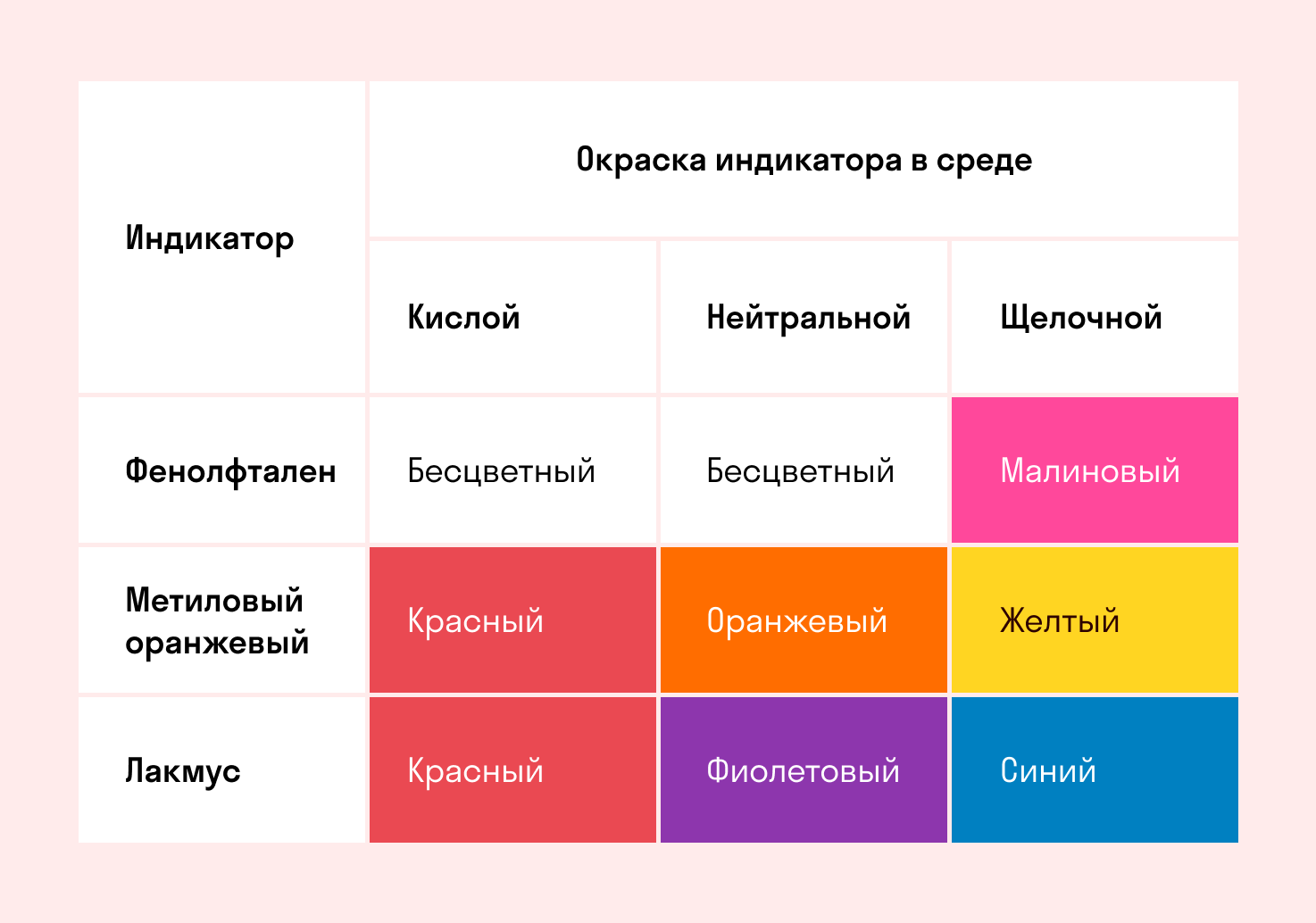
Способность окрашивать индикаторы
Индикаторы кислот — это специальные вещества, при помощи которых определяют наличие кислот в растворе.
Вопросы для самоконтроля
С чем реагируют кислоты?
При каких условиях кислоты взаимодействуют с солями? Приведите пример.
Составьте уравнения реакций и назовите продукты реакций:
Разбавленный раствор серной кислоты реагирует с: медью, хлоридом меди, сульфатом меди, цинком?
Соляная кислота вступает в реакцию с каждым из двух веществ:
Химические свойства основных оксидов
Химические свойства основных оксидов
Подробно про оксиды, их классификацию и способы получения можно прочитать здесь.
1. Взаимодействие с водой. С водой способны реагировать только основные оксиды, которым соответствуют растворимые гидроксиды (щелочи). Щелочи образуют щелочные металлы (литий, натрий, калий, рубидий и цезий) и щелочно-земельные (кальций, стронций, барий). Оксиды остальных металлов с водой химически не реагируют. Оксид магния реагирует с водой при кипячении.
CuO + H2O ≠ (реакция не идет, т.к. Cu(OH)2 — нерастворимый гидроксид)
2. Взаимодействие с кислотными оксидами и кислотами. При взаимодействии основным оксидов с кислотами образуется соль этой кислоты и вода. При взаимодействии основного оксида и кислотного образуется соль:
основный оксид + кислота = соль + вода
основный оксид + кислотный оксид = соль
При взаимодействии основных оксидов с кислотами и их оксидами работает правило:
Хотя бы одному из реагентов должен соответствовать сильный гидроксид (щелочь или сильная кислота).
Иными словами, основные оксиды, которым соответствуют щелочи, реагируют со всеми кислотными оксидами и их кислотами. Основные оксиды, которым соответствуют нерастворимые гидроксиды, реагируют только с сильными кислотами и их оксидами (N2O5, NO2, SO3 и т.д.).
| Основные оксиды, которым соответствуют щелочи | Основные оксиды, которым соответствуют нерастворимые основания |
| Реагируют со всеми кислотами и их оксидами | Реагируют только с сильными кислотами и их оксидами |
| Na2O + SO2 → Na2SO3 | CuO + N2O5 → Cu(NO3)2 |
3. Взаимодействие с амфотерными оксидами и гидроксидами.
При взаимодействии основных оксидов с амфотерными образуются соли:
основный оксид + амфотерный оксид = соль
С амфотерными оксидами при сплавлении взаимодействуют только основные оксиды, которым соответствуют щелочи . При этом образуется соль. Металл в соли берется из более основного оксида, кислотный остаток — из более кислотного. В данном случае амфотерный оксид образует кислотный остаток.
CuO + Al2O3 ≠ (реакция не идет, т.к. Cu(OH)2 — нерастворимый гидроксид)
(чтобы определить кислотный остаток, к формуле амфотерного или кислотного оксида добавляем молекулу воды: Al2O3 + H2O = H2Al2O4 и делим получившиеся индексы пополам, если степень окисления элемента нечетная: HAlO2. Получается алюминат-ион AlO2 — . Заряд иона легко определить по числу присоединенных атомов водорода — если атом водорода 1, то заряд аниона будет -1, если 2 водорода, то -2 и т.д.).
Амфотерные гидроксиды при нагревании разлагаются, поэтому реагировать с основными оксидами фактически не могут.
4. Взаимодействие оксидов металлов с восстановителями.
При оценке окислительно-восстановительной активности металлов и их ионов можно использовать электрохимический ряд напряжений металлов:
Восстановительные свойства (способность отдавать электроны) у простых веществ-металлов здесь увеличиваются справа налево, окислительные свойства ионов металлов — увеличиваются наоборот, слева направо. При этом некоторые ионы металлов в промежуточных степенях окисления могут проявлять также восстановительные свойства (например ион Fe 2+ можно окислить до иона Fe 3+ ).
Более подробно про окислительно-восстановительные реакции можно прочитать здесь.
Таким образом, ионы некоторых металлов — окислители (чем правее в ряду напряжений, тем сильнее). При взаимодействии с восстановителями металлы переходят в степень окисления 0.
4.1. Восстановление углем или угарным газом.
Углерод (уголь) восстанавливает из оксидов до простых веществ только металлы, расположенные в ряду активности после алюминия. Реакция протекает только при нагревании.
FeO + C = Fe + CO
Активные металлы, расположенные в ряду активности левее алюминия, активно взаимодействуют с углеродом, поэтому при взаимодействии их оксидов с углеродом образуются карбиды и угарный газ:
CaO + 3C = CaC2 + CO
Угарный газ также восстанавливает из оксидов только металлы, расположенные после алюминия в электрохимическом ряду:
CuO + CO = Cu + CO2
4.2. Восстановление водородом .
Водород восстанавливает из оксидов только металлы, расположенные в ряду активности правее алюминия. Реакция с водородом протекает только в жестких условиях – под давлением и при нагревании.
CuO + H2 = Cu + H2O
4.3. Восстановление более активными металлами (в расплаве или растворе, в зависимости от металла)
При этом более активные металлы вытесняют менее активные. То есть добавляемый к оксиду металл должен быть расположен левее в ряду активности, чем металл из оксида. Реакции, как правило, протекают при нагревании.
Например , оксид цинка взаимодействует с алюминием:
3ZnO + 2Al = Al2O3 + 3Zn
но не взаимодействует с медью:
ZnO + Cu ≠
Восстановление металлов из оксидов с помощью других металлов — это очень распространенный процесс. Часто для восстановления металлов применяют алюминий и магний. А вот щелочные металлы для этого не очень подходят – они слишком химически активны, что создает сложности при работе с ними.
Алюмотермия – это восстановление металлов из оксидов алюминием.
Например : алюминий восстанавливает оксид меди (II) из оксида:
3CuO + 2Al = Al2O3 + 3Cu
Магниетермия – это восстановление металлов из оксидов магнием.
CuO + Mg = Cu + MgO
Железо можно вытеснить из оксида с помощью алюминия:
При алюмотермии образуется очень чистый, свободный от примесей углерода металл.
4.4. Восстановление аммиаком.
Аммиаком можно восстанавливать только оксиды неактивных металлов. Реакция протекает только при высокой температуре.
Например , аммиак восстанавливает оксид меди (II):
3CuO + 2NH3 = 3Cu + 3H2O + N2
5. Взаимодействие оксидов металлов с окислителями.
Под действием окислителей некоторые основные оксиды (в которых металлы могут повышать степень окисления, например Fe 2+ , Cr 2+ , Mn 2+ и др.) могут выступать в качестве восстановителей.
Например , оксид железа (II) можно окислить кислородом до оксида железа (III):
http://skysmart.ru/articles/chemistry/himicheskie-svojstva-kislot
http://chemege.ru/basicoxides/