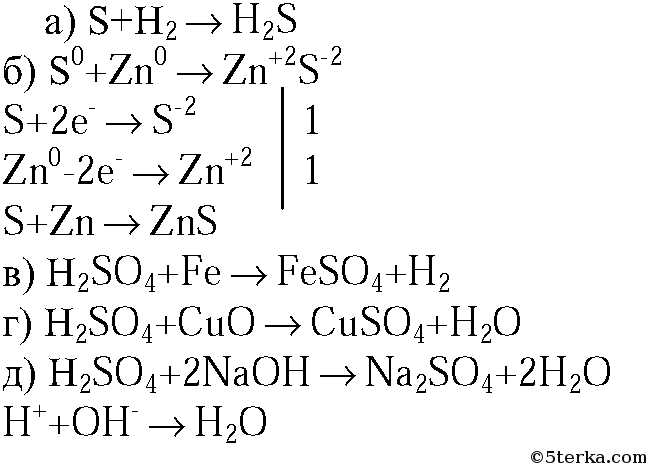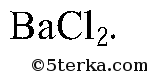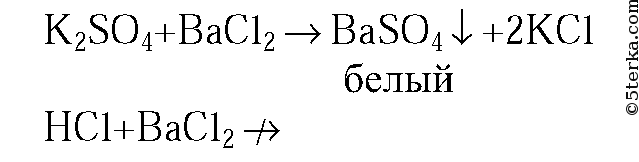Взаимодействие серы с натрием уравнение

Натрий — активный щелочной металл. Во избежание окисления и взаимодействия с парами воды натрий хранят в керосине. Небольшой кусочек натрия помещает в ступку с порошком серы. Осторожно растираем натрий. Он активно взаимодействует с серой. Продукт реакции – сульфид натрия.
Оборудование: ступка фарфоровая с пестиком, шпатель, скальпель, пинцет, фильтровальная бумага.
Техника безопасности. Опыт следует проводить под тягой. Соблюдать правила работы со щелочными металлами. Во избежании химических ожогов обернуть руку полотенцем.
Постановка опыта и текст – к.п.н. Павел Беспалов.
Вариант 3
Вопросы:
1. Составьте уравнения реакций: а) серы с водородом; б) серы с натрием (укажите степени окисления атомов и расставьте коэффициенты с помощью метода электронного баланса); в) раствора серной кислоты с железом; г) раствора серной кислоты с оксидом алюминия; д) раствора серной кислоты с раствором гидроксида кальция (в молекулярной и ионной формах).
2. Напишите названия простых веществ, которые образованы химическими элементами кислородом и серой. Поясните сущность этого явления.
3. В одной пробирке находится раствор сульфата калия, а в другой — соляная кислота. Как можно распознать эти растворы? Напишите уравнения соответствующих реакций.
Ответы и решения:
Это явление (образования нескольких простых веществ одним элементом) носит название аллотропия.
3. Эти вещества можно распознать при помощи раствора

задача №3
к главе «Тема II. Подгруппа кислорода. Основные закономерности течения химических реакций. Работа 1. Кислород. Сера. Серная кислота».
Опыты по химии. Сера и её соединения
Взаимодействие серы с медью
Медь — неактивный металл. Но при повышенных температурах она активно взаимодействует с серой. Нагреем серу в пробирке до кипения. Сера плавится и постепенно закипает. Пробирка наполняется бурыми парами серы. Опустим медную проволоку в пробирку. В парах серы медь загорается. Продукт взаимодействия – черный сульфид меди.
Cu + S = CuS
Оборудование: штатив, пробирка, горелка, тигельные щипцы.
Техника безопасности. Опыт следует проводить под тягой. Соблюдать правила работы с горючими веществами и нагревательными приборами.
Постановка опыта и текст – к.п.н. Павел Беспалов.
Взаимодействие серы с натрием
Натрий — активный щелочной металл. Во избежание окисления и взаимодействия с парами воды натрий хранят в керосине. Небольшой кусочек натрия помещает в ступку с порошком серы. Осторожно растираем натрий. Он активно взаимодействует с серой. Продукт реакции – сульфид натрия.
Na + S = Na2S
Оборудование: ступка фарфоровая с пестиком, шпатель, скальпель, пинцет, фильтровальная бумага.
Техника безопасности. Опыт следует проводить под тягой. Соблюдать правила работы со щелочными металлами. Во избежании химических ожогов обернуть руку полотенцем.
Постановка опыта и текст – к.п.н. Павел Беспалов.
Взаимодействие серы с цинком
Цинк менее активен по сравнению с натрием. Для протекания реакции с серой необходимо нагревание. Смесь порошков серы и цинка поджигаем. Смесь энергично сгорает с образованием сульфида цинка.
Zn + S = ZnS
Оборудование: шпатель, огнезащитная прокладка, горелка, лучина.
Техника безопасности. Соблюдать правила работы с нагревательными приборами. Опыт проводить под тягой.
Постановка опыта и текст – к.п.н. Павел Беспалов.
Получение пластической серы
Сера – кристаллическое вещество. В кристаллах молекулы всегда расположены в строгом порядке. Сера, измельченная в порошок, сохраняет кристаллическую структуру. Нагреем порошок серы. Сера плавится при температуре 120 градусов и становится легко подвижной желтой жидкостью. При дальнейшем повышении температуры сера начинает темнеть, превращается в темно-бурую, вязкую жидкость – пластическую серу. При быстром охлаждении в воде сера сохраняет пластические свойства. Пластическая сера с течением времени кристаллизуется и твердеет.
Оборудование: пробирка, штатив для пробирок, шпатель, химический стакан, спиртовка, держатель для пробирок.
Техника безопасности. Соблюдать правила обращения с нагревательными приборами. Не допускать попадания расплавленной серы на поверхность стола. При возгорании серы тушить пламя речным песком.
Постановка опыта – Елена Махиненко, текст – к.п.н. Павел Беспалов.
Получение сероводорода и изучение его свойств
Сероводород – токсичный бесцветный газ с запахом тухлых яиц. Сероводород (H2S) в лаборатории можно получить нагреванием смеси парафина с серой. В пробирку помещаем кусочек парафина и желтый порошок серы, закрываем пробкой с газоотводной трубкой и нагреваем на пламени спиртовки. Выделяющийся сероводород можно обнаружить с помощью влажной универсальной индикаторной бумаги: под действием сероводорода она краснеет. Раствор сероводорода в воде – очень слабая кислота. Пропускаем сероводород через холодную дистиллированную воду. Сероводород частично растворяется, образуется сероводородная вода. Лакмус краснеет в сероводородной воде, это действительно слабая кислота. Качественная реакция на сульфид ион – реакция с ионами свинца, мы проведем похожую ‑ реакцию с ионами меди. При добавлении сульфата меди к сероводородной воде выпадает черный осадок сульфида меди.
CuSO4 + H2S = CuS ↓+ H2SO4
Так же выглядит осадок сульфида свинца. По черному осадку сульфида свинца можно обнаружить сульфид-ион.
Оборудование: пробирки, газоотводная трубка, штатив, штатив для пробирок, шпатель, щипцы, фарфоровые тигли, спиртовка, держатель для пробирок.
Техника безопасности. Следует соблюдать правила обращения с ядовитыми газами. Опыт необходимо проводить в вытяжном шкафу. Соблюдать правила обращения с нагревательными приборами.
Постановка опыта – Елена Махиненко, текст – к.п.н. Павел Беспалов.
Получение сернистой кислоты
Сернистую кислоту можно получить растворением сернистого газа в воде. Для получения сернистого газа понадобится концентрированная серная кислота и медь: в пробирку с концентрированной серной кислотой поместим кусочек меди и нагреем раствор.
Cu + 2H2SO4 = CuSO4 + SO2↑ + H2O
Направим ток сернистого газа в пробирку с водой. При растворении сернистого газа частично происходит реакция с водой, и образуется слабая сернистая кислота.
SO2 + H2O = H2SO3
Пропуская сернистый газ через воду, мы получили сернистую кислоту. Сернистый газ в огромных количествах выделяется из недр Земли у действующих вулканов. Сернистый газ раздражает слизистые оболочки дыхательных путей, вызывает их воспаление, потерю аппетита, в больших концентрациях ‑ потерю сознания. Поэтому обращаться с сернистым газом нужно, соблюдая все меры предосторожности.
Оборудование: пробирки, газоотводная трубка, штатив, штатив для пробирок, пинцет, спиртовка.
Техника безопасности. Опыт необходимо проводить под тягой. Соблюдать правила обращения с нагревательными приборами. Необходима особая осторожность при работе с концентрированной серной кислотой. Следует соблюдать правила работы с концентрированными кислотами.
Недопустимо вдыхание выделяющегося сернистого газа.
Постановка опыта – Елена Махиненко, текст – к.п.н. Павел Беспалов.
Свойства сернистой кислоты
Раствор сернистой кислоты H2SO3 обладает восстановительными свойствами. Сернистая кислота взаимодействует с раствором йода, обесцвечивая его. При этом образуются йодоводородная и серная кислоты.
H2SO3 + I2 + H2O = H2SO4 + 2НI
Как и все кислоты, сернистая кислота меняет цвет растворов индикаторов. Метиловый оранжевый в растворе кислоты становится красным. В старину дамские соломенные шляпки отбеливали сернистой кислотой. Раствор сернистой кислоты отбеливает ткани из растительного материала, шерсти, шелка.
Оборудование: пробирки, газоотводная трубка, штатив, штатив для пробирок, пинцет, спиртовка.
Техника безопасности. Опыт необходимо проводить под тягой. Соблюдать правила обращения с нагревательными приборами. Недопустимо вдыхание выделяющегося сернистого газа.
Постановка опыта – Елена Махиненко, текст – к.п.н. Павел Беспалов .
http://5terka.com/node/11408
http://www.yoursystemeducation.com/opyty-po-ximii-sera-i-eyo-soedineniya/