Углерод
Углерод
Углерод — неметаллический элемент IV группы периодической таблицы Д.И. Менделеева, является важнейшей частью всех органических веществ в природе.
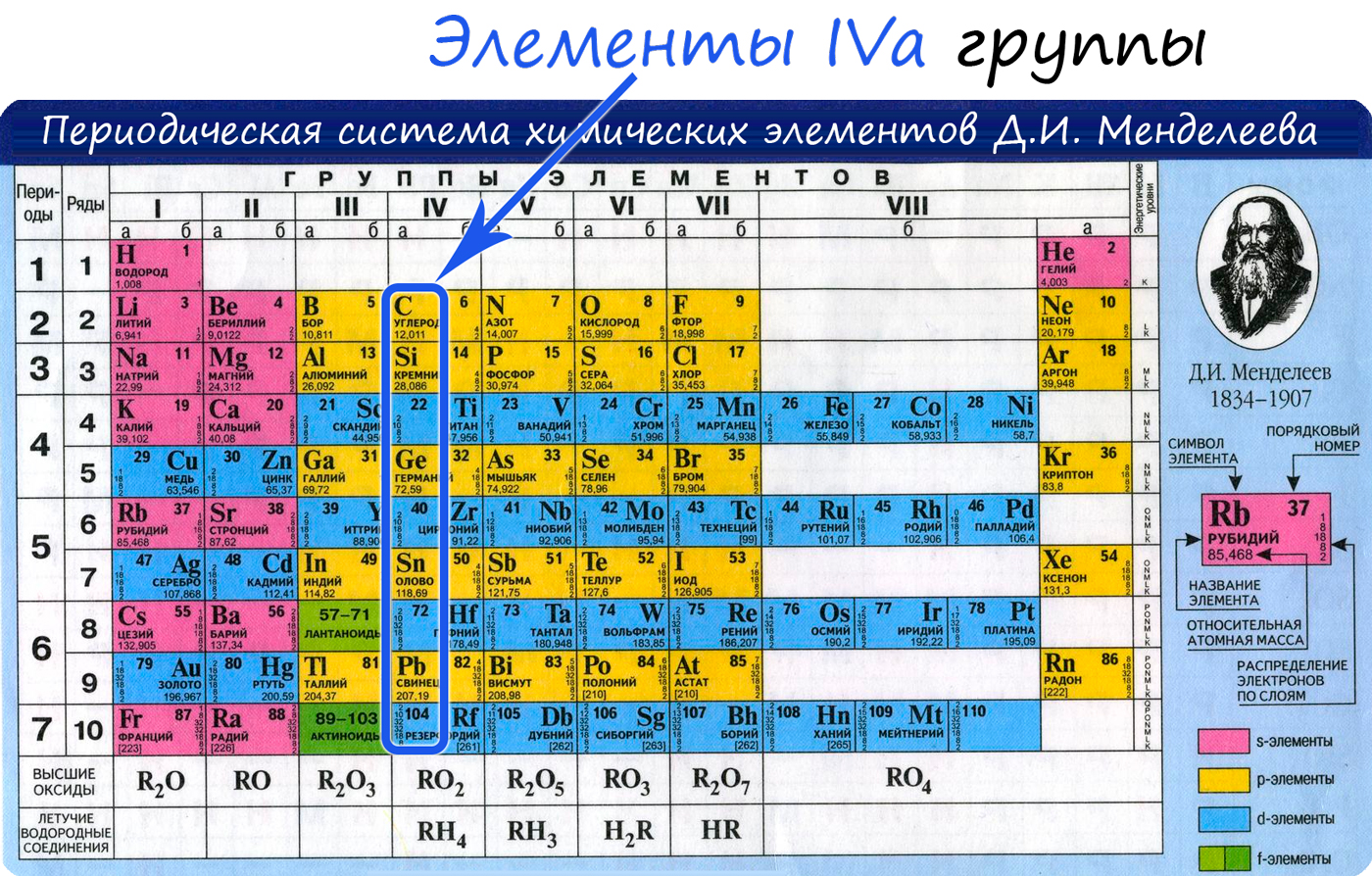
Общая характеристика элементов IVa группы
От C к Pb (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств. Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
Из элементов IVа группы углерод и кремний относятся к неметаллам, германий, олово и свинец — металлы.
Электронные конфигурации у данных элементов схожи, так как они находятся в одной группе (главной подгруппе!), общая формула ns 2 np 2 :
- C — 2s 2 2p 2
- Si — 3s 2 3p 2
- Ge — 4s 2 4p 2
- Sn — 5s 2 5p 2
- Pb — 6s 2 6p 2
Природные соединения
В природе углерод встречается в виде следующих соединений:
- Аллотропных модификаций — графит, алмаз, фуллерен
- MgCO3 — магнезит
- CaCO3 — кальцит (мел, мрамор)
- CaCO3*MgCO3 — доломит
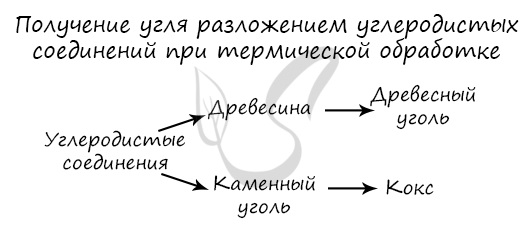
Получение
Углерод получают в ходе пиролиза углеводородов (пиролиз — нагревание без доступа кислорода). Также применяется получение углеродистых соединений: древесины и каменного угля.
Химические свойства
- Реакции с неметаллами
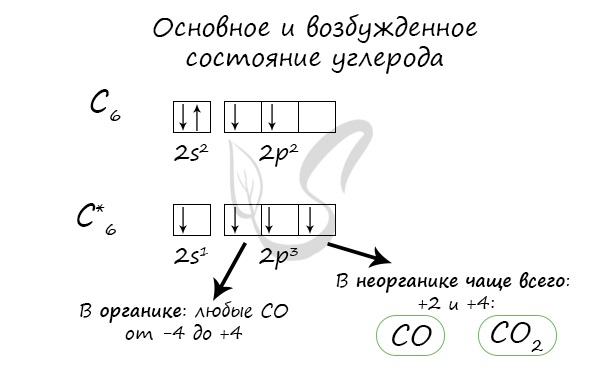
При нагревании углерод реагирует со многими неметаллами: водородом, кислородом, фтором.
2С + O2 → (t) 2CO (угарный газ — продукт неполного окисления углерода, образуется при недостатке кислорода)
С + O2 → (t) CO2 (углекислый газ — продукт полного окисления углерода, образуется при достаточном количестве кислорода)
Реакции с металлами
При нагревании углерод реагирует с металлами, проявляя свои окислительные свойства. Напомню, что металлы могут принимать только положительные степени окисления.
Ca + C → CaC2 (карбид кальция, СО углерода = -1)
Al + C → Al4C3 (карбид алюминий, СО углерода -4)
Очевидно, что степень окисления углерода в соединении с различными металлами может отличаться.
Углерод — хороший восстановитель. С помощью него металлургическая промышленность справляется с задачей получения чистых металлов из их оксидов:
Углерод восстанавливает не только металлы из их оксидов, но и неметаллы подобным образом:
SiO2 + C → (t) Si + CO
Может восстановить и собственный оксид:
Известная реакция взаимодействия угля с водяным паром, называемая также газификацией угля, торфа, сланца — крайне важна в промышленности:
Реакции с кислотами
В реакциях с кислотами углерод проявляет себя как восстановитель:
Оксид углерода II — СO
Оксид углерода II — продукт неполного окисления углерода. Несолеобразующий оксид. Это чрезвычайно опасное вещество часто образуется при пожарах в замкнутых помещениях, при прогревании машины в гараже.
Растворяясь в крови угарный газ (имеющий в 300 раз большее сродство к гемоглобину, чем кислород) легко выигрывает конкуренцию у кислорода и занимает его место в эритроцитах. Отравление угарным газом нередко заканчивается летальным исходом.
В промышленности угарный газ получают восстановлением оксида углерода IV или газификацией угля (t = 1000 °С).
В лаборатории угарный газ получают при разложении муравьиной кислоты в присутствии серной:
Полностью окисляется до углекислого газа в реакции с кислородом, восстанавливает оксиды металлов.
FeO + CO → Fe + CO2
Образование карбонилов — чрезвычайно токсичных веществ.
Оксид углерода IV — CO2
Продукт полного окисления углерода. Относится к кислотным оксидам, соответствует угольной кислоте H2CO3. Бесцветный газ, без запаха.
В промышленности углекислый газ получают при разложении известняка, в ходе производства алкоголя, при спиртовом брожении глюкозы.
В лабораторных условиях используют реакцию мела (мрамора) с соляной кислотой.
Углекислый газ образуется при горении органических веществ:
- Реакция с водой
В результате реакции с водой образуется нестойкая угольная кислота, которая сразу же распадается на воду и углекислый газ.
Реакции с основными оксидами и основаниями
В ходе реакций с основаниями и основными оксидами углекислый газ образует соли угольной кислоты: средние — карбонаты (при избытке основания), кислые — гидрокарбонаты (при избытке кислотного оксида).
2KOH + CO2 → K2CO3 + H2O (соотношение основание — кислотный оксид 2:1)
KOH + CO2 → KHCO3 (соотношение основание — кислотный оксид 1:1)
При нагревании способен окислять металлы до их оксидов.
Zn + CO2 → (t) ZnO + CO
Угольная кислота
Слабая двухосновная кислота, существующая только в растворах, разлагается на воду и углекислый газ.
Определить наличие карбонат-иона можно с помощью кислоты: такая реакция сопровождается «закипанием» — появлением пузырьков бесцветного газа без запаха.
Я не раз встречал описание реакций, связанных с этой кислотой, которое заслуживает нашего внимания. В задании было сказано, что при добавлении к раствору гидроксида кальция углекислого газа осадок появлялся, при дальнейшем пропускании углекислого газа — помутнение исчезало.
Это можно легко объяснить, вспомнив про способность угольной кислоты образовывать кислые соли, которые растворимы.
Чтобы сделать из средней соли (карбоната) — кислую соль (гидрокарбонат) нужно добавить угольную кислоту. Однако написать ее формулу H2CO3 — ошибка. Ее следует записать в виде воды и углекислого газа.
Li2CO3 + CO2 + H2O → LiHCO3 (средняя соль + кислота = кислая соль)
Чтобы вернуть среднюю соль, следует добавить к кислой соли щелочь.
Нагревание солей угольной кислоты
При нагревании карбонаты распадаются на соответствующий оксид металла и углекислый газ, гидрокарбонаты — на карбонат металла, углекислый газ и воду.
© Беллевич Юрий Сергеевич 2018-2022
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Углерод
В XVII – XVIII вв., в период расцвета теории флогистона, считали , что уголь полностью состоит из этого таинственного вещества: ведь при горении угля почти не образуется твердого остатка. И только А.Л.Лавуазье, изучая горение угля, пришел к выводу, что уголь – всего лишь простое вещество. Лавуазье назвал новый элемент Carboneum вместо старого латинского названия carbone pur – «чистый уголь», которым долгое время пользовались химики.
Алмаз. При слове «алмаз» сразу же вспоминаются окутанные завесой тайны истории, повествующие о поисках сокровищ. Когда-то люди, охотившиеся за алмазами, и не подозревали, что предметом их страсти является кристаллический углерод – тот самый углерод, который образует сажу, копоть и уголь. Впервые это доказал Лавуазье. Он поставил опыт по сжиганию алмаза, используя собранную специально для этого зажигательную машину. Оказалось, алмаз сгорает на воздухе при температуре около 700 о С, не оставляя твердого остатка, как и обычный древесный уголь.

В структуре алмаза каждый атом углерода имеет четырех соседей, которые расположены от него на равных расстояниях в вершинах тетраэдра. Весь кристалл представляет собой единый трёхмерный каркас. С этим связаны многие свойства алмаза, в частности его самая высокая среди минералов твёрдость. Она-то и дала камню имя, которое происходит от греч. «адамас» — «твердый, непреклонный, несокрушимый».
Кристаллы алмаза, особенно огранённые (бриллианты), очень сильно преломляют свет. Этим и обусловлена знаменитая «игра бриллиантов».
В России ювелирные алмазы вошли в моду в середине XVIII в. Ими украшали не только царские диадемы и скипетры, но также брелки, застежки, трости, табакерки и даже обувь! Мелкие алмазы используются для резки стекла и металлов, служат наконечниками свёрл, резцов. Алмазный порошок издревле применяют для полировки и огранки драгоценных камней.
Графит. В древности графит считали одним из минералов свинца, возможно из-за того, что, подобно свинцу, он оставляет на бумаге след (поэтому из графита делают грифели). В XVIII в. К. В. Шееле доказал, что графит представляет собой минеральный уголь». Родственные отношения между алмазом и графитом были подробно изучены коллегой Лавуазье французским химиком Луи Бернаром Гитоном де Морво: при осторожном нагревании алмаза без доступа воздуха он получил порошок графита.

Графит – мягкое вещество серого цвета. Атомы углерода связаны в нем в плоские слои, состоящие из соединенных рёбрами шестиугольников, наподобие пчелиных сот. Каждый атом в таком слое имеет трёх соседей. Для образования трёх ковалентных связей атом предоставляет три электрона, а четвертый электрон, образуя π-связи, делокализован по всему кристаллу. Этим объясняются такие свойства графита, как металлический блеск и электропроводность.
Поскольку электронные облака атомов из соседних плоских слоев перекрываются, между слоями возникают слабые связи, которые рвутся даже при незначительной нагрузке. Для того чтобы убедиться, достаточно провести карандашом по листу бумаги: на листе останется след из чешуек графита.
Графит широко применяется в технике. Графитовый порошок используется для изготовления минеральных красок, а также в качестве смазочного материала – между отдельными слоями графита взаимодействие настолько слабое, что возникает скольжение. Графитовые стержни служат электродами во многих электрохимических процессах; из смеси графита с глиной изготовляют тигли для плавки металлов. Блоки из особо чистого графита являются основным материалом для создания атомных реакторов. В первом отечественном реакторе, например, было использовано 450 т графита.
В отсутствии кислорода графит и алмаз выдерживают нагревание до высоких температур: эти вещества переходят в газовую фазу в виде молекул Сn лишь при 3000 о С. Поэтому графит используют как теплозащитный материал для головных частей ракет.
Химические свойства углерода
При обычной температуре углерод малоактивен. При нагревании он реагирует со многими простыми и сложными веществами.
Углерод может быть как окислителем, так и восстановителем, поэтому в соединениях может проявлять положительную и отрицательную степень окисления.
- Углерод как восстановитель
Как и другие неметаллы, углерод проявляет свойства при взаимодействии с кислородом и другими более электроотрицательными элементами.
а) углерод горит на воздухе с выделением большого количества тепла. При этом образуется СО2:
При недостатке кислорода образуется СО:
б) раскаленный углерод реагирует с парами серы, легко соединяется с хлором и другими галогенами:
в) так как для углерода в отличие от других неметаллов весьма характерны восстановительные свойства, он может восстанавливать оксиды металлов и неметаллов:
2C + PbO2 = Pb + 2CO
Это свойство углерода широко используется в металлургии.
г) при пропускании через раскаленный уголь водяного пара получается смесь оксида углерода (II) с водородом, или водяной газ:
- Углерод как окислитель
Углерод проявляет окислительные свойства при взаимодействии с металлами и водородом.
а) углерод взаимодействует с металлами, образуя карбиды металлов:
В промышленности карбид кальция получают при взаимодействии углерода с негашеной известью СаО, которую получают из известняка СаСО3:
CaO + 3C = CaC2 + CO↑
б) углерод реагирует с водородом, при этом образуется метан СН4:
Кислородные соединения углерода
Оксид углерода (II) СО, или угарный газ. Он не имеет запаха и цвета, плохо растворим в воде, токсичен.
В лаборатории его получают разложением муравьиной кислоты при нагревании в присутствии серной кислоты или фосфорного ангидрида:
Углерод в угарном газе имеет степень окисления +2, поэтому для него характерны реакции присоединения, в которых он является восстановителем.
Угарный газ горит с образованием углекислого газа и выделением тепла:
Он реагирует с хлором на свету в присутствии катализатора – угля. При этом образуется фосген:
Фосген – ядовитый газ, применялся как отравляющее средство в первую мировую войну.
Восстановительные свойства угарного газа используются в металлургии для получения металлов из руд:
CO + FeO = CO2 + Fe
Оксид углерода (IV), или углекислый газ СО2.
Он бесцветен, не имеет запаха, тяжелее воздуха, плохо растворяется в воде. Он образуется при:
а) горении углерода в избытке кислорода:
б) разложении карбонатов и гидрокарбонатов при нагревании:
Оксид углерода (IV) не поддерживает горения. Только некоторые активные металлы горят в нем, так как отнимают кислород:
2Mg + CO2 = 2MgO + C
Оксид углерода (IV) – кислотный оксид. Он реагирует с основаниями, основными оксидами, с водой. При взаимодействии с водой образуется угольная кислота:

Угольная кислота. Как двухосновная кислота она диссоциирует по двум ступеням и поэтому образует два ряда солей – нормальные и кислые соли (карбонаты и гидрокарбонаты). Примеры солей: гидрокарбонаты – NaHCO3, Mg(HCO3)2; карбонаты — Na2CO3, CaCO3.
Карбонаты щелочных металлов и аммония хорошо растворимы в воде. Карбонаты щелочноземельных металлов в воде практически нерастворимы. Карбонаты алюминия, хрома, железа не могут существовать в водных растворах, так как подвергаются полному гидролизу, в результате которого выпадает осадок соответствующего гидроксида и выделяется углекислый газ.
Все карбонаты, кроме карбонатов щелочных металлов, при нагревании разлагаются на оксид металла и углекислый газ:
Качественной реакцией на карбонаты и гидрокарбонаты является их взаимодействие с растворами кислот, при котором выделяется углекислый газ:
При пропускании СО2 через известковую воду Са(ОН)2 выпадает осадок СаСО3 (раствор мутнеет):
Са(ОН)2 + СО2 = СаСО3↓ + Н2О (качественная реакция на СО2)
Скачать:
Скачать бесплатно реферат на тему: «Углерод» Углерод.doc (246 Загрузок)
Скачать бесплатно реферат на тему: «Углерод в природе» Углерод-в-природе.doc (269 Загрузок)
Скачать бесплатно реферат на тему: «Подгруппа углерода» Подгруппа-углерода.-Углерод.docx (214 Загрузок)
Скачать бесплатно реферат на тему: «Углеродные нанотрубки» Углеродные-нанотрубки.doc (226 Загрузок)
Скачать бесплатно реферат на тему: «Алмаз-минерал» Алмаз-минерал.docx (243 Загрузки)
Скачать бесплатно реферат на тему: «Алмаз-графит» Алмаз-графит.docx (240 Загрузок)
Скачать бесплатно реферат на тему: «Уголь» Уголь.docx (224 Загрузки)
Скачать рефераты по другим темам можно здесь
*(на изображении записи фотография бриллианта)
Похожее
Один ответ на “Углерод”
Все интересно написано , в статье об углероде не много не понятно для чего там просто написан Na2CO3
Добавить комментарий Отменить ответ
Репетитор по химии. Занятия проходят онлайн по Скайпу. По всем вопросам пишите в Ватсапп: +7 928 285 70 42
Свойства углерода, его взаимодействие с кислородом
Механизмы реакций с O₂
Углерод — химический элемент, формирующий множество соединений органической и неорганической природы. Это главный биогенный элемент Земли, который присутствует в составе всех населяющих планету живых существ. Этот элемент может существовать в кардинально отличающихся по своим параметрам формах, состоящих исключительно из атомов углерода.
История открытия углерода и основные характеристики элемента
Углерод известен людям еще с древности, ведь каменный уголь — один из основных минералов в природе. Кроме угля, люди использовали графит и алмазы.
В 1725 году коммерческое значение приобрели драгоценные камни (алмазы), а в 1970 году люди освоили технологию получения алмазов искусственным путем. В 1779 году ученые приступают к исследованию химических свойств углерода, используя работы химика Карла Шееле. Так, им удалось сделать ряд важнейших открытий, которые послужили основой для выяснения всех уникальных особенностей химического элемента углерод.
В периодической системе Менделеева углерод располагается в 4 группе, главной подгруппе. Порядковый номер элемента — 6, атомный вес — 12,011. Элемент обозначается знаком «С» (от латинского carboneum). Углерод существует в нескольких формах, по этой причине его формула бывает различна и зависит от конкретной модификации. Для написания уравнений реакций используется единственная молекулярная формула углерода, обозначающая вещество в чистом виде — С (без индексации).
Химическая активность углерода
Благодаря устойчивой конфигурации, молекулярный углерод проявляет низкую химическую активность. Вступить в реакцию углерод может, если сообщить атому дополнительную энергию и заставить распариться электроны внешнего уровня. В этот момент валентность элемента становится равной 4. По этой причине в соединениях углерод имеет степень окисления «+2», «+4», «-4».
Все реакции углерода с простыми веществами (металлами и неметаллами) протекают под воздействием высоких температур. Данный элемент может быть и окислителем, и восстановителем. Восстанавливающие свойства углерода выражены сильно, поэтому элемент используется в металлургической промышленности и других отраслях.
Способность углерода вступать в химические реакции зависит от таких факторов: температуры реакции, аллотропной модификации и дисперсности. Углерод взаимодействует с такими веществами: металлами (железом, алюминием, кальцием и другими), неметаллами (кислородом и водородом), оксидами металлов и их солями.
С щелочами и кислотами углерод в реакцию не вступает, очень редко он взаимодействует с галогенами. Одно из основных свойств углерода — способность элемента образовывать длинные цепи между собой. Цепи замыкаются в цикл, формируют разветвления — так образуются миллионы органических соединений. Их основой выступают два элемента — углерод и водород. В состав соединений могут входить другие атомы: азот, кислород, сера, фосфор, галогены, металлы.
Реакция углерода с кислородом
Взаимодействие кислорода и углерода нашло практическое применение в металлургической промышленности.
Генри Бессемер, английский инженер изобретатель, искал такой способ производства стали, который позволил бы исключить дорогостоящую стадию получения сварочного железа. Чтобы удалить из чугуна избыточный углерод, инженер пропускал струю воздуха через расплавленный металл. Металл при этом не затвердевал и не охлаждался. Даже наоборот: в результате реакции углерода с кислородом выделялось тепло, и температура расплава повышалась. Прекращая подачу воздуха в соответствующий момент, Бессемер получил сталь.
В механизме этой реакции основным вопросом являются первичные продукты реакции углерода с кислородом. Выдвигались теории, объясняющие, какие продукты реакции горения углерода являются первичными. Правильное экспериментальное решение вопроса о первичных продуктах реакции горения затрудняется процессами окисления окиси углерода в газовой фазе и восстановления двуокиси углерода. Для исключения влияния вторичных реакций применялись разные методы исследования: низкое давление, высокие скорости газа, ингибиторы и низкие температуры.
Сложная реакция углерода с кислородом, включающая последовательно-параллельные простые реакции, может быть описана двумя уравнениями скоростей, составленными по отношению к двум ключевым веществам. Из этого следует, что одна из констант реакций горения углерода (реакция С → СO₂), должна быть предварительно экспериментально определена.
В этом случае по двум кинетическим уравнениям скоростей расходования или образования ключевых веществ, по составу продуктов реакций легко вычисляются неизвестные константы остальных двух реакций. Здесь вы узнаете об основных свойствах углерода и областях его применения.
Значительная часть мировой потребности в энергии удовлетворяется реакциями углерода и углеродсодержащих материалов с газами: с кислородом, двуокисью углерода, водяным паром и водородом. Экзотермическая реакция углерода с кислородом была и есть основным источником энергии. Эндотермическая реакция углерода с водяным паром дает окись углерода и водород, которые употребляются как газовое топливо или как синтетический газ, который может быть каталитически превращен в углеводородные топлива или в другие органические соединения. Так как двуокись углерода — это первичный продукт реакции углерода с кислородом и вторичный продукт реакции углерода с водяным паром в реакции водяного газа, то вторичная реакция двуокиси углерода с углеродом в слое топлива тесно связана с основными реакциями углерода. В настоящее время реакция углерода с водородом с образованием метана не имеет промышленного значения, но ей принадлежит будущее.
http://al-himik.ru/uglerod/
http://melscience.com/RU-ru/articles/svojstva-ugleroda-ego-vzaimodejstvie-s-kislorodom/