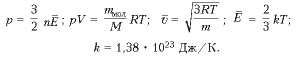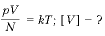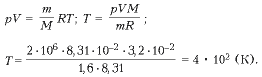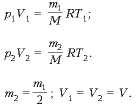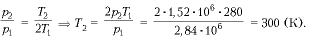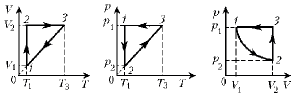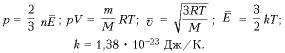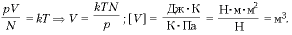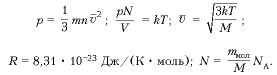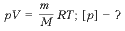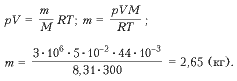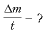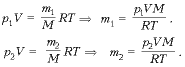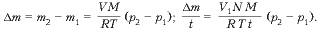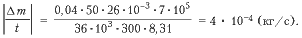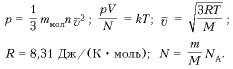Решение задач по теме «Уравнение состояния идеального газа»
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
ТЕМА: Решение задач по теме «Уравнение состояния идеального газа»
Учебная: Диагностика степени усвоения знаний по теме «Уравнение состояния идеального газа» и формирование практических умений по их применению .
Развивающая: Развивать интерес к физике, развивать практические умения учащихся при решении задач.
Воспитательная : воспитывать сознательное отношение к учебе и заинтересованность в изучении физики.
Тип урока: урок комплексного применения знаний
I. Организационно — мотивационный этап
1) Организация начала урока
2) Проверка домашнего задания
II. Организационно — мотивационный этап
3) Актуализация имеющихся знаний.
4) Закрепление знаний и способов действия
6) Первоначальная проверка понимания
III. Рефлексийна — заключальны этап
7) Подведение итогов занятия. Выставление оценок
8) Домашнее задание
I. Организационно — мотивационный этап
1) Организация начала урока
Приветствие учащихся и учителя. Проверить подготовленность учащихся к уроку, правильную организацию рабочего места. Отметить отсутствующих в журнале.
2) Проверка домашнего задания
Фронтальная проверка выполнения домашнего задания. Обсуждения результатов выполнения
II. Операционно — познавательный этап.
3) Актуализация имеющихся знаний.
А) Фронтальный опрос
— Перечислите макроскопические параметры состояния идеального газа ( Р,V,Т)
— Какое уравнение называют уравнением состояния? (Уравнение, выражающее связь между макроскопическими параметрами состояния вещества)
-В чем заключается основная задача МКТ? ( Установление связи между макроскопическими параметрами, т.е. нахождение уравнения состояния того или иного тела)
-Сформулировать и доказать закон Дальтона (Давление смеси химически не взаимодействующих идеальных газов равно сумме парциальных давлений этих газов, p=p1 +…рn )
-Записать уравнение Клапейрона. При каких условиях оно справедливо? (PV\T=P0V0\\T0, m=const, M=const)
— Записать уравнение Менделеева — Клапейрона.
4) Закрепление знаний и способов действия
Задачи решаются на доске:
1. Определить массу водорода, находящегося в баллоне вместимостью 20 л при давлении 830 кПа, если температура газа равна 17 °С.
Дано: V = 20 л, р = 830 кПа, t = 17 ° C , М = 2·10-3 кг/моль, R = 8,31 Дж/(моль·К).
Решение 
Ответ: m = 1,38·10 -2 кг.
2 . Газ при давлении 0,2 МПа и температуре 15 0 С имеет объем 5 л. Чему будет равен объем этой массы газа при нормальных условиях?
3. В баллоне находится газ под давлением 40 Па и при температуре 27 °С. Когда из баллона выпустили 3/5 газа, содержавшегося в нем, его температура понизилась до -33 °С. Определить давление газа, оставшегося в сосуде.
Дано: V — const , р1 = 40 МПа, t 1 = 27 °С, t 2 = -33 °С, m 2 = 2/5 m 1
Решение
Ответ: р2 = 12,8 Па.
4. При уменьшении объема газа в 2 раза давление увеличилось на 120 кПа, а абсолютная температура возросла на 10 %. Каким было первоначальное давление?
6) Первоначальная проверка понимания
Задачи решаются самостоятельно учениками
1. Определите температуру кислорода массой 64 г, находящегося в сосуде объёмом 1 л при давлении 5 • 10 6 Па. Молярная масса кислорода М = 0,032 кг/моль.
Р е ш е н и е. Согласно уравнению Менделеева—Клапейрона 

2. Найти плотность водорода при температуре 15 0 С и давлении 9,8·10 4 Па. (0,085 кг/м 3 )
3. В баллоне находится газ при температуре 15 0 С. Во сколько раз уменьшится давление газа, если 40 % его выйдет из баллона, а температура при этом понизится на 8 0 С?

III. Рефлексийно – заключительный этап
7) Подведение итогов занятия. Выставление оценок
8) Домашнее задание упр.3(5-7). Подготовится к проверочной работе
9) Рефлексия: Ребята высказываются одним предложением, выбирая начало фразы из рефлексивного экрана на доске: Сегодня я узнал… Было интересно… Было трудно… Я понял, что…
Решение задач по теме «Уравнение состояния идеального газа»
1. Определить массу водорода, находящегося в баллоне вместимостью 20 л при давлении 830 кПа, если температура газа равна 17 °С.
2 . Газ при давлении 0,2 МПа и температуре 15 0 С имеет объем 5 л. Чему будет равен объем этой массы газа при нормальных условиях?
3. В баллоне находится газ под давлением 40 Па и при температуре 27 °С. Когда из баллона выпустили 3/5 газа, содержавшегося в нем, его температура понизилась до -33 °С. Определить давление газа, оставшегося в сосуде.
4. При уменьшении объема газа в 2 раза давление увеличилось на 120 кПа, а абсолютная температура возросла на 10 %. Каким было первоначальное давление?
1. Определите температуру кислорода массой 64 г, находящегося в сосуде объёмом 1 л при давлении 5 • 10 6 Па. Молярная масса кислорода М = 0,032 кг/моль.
2. Найти плотность водорода при температуре 15 0 С и давлении 9,8·10 4 Па. (0,085 кг/м 3 )
3. В баллоне находится газ при температуре 15 0 С. Во сколько раз уменьшится давление газа, если 40 % его выйдет из баллона, а температура при этом понизится на 8 0 С?
Решение задач по теме «Уравнение состояния идеального газа»
1. Определить массу водорода, находящегося в баллоне вместимостью 20 л при давлении 830 кПа, если температура газа равна 17 °С.
2 . Газ при давлении 0,2 МПа и температуре 15 0 С имеет объем 5 л. Чему будет равен объем этой массы газа при нормальных условиях?
3. В баллоне находится газ под давлением 40 Па и при температуре 27 °С. Когда из баллона выпустили 3/5 газа, содержавшегося в нем, его температура понизилась до -33 °С. Определить давление газа, оставшегося в сосуде.
4. При уменьшении объема газа в 2 раза давление увеличилось на 120 кПа, а абсолютная температура возросла на 10 %. Каким было первоначальное давление?
1. Определите температуру кислорода массой 64 г, находящегося в сосуде объёмом 1 л при давлении 5 • 10 6 Па. Молярная масса кислорода М = 0,032 кг/моль.
2. Найти плотность водорода при температуре 15 0 С и давлении 9,8·10 4 Па. (0,085 кг/м 3 )
3. В баллоне находится газ при температуре 15 0 С. Во сколько раз уменьшится давление газа, если 40 % его выйдет из баллона, а температура при этом понизится на 8 0 С?
Уравнение состояния идеального газа
Решение задач. 10-й класс. Базовый курс
Предлагаемые два варианта заданий можно использовать при проведении урока с элементами коллективного и индивидуального соревнований, а также для зачетов. На уроке я делю класс на две команды. Вначале каждый участник пытается решить посильное самостоятельно, затем под руководством капитанов – в группе. Разрешается совещаться и обращаться с вопросами ко мне. В конце урока за индивидуальную работу ставится оценка (зачет).
1. Баллон емкостью 0,0831 м 3 содержит 1,6 кг кислорода. При какой температуре баллон может разорваться, если он выдерживает давление 2 • 10 6 Па?
2. Баллон, наполненный газом под давлением 2,84 МПа, находился на складе при температуре 7 °С. После того как половину газа израсходовали, баллон внесли в помещение. Какова температура в помещении, если давление газа в баллоне через некоторое время стало 1,52 МПа?
4. Определите молярную массу углекислого газа.
5. Прибор для измерения давления газа
6. Почему нагретая медицинская банка «присасывается» к телу человека?
7. Найдите ошибки:
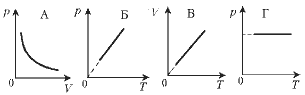
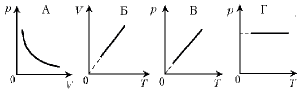
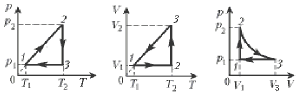
8. Какой график отражает закон Шарля?
9. Выразите величину V и проверьте правильность полученных единиц ее измерения:
V = 0,0831 м 3 ,
m = 1,6 кг,
M(O2) = 32 • 10 –3 кг/моль,
p = 2 • 10 6 Па.
_______________
T – ?
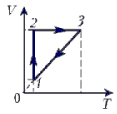
3. 1–2 – изотермический (расширение); 2–3 – изохорный (нагревание); 3–1 – изобарный (сжатие).
4. M(CO2) = (12 + 32) • 10 –3 = 44 • 10 –3 (кг/моль).
6. При нагревании воздуха в банке часть его выходит, так что при охлаждении давление в банке становится меньше атмосферного.
1. Определите массу углекислого газа, находящегося в баллоне емкостью 5 • 10 –2 м 3 при температуре 300 К. Давление газа 3 • 10 6 Па.
2. В сварочном цехе стоит 50 баллонов ацетилена (С2Н2) емкостью 40 л каждый. Все баллоны включены в общую магистраль. После 10 ч непрерывной работы давление во всех баллонах упало с 1,2 • 10 6 до 5 • 10 5 Па. Найдите средний расход ацетилена за секунду, если температура в цехе оставалась неизменной и равнялась 27 °С.
4. Определите молярную массу серной кислоты (H2SO4).
5. Прибор для измерения параметра состояния термодинамической системы.
6. Почему у глубоководных рыб плавательный пузырь выходит через рот наружу, если их извлечь из воды?
7. Найдите ошибки:
8. Какой график отражает закон Гей-Люссака?
9. Выразите величину р и проверьте правильность получаемых единиц ее измерения:
V = 5 • 10 –2 м 3 ,
T = 300 К,
p = 3 • 10 6 Па,
M(СО2) = 44 • 10 –3 кг/моль.
_________________
m – ?
M(C2H2) = 26 • 10 –3 кг/моль,
N = 50,
V1 = 40 л, СИ: 0,04 м 3
t = 10 ч, СИ: 36 • 10 3 с
p1 = 1,2 • 10 6 Па,
p2 = 5 • 10 5 Па,
t = 27 °С. СИ: T = 300 К
_____________


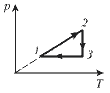
3. 1–2 – изохорный (нагревание); 2–3 – изотермический (расширение); 3–1 – изобарный (сжатие).
6. Давление на большой глубине намного превышает атмосферное, поэтому плавательный пузырь при подъеме рыбы значительно увеличивается в объеме.
7.
Задача по теме уравнение состояния идеального газа
Репетитор
по физикеРепетитор
по алгебре\( P \) — Давление газа (Паскали)
\( \nu \) — Количество вещества
\( R \) — Универсальная газовая посиоянная
\( T \) — Температура в Кельвинах
В баллоне находится газ под давлением \(P= 8,31 \cdot 10^6 \; Па \), температура газа \(T=300 К \).
Количество вещества газа \( \nu=100 Моль \).
Найти объем баллона
Универсальная газовая постоянная \( R=8,31 \frac<Дж> <Моль \cdot K>\)
Дать ответ в литрах.
Показать ответ Показать решение ВидеорешениеЗапишем уравнение Менделеева-Клапейрона :
источники:http://fiz.1sept.ru/2000/no44_1.htm
http://kornev-school.ru/f10_Mendeleev-Clapeyron_equation.html