Реакции ионного обмена. Карточки-задания и алгоритм составления ионных уравнений
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
Карточки-задания на составление ионных уравнений реакций
Закончите уравнения реакций. Составьте полное и сокращенное ионное уравнения этих реакций.
При выполнении задания можно воспользоваться страничкой приложения 1 .
Закончите уравнения реакций. Составьте полное и сокращенное ионное уравнения этих реакций.
При выполнении задания можно воспользоваться страничкой приложения 1.
Закончите уравнения реакций. Составьте полное и сокращенное ионное уравнения этих реакций.
При выполнении задания можно воспользоваться страничкой приложения 1.
Реакции ионного обмена. Условия протекания.
Реакции ионного обмена – это реакции между ионами, образовавшимися в результате диссоциации электролитов.
Реакции ионного обмена протекают до конца в следующих случаях:
Если образуется осадок (нерастворимое в воде вещество):
NaCl + AgNO 3 = AgCl + NaNO 3
Если образуется газообразное вещество :
2 Na + + C O 3 2- + 2Н + + 2С l — = 2 Na + + 2 Cl — + Н 2 O + СО2
Если в растворах нет таких ионов, которые могут связываться между собой с образованием осадка, газа, или воды Н 2 O , то реакция является обратимой.
Составление ионных уравнений.
Простые вещества, оксиды, нерастворимые кислоты, основания и соли не диссоциируют.
Для реакции берут растворы веществ, поэтому даже малорастворимые вещества находятся в растворах в виде ионов.
Если малорастворимое вещество образуется в результате реакции, то при записи ионного уравнения его считают нерастворимым.
Алгоритм составления ионного уравнения реакции.
Записать молекулярное уравнение реакции. Расставить коэффициенты.
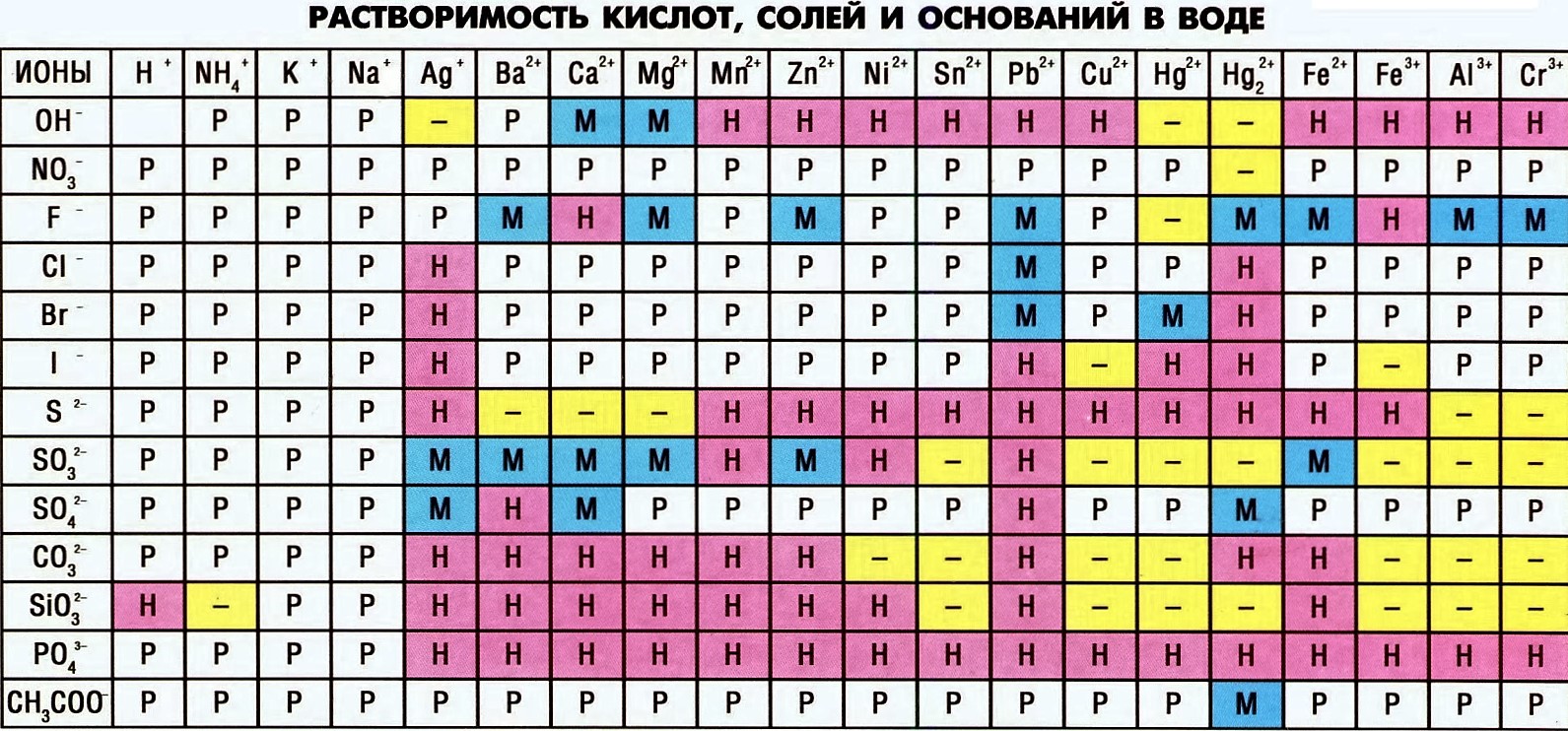
С помощью таблицы растворимости определить растворимость каждого вещества
Составить полное ионное уравнение, записывая растворимые в воде вещества в виде ионов, а нерастворимые вещества, газообразные вещества и воду в виде молекул.
Составить сокращённое ионное уравнение, найдя одинаковые ионы в уравнении слева и справа и сократив их.
3 Na ОН + FeCl 3 = Fe (ОН) 3 + 3 NaCl
3 Na ОН + FeCl 3 = Fe (ОН) 3 + 3 NaCl
3 Na + +3ОН — + Fe 3+ +3 Cl — = Fe (ОН) 3 + 3 Na + +3 Cl —
3ОН — + Fe 3+ = Fe (ОН) 3
Курс повышения квалификации
Дистанционное обучение как современный формат преподавания
- Сейчас обучается 939 человек из 80 регионов
Курс повышения квалификации
Инструменты онлайн-обучения на примере программ Zoom, Skype, Microsoft Teams, Bandicam
- Курс добавлен 31.01.2022
- Сейчас обучается 23 человека из 14 регионов
Курс повышения квалификации
Педагогическая деятельность в контексте профессионального стандарта педагога и ФГОС
- Сейчас обучается 40 человек из 24 регионов
Ищем педагогов в команду «Инфоурок»
Дистанционные курсы для педагогов
«Взбодрись! Нейрогимнастика для успешной учёбы и комфортной жизни»
Свидетельство и скидка на обучение каждому участнику
Найдите материал к любому уроку, указав свой предмет (категорию), класс, учебник и тему:
5 587 999 материалов в базе
Самые массовые международные дистанционные
Школьные Инфоконкурсы 2022
33 конкурса для учеников 1–11 классов и дошкольников от проекта «Инфоурок»
«Психологические методы развития навыков эффективного общения и чтения на английском языке у младших школьников»
Свидетельство и скидка на обучение каждому участнику
Другие материалы
- 28.08.2016
- 1034
- 2
- 28.08.2016
- 2367
- 22
- 27.08.2016
- 2361
- 14
- 27.08.2016
- 645
- 0
- 26.08.2016
- 455
- 0
- 26.08.2016
- 563
- 4
- 26.08.2016
- 1074
- 4
Вам будут интересны эти курсы:
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
Добавить в избранное
- 28.08.2016 24321
- DOCX 19.9 кбайт
- 691 скачивание
- Рейтинг: 4 из 5
- Оцените материал:
Настоящий материал опубликован пользователем Гуторова Наталья Борисовна. Инфоурок является информационным посредником и предоставляет пользователям возможность размещать на сайте методические материалы. Всю ответственность за опубликованные материалы, содержащиеся в них сведения, а также за соблюдение авторских прав несут пользователи, загрузившие материал на сайт
Если Вы считаете, что материал нарушает авторские права либо по каким-то другим причинам должен быть удален с сайта, Вы можете оставить жалобу на материал.
Автор материала
- На сайте: 5 лет и 5 месяцев
- Подписчики: 0
- Всего просмотров: 39210
- Всего материалов: 11
Московский институт профессиональной
переподготовки и повышения
квалификации педагогов
Дистанционные курсы
для педагогов
663 курса от 690 рублей
Выбрать курс со скидкой
Выдаём документы
установленного образца!
Учителя о ЕГЭ: секреты успешной подготовки
Время чтения: 11 минут
В Швеции запретят использовать мобильные телефоны на уроках
Время чтения: 1 минута
Каждый второй ребенок в школе подвергался психической агрессии
Время чтения: 3 минуты
В России действуют более 3,5 тысячи студенческих отрядов
Время чтения: 2 минуты
Приемная кампания в вузах начнется 20 июня
Время чтения: 1 минута
Инфоурок стал резидентом Сколково
Время чтения: 2 минуты
В ростовских школах рассматривают гибридный формат обучения с учетом эвакуированных
Время чтения: 1 минута
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.
Только 23 февраля!
Получите новую
специальность
по низкой цене
Цена от 1220 740 руб. Промокод на скидку Промокод скопирован в буфер обмена ПП2302 Выбрать курс Все курсы профессиональной переподготовки
ЗАДАНИЯ ПО ТЕМЕ «РЕАКЦИИ ИОННОГО ОБМЕНА»
Определите, может ли осуществляться взаимодействие между растворами следующих веществ: гидроксид калия и хлорид аммония., записать реакции в молекулярном, полном, кратком ионном виде:
— Составляем химические формулы веществ по их названиям, используя валентности и записываем РИО в молекулярном виде (проверяем растворимость веществ по ТР):
KOH + NH 4 Cl = KCl + NH 4 OH
так как NH 4 OH неустойчивое вещество и разлагается на воду и газ NH 3 уравнение РИО примет окончательный вид
KOH (p) + NH 4 Cl (p) = KCl (p) + NH 3 ↑+ H 2 O
-Cоставляем полное ионное уравнение РИО, используя ТР (не забывайте в правом верхнем углу записывать заряд иона):
K + + OH — + NH 4 + + Cl — = K + + Cl — + NH 3 ↑+ H 2 O
— Cоставляем краткое ионное уравнение РИО, вычёркивая одинаковые ионы до и после реакции:
OH — + NH 4 + = NH 3 ↑+ H 2 O
Взаимодействие между растворами следующих веществ может осуществляться, так как продуктами данной РИО являются газ (NH 3 ↑) и малодиссоциирующее вещество вода (H 2 O).
Подберите вещества, взаимодействие между которыми в водных растворах выражается следующими сокращёнными уравнениями. Составьте соответствующие молекулярное и полное ионное уравнения.
— Используя ТР подбираем реагенты — растворимые в воде вещества, содержащие ионы 2H + и CO 3 2- .
Например, кислота — H 2 SO 4 (p) и соль -K 2 CO 3 (p).
— Составляем молекулярное уравнение РИО:
так как угольная кислота – неустойчивое вещество, она разлагается на углекислый газ CO 2 ↑ и воду H 2 O:
H 2 SO 4 (p) +K 2 CO 3 (p) ->K 2 SO 4 (p) + CO 2 ↑ + H 2 O
— Составляем полное ионное уравнение РИО:
2H + + SO 4 2- + 2 K + + CO 3 2- -> 2 K + + SO 4 2- + CO 2 ↑ + H 2 O
-Составляем краткое ионное уравнение РИО:
2H + + CO 3 2- = CO 2 ↑ + H 2 O
— Делаем вывод:
В конечном итоге мы получили искомое сокращённое ионное уравнение, следовательно, задание выполнено верно.
ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОЙ РАБОТЫ
Задание №1
Закончите уравнения реакций в молекулярном, полном и кратком ионном виде:
При выполнении задания используйте таблицу растворимости веществ в воде. Помните об исключениях!
Задание №2
Посмотрите следующий эксперимент
Составьте уравнение реакции ионного обмена в молекулярном, полном и кратком ионном виде для наблюдаемых химических процессов.
Задание №3
Закончите уравнения реакций в молекулярном, полном и кратком ионном виде:
При выполнении задания используйте таблицу растворимости веществ в воде. Помните об исключениях!
Разбор и решение задания №8 ОГЭ по химии
Реакции ионного обмена
Перейдем к рассмотрению реакций ионного обмена в задании №8 ОГЭ по химии, или А8. Тематика задания сформулирована следующим образом:
- реакции ионного обмена
- условия их осуществления
Теория к заданию №8 ОГЭ по химии
Итак, начнем с определений:
Реакция ионного обмена — одна из видов химических реакций, продуктами которой являются вода, газ или осадок.
Иначе говоря, вещества обмениваются ионами только тогда, когда образуется либо газ, покидающий реакционную смесь, либо малорастворимое вещество — осадок или вода. Более профессиональным языком можно сказать, что движущей силой реакции ионного обмена является образование продукта иного агрегатного или фазового состояния в сравнении с реагентами.
На практике чаще всего мы сталкиваемся с реакциями в растворах, в результате которых образуется осадок, либо газ, либо вода. Чаще всего это реакции обмена.
Пример — реакция карбоната натрия и серной кислоты с выделением углекислого газа:
В сокращенном ионном виде:
Для успешного решения задач нам необходимо запомнить следующие правила:
- используем таблицу растворимости: если видим, что продукт (то, что слева в уравнении) нерастворим, то реакция идет.
- если видим в левой части газ (CO2, H2S, SO2 — типичные для ионного обмена), реакция идет.
- если видим воду (H2O), реакция идет.
Разбор типовых вариантов задания №8 ОГЭ по химии
Первый вариант задания
Газ выделяется при взаимодействии
Рассмотрим каждый случай.
MgCl2 + Ba(NO3)2 = Mg(NO3)2 + BaCl2
Смотрим в таблицу растворимости: нитрат магния растворим (кстати, как и все нитраты), хлорид бария — тоже, поэтому реакция не идет. Это во-первых, а во-вторых, нас спрашивают про газ, а газом здесь и не пахнет. 🙂
Na2CO3 + CaCl2 = 2 NaCl + CaCO3
Карбонат кальция нерастворим, реакция ионного обмена идет, но газа в продуктах в ней нет, поэтому этот вариант нам не подходит.
NH4Cl + NaOH = NH4OH + NaCl
NH4OH можно записать как NH3 и H2O, особенно актуально это для щелочной среды, в ней всегда выделяется аммиак!
NH4Cl + NaOH = NH3 + H2O + NaCl
Аммиак — газ, да еще и ядовитый, поэтому этот вариант нам подходит.
CuSO4 + 2 KOH = Cu(OH)2 + K2SO4
Гидроксид меди нерастворим, но газа здесь не наблюдается.
http://www.sites.google.com/site/himulacom/%D0%B7%D0%B2%D0%BE%D0%BD%D0%BE%D0%BA-%D0%BD%D0%B0-%D1%83%D1%80%D0%BE%D0%BA/9-%D0%BA%D0%BB%D0%B0%D1%81%D1%81-%D0%B2%D1%82%D0%BE%D1%80%D0%BE%D0%B9-%D0%B3%D0%BE%D0%B4-%D0%BE%D0%B1%D1%83%D1%87%D0%B5%D0%BD%D0%B8%D1%8F/%D1%83%D1%80%D0%BE%D0%BA-10-%D1%80%D0%B5%D0%B0%D0%BA%D1%86%D0%B8%D0%B8-%D0%B8%D0%BE%D0%BD%D0%BD%D0%BE%D0%B3%D0%BE-%D0%BE%D0%B1%D0%BC%D0%B5%D0%BD%D0%B0-%D0%B8-%D1%83%D1%81%D0%BB%D0%BE%D0%B2%D0%B8%D1%8F-%D0%B8%D1%85-%D0%BF%D1%80%D0%BE%D1%82%D0%B5%D0%BA%D0%B0%D0%BD%D0%B8%D1%8F/%D0%B7%D0%B0%D0%B4%D0%B0%D0%BD%D0%B8%D1%8F-%D0%BF%D0%BE-%D1%82%D0%B5%D0%BC%D0%B5-%D1%80%D0%B5%D0%B0%D0%BA%D1%86%D0%B8%D0%B8-%D0%B8%D0%BE%D0%BD%D0%BD%D0%BE%D0%B3%D0%BE-%D0%BE%D0%B1%D0%BC%D0%B5%D0%BD%D0%B0
http://spadilo.ru/zadaniye-8-oge-po-ximii/