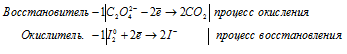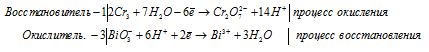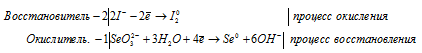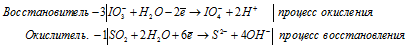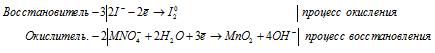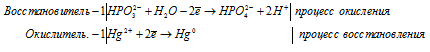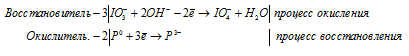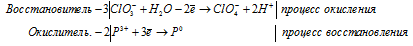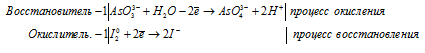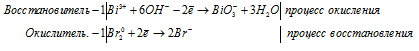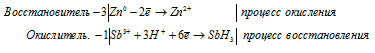Закончите уравнения реакций, схемы которых:а) Н2O + SO2 -→б) К2O + Н2O→в) Ba + Н2O→г) K + H2O→д) CaH2 + H2O→е) Al3C4 + Н2O→ Укажите
Ваш ответ
решение вопроса
Похожие вопросы
- Все категории
- экономические 43,299
- гуманитарные 33,630
- юридические 17,900
- школьный раздел 607,256
- разное 16,836
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Оксид калия: способы получения и химические свойства
Оксид калия K2O — Бинарное неорганическое вещество . Белый, термически устойчивый.
Относительная молекулярная масса Mr = 94,20; относительная плотность для тв. и ж. состояния d = 2,33; tпл = 740º C при избыточном давлении.
Способ получения
1. Оксид калия можно получить путем взаимодействия калия и гидроксида калия при 450º С, в результате образуется оксид калия и водород :
2K + 2KOH = 2K2O + H2
2. При взаимодействии надпероксида калия и калия при температуре 700º C и избыточном давлении образуется оксид калия:
Химические свойства
1. При разложении оксида калия образуется пероксид калия и калий, температура при этом должна быть 350–430º С:
2. Оксид калия взаимодействует со сложными веществами:
2.1. Оксид калия реагирует с водой . Образуется гидроксид калия:
2.2. Оксид калия взаимодействует с кислотами . При этом образуются соль и вода.
Например , оксид калия с разбавленной соляной кислотой образует хлорид калия и воду:
K2O + 2HCl = 2KCl + H2O.
2.3. При взаимодействии калия с оксидами образуются соли.
2.3.1. Реагируя с углекислым газом при 400º C оксид калия образует карбонат калия:
2.3.2. При 150–200º C, в результате взаимодействия оксида калия, и оксидом азота (IV) образуются нитрат калия и нитрит калия:
2.3.3. Оксид калия взаимодействует с оксидом алюминия при 1000º С. При это образуется алюминат калия:
Составление уравнений реакций окислительно-восстановительных процессов
Задача 637.
Закончить уравнения реакций, записать их в молекулярной форме:
а) С2O4 2- + I2 → CO2 +
б) BiO3 — + Cr 3+ + H + → Cr2O7 2- +
в) SeO3 2- + I — + H2O → Se +
г) IO3 — + SO2 + H2O →
Решение:
а) С2O4 2- + I2 → CO2 +
Молекулярная форма процесса
б) BiO3 — + Cr 3+ + H + → Cr2O7 2- +
После приведения членов в обеих частях равенства получим:
Молекулярная форма процесса:
в) SeO3 2- + I — + H2O → Se +
Молекулярная форма процесса:
Молекулярная форма процесса:
Задача 638.
Закончить уравнения реакций, записать их в молекулярной форме:
а) MnO4 — + I — + H2O →
б) HPO3 2- + Hg 2+ + H2O → Hg +
в) P + IO3 — + OH — →
г) PCl3 + ClO3 — + H2O →
д) AsO3 — + I2 + H2O → AsO4 — +
е) Bi 3+ Br2 + OH — → BiO3 — +
ж) Sb3+ + Zn + H + → SbH3 +
Решение:
а) MnO4 — + I — + H2O →
Молекулярная форма процесса:
б) HPO3 2- + Hg 2+ + H2O → Hg +
Молекулярная форма процесса:
в) P + IO3 — + OH — →
Молекулярная форма процесса:
3ClO3 — + 2P 3+ + 3H2O → 3ClO4 — + 2P 0 + 6H +
Молекулярная форма процесса:
Молекулярная форма процесса:
е) Bi 3+ Br2 + OH — → BiO3 — +
Ионно-молекулярная форма процесса:
Молекулярная форма процесса:
ж) Sb3+ + Zn + H + → SbH3 +
Уравнения полуреакций:
Sb 3+ + 3Zn 0 + 3H + → SbH3 + 3Zn 2+
http://chemege.ru/oksid-kaliya/
http://buzani.ru/zadachi/khimiya-glinka/1219-zakanchivanie-uravnenij-reaktsij-zadacha-637