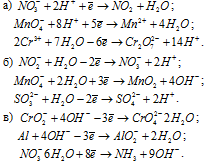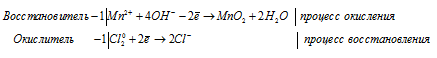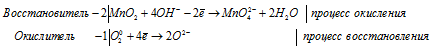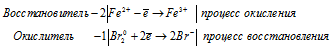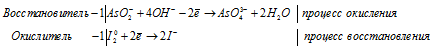Составление уравнений полуреакций окисления с учетом кислотности среды
Задача 625.
Составить уравнения полуреакций окисления с учетом кислотности среды: 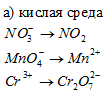
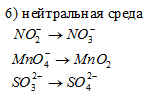
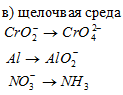
Решение:
Задача 626.
Закончить уравнения реакций:
а) Mn(OH)2 + Cl2 + KOH = MO2 +
б) MnO2 + O2 + KOH = K2MnO4 +
в) FeSO4 + Br2 + H2SO4 =
г) NaAsO2 + I2 + NaOH = Na3AsO4 +
Решение:
а) Mn(OH)2 + Cl2 + KOH = MO2 +
Одна молекула Mn(OH)2 превращается в один ион Mn 2+ и два иона OH — :
Источником кислорода для протекания процесса превращения Mn 2+ в MnO2 служат ионы OH — в щелочной среде. Окислителем данного процесса являются атомы хлора из молекул Cl2.
Марганец повышает свою степень окисления от +4 до +6, т. е. проявляет свойства восстановителя, а кислород понижает свою степень окисления от 0 до -2, проявляя свойства окислителя.
Молекулярная форма процесса:
2Fe 2+ + Br2 0 = 2Fe 3+ + 2Br —
Молекулярная форма процесса:
г) NaAsO 2 + I 2 + NaOH = Na 3 AsO 4 +
AsO 2- + I2 0 + 4OH — = AsO4 3- + 2I — + 2H2O
Гидроксид марганца II
| Гидроксид марганца II | |
|---|---|
| Систематическое наименование | Гидроксид марганца II |
| Традиционные названия | Гидроокись марганца |
| Хим. формула | Mn(OH)2 |
| Состояние | светло-розовые кристаллы |
| Молярная масса | 88,95 г/моль |
| Плотность | 3,258 г/см³ |
| Растворимость | |
| • в воде | 0,0002 г/100 мл |
| Показатель преломления | 1,681; 1,723 |
| Рег. номер CAS | 18933-05-6 |
| PubChem | 73965 |
| Рег. номер EINECS | 606-171-3 |
| SMILES | |
| ChEBI | 143901 |
| ChemSpider | 66594 и 23354143 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Гидроксид марганца II — неорганическое соединение, гидроксид металла марганца с формулой Mn(OH)2, светло-розовые кристаллы, не растворимые в воде.
Содержание
Описание
Гидроксид марганца II — студнеобразный светло-розовый осадок. Нерастворим в воде. Проявляет слабо основные свойства. Окисляется на воздухе.
Гидроксид марганца II образует светло-розовые кристаллы триклинной сингонии, пространственная группа P 3 m1, параметры ячейки a = 0,334 нм, c = 0,468 нм, Z = 1.
Реакция взаимодействия гидроксида марганца (II) кислорода и воды
Реакция взаимодействия гидроксида марганца (II) кислорода и воды
Уравнение реакции взаимодействия гидроксида марганца (II) кислорода и воды:
Реакция взаимодействия гидроксида марганца (II) кислорода и воды.
В результате реакции образуется гидроксида марганца (IV).
Реакция протекает при нормальных условиях.
Формула поиска по сайту: 2Mn(OH)2 + O2 + 2H2O → 2Mn(OH)4.
Реакция взаимодействия фтороводорода и оксида серы (VI)
Реакция взаимодействия оксида галлия (III) и йодоводорода
Реакция взаимодействия оксида ванадия (V) и кальция
Выбрать язык
Популярные записи
Предупреждение.
Все химические реакции и вся информация на сайте предназначены для использования исключительно в учебных целях — только для решения письменных, учебных задач. Мы не несем ответственность за проведение вами химических реакций.
Химические реакции и информация на сайте
не предназначены для проведения химических и лабораторных опытов и работ.
http://chem.ru/gidroksid-marganca-ii.html
http://chemicalstudy.ru/reaktsiya-vzaimodejstviya-gidroksida-margantsa-ii-kisloroda-i-vody/