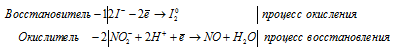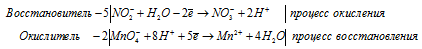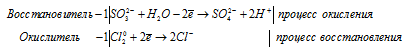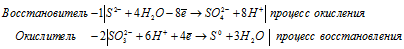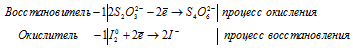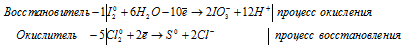Please wait.
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 6e1ac2228b11426c • Your IP : 85.95.188.35 • Performance & security by Cloudflare
Закончите уравнения реакций na h2s
Вопрос по химии:
ПОМОГИТЕ ПОЖАЛУЙСТА.
Закончите уравнения реакций:
S + O2
S + Na
S + H2
Расставьте коэффициенты методом электронного баланса, укажите окислитель, восстановитель
Трудности с пониманием предмета? Готовишься к экзаменам, ОГЭ или ЕГЭ?
Воспользуйся формой подбора репетитора и занимайся онлайн. Пробный урок — бесплатно!
Ответы и объяснения 1
S(0)-4e = S(+4) восстановитель, окисление
O2(0) +4e=2O(-2) окислитель, восстановление
S(0)+2e=S(-2) 1 окислитель, восстановление
Na(0)-1e=Na(+1) 2 восстановитель, окисление
S(0)+2e =S(-2) окислитель, восстановление
H2-2e=2H(+1) восстановитель, окисление
Знаете ответ? Поделитесь им!
Как написать хороший ответ?
Чтобы добавить хороший ответ необходимо:
- Отвечать достоверно на те вопросы, на которые знаете правильный ответ;
- Писать подробно, чтобы ответ был исчерпывающий и не побуждал на дополнительные вопросы к нему;
- Писать без грамматических, орфографических и пунктуационных ошибок.
Этого делать не стоит:
- Копировать ответы со сторонних ресурсов. Хорошо ценятся уникальные и личные объяснения;
- Отвечать не по сути: «Подумай сам(а)», «Легкотня», «Не знаю» и так далее;
- Использовать мат — это неуважительно по отношению к пользователям;
- Писать в ВЕРХНЕМ РЕГИСТРЕ.
Есть сомнения?
Не нашли подходящего ответа на вопрос или ответ отсутствует? Воспользуйтесь поиском по сайту, чтобы найти все ответы на похожие вопросы в разделе Химия.
Трудности с домашними заданиями? Не стесняйтесь попросить о помощи — смело задавайте вопросы!
Химия — одна из важнейших и обширных областей естествознания, наука о веществах, их составе и строении, их свойствах, зависящих от состава и строения, их превращениях, ведущих к изменению состава — химических реакциях, а также о законах и закономерностях, которым эти превращения подчиняются.
Составление уравнений реакций, характеризующих окислительно-восстановительную двойственность элементов
Задача 633.
Закончить уравнения реакций. Обратить внимание на окислительно-восстановительную двойственность элементов, находящихся в промежуточной степени окисленности:
а) KI + HNO2 + CH3COOH ⇒ NO +
KMnO4 + KNO2 + H2SO4 ⇒ KNO3 +
б) H2SO3 + Cl2 + H2O ⇒ H2SO4 +
H2SO3 + H2S ⇒ S +
в) Na2S2O3 + I2 ⇒ Na2S4O6 +
Cl2 + I2 + H2O ⇒ HIO3 +
Решение:
а)
1). KI + HNO2 + CH3COOH ⇒ NO +
После приведения членов обеих частей уравнения, получим:
2). KMnO 4 + KNO 2 + H 2SO 4 ⇒ KNO 3 +
После приведения членов обеих частей уравнения, получим:
В KNO3 атом азота находится в своей промежуточной степени окисления +4, поэтому KNO3 в реакциях окисления-восстановления может проявлять свойства как окислителя (реакция 1), так и восстановителя (реакция 2).
б)
1). H 2 SO 3 + Cl 2 + H 2 O ⇒ H 2 SO 4 +
После приведения членов обеих частей уравнения, получим:
2). H 2 SO 3 + H 2 S ⇒ S +
После приведения членов обеих частей уравнения, получим:
В H2SO3 атом серы находится в своей промежуточной степени окисления +4, поэтому H2SO3 в реакциях окисления-восстановления может проявлять свойства как окислителя (реакция 2), так и восстановителя (реакция 1).
в)
1). Na 2 S 2 O 3 + I 2 ⇒ Na 2 S 4 O 6 +
После приведения членов обеих частей уравнения, получим:
2). Cl 2 + I 2 + H 2 O ⇒ HIO 3 +
После приведения членов обеих частей уравнения, получим:
В I2 атом йода находится в своей промежуточной степени окисления 0, поэтому I2 в реакциях окисления-восстановления может проявлять свойства как окислителя (реакция 1), так и восстановителя (реакция 2).
http://online-otvet.ru/himia/5cea796296f4e19a29047cf2
http://buzani.ru/zadachi/khimiya-glinka/1215-okislitelno-vosstanovitelnuyu-dvojstvennost-elementov-zadacha-633