Составьте уравнение реакции и расставьте коэффициенты ZnCl2+K4[Fe(CN)6]
Ваш ответ
решение вопроса
Похожие вопросы
- Все категории
- экономические 43,297
- гуманитарные 33,622
- юридические 17,900
- школьный раздел 607,223
- разное 16,830
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
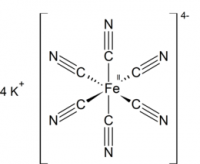
Желтая кровяная соль
| Калий железистосинеродистый | |
|---|---|
 | |
 |
наименование
тригидрат — бледно-жёлтые кристаллы
650 °C
Гексацианоферрат (II) калия (железистосинеродистый калий, ферроцианид калия, гексацианоферроат калия, жёлтая кровяная соль) — комплексное соединение двухвалентного железа K4[Fe(CN)6], существующее обычно в виде тригидрата K4[Fe(CN)6]·3H2O.
Содержание
- 1 История открытия и тривиальные названия
- 2 Получение
- 3 Химические свойства
- 4 Токсичность
- 5 Применение
- 6 Мнемоническое правило
История открытия и тривиальные названия
- жёлтая кровяная соль — кристаллогидрат K4[Fe(CN)6]·3H2O.
- жёлтое синькали
- жёлтая соль
- кровещелочная соль
Тривиальное название появилось из-за того, что ранее «жёлтую кровяную соль» получали путём сплавления отходов с боен (в частности, крови) с поташом и железными опилками. Это, а также жёлтый цвет кристаллов, обусловили название соединения.
Получение
В настоящее время в промышленности получают из отработанной массы после очистки газов на газовых заводах (содержит цианистые соединения); эту массу обрабатывают суспензией Ca(OH)2; фильтрат, содержащий Ca2[Fe(CN)6], перерабатывают путём последовательного добавления сначала KCl, а затем K2CO3.
Он также может быть получен путём взаимодействия суспензии FeS с водным раствором KCN. Реакцию можно представить следующей схемой:
1. цианид калия переводит Fe 2+ в белый осадок гексацианоферрата(II) железа(II) (а не в цианид железа(II), как считалось ранее, что вытекает из взаимодействия этого цианида со щёлочью: 3Fe(CN)2 + 4KOH → 2Fe(OH)2↓ + K4[Fe(CN)6]):
2. затем осадок растворяется в избытке KCN с образованием «жёлтой кровяной соли»:
Fe2[Fe(CN)6] + 12CN − → 3[Fe(CN)6] 4−
Химические свойства
Светло-жёлтые кристаллы с тетрагональной решеткой, существующие в виде тригидрата K4[Fe(CN)6]·3H2O.
Плотность 1,853 г/см³ при 17 °C. Растворимость в воде 31,5 г/100 г при 25 °C, 48,3 г при 50 °C. Практически не растворяется в эфире, этаноле, пиридине, анилине, этилацетате.
Гексацианоферрат(II) калия диамагнитен.
Выше 87,3 °C (по другим данным, выше 120 °C) превращается в безводную соль с плотностью 1,935 г/см³. Выше 650 °C разлагается:
В реакции с соляной кислотой выделяется белый осадок железистосинеродистой кислоты (H4[Fe(CN)6]).
С концентрированной серной кислотой реагирует по уравнению:
Этим способом можно пользоваться в лаборатории для получения монооксида углерода.
С солями металлов в степени окисления +2 и +3, образует малорастворимые соединения гексацианоферратов(II) (см. в разделе «применение»).
В водных растворах окисляется хлором и другими окислителями, такими, как пероксид водорода до K3[Fe(CN)6]:
Анион [Fe(CN)6] 4− очень прочен (константа нестойкости 8⋅10 -36 ), не разлагается ни щелочами, ни кислотами, устойчив по отношению к воздуху; поэтому растворы ферроцианидов не показывают реакций ни на Fe 2+ , ни на CN − .
Токсичность
Нейтральное вещество, не разлагается в воде и внутри человеческого организма. Летален при приёме перорально дозы в 6400 мг/кг (испытания на крысах).
Применение
Применяют при изготовлении пигментов, крашении шёлка, в производстве цианистых соединений, ферритов, цветной бумаги, как компонент ингибирующих покрытий и при цианировании сталей, для выделения и утилизации радиоактивного цезия.
В Российской Федерации широко применяют при производстве продуктов питания — соли, творожных продуктов, в виноделии и пр.
Гексацианоферрат(II) калия применяется в аналитической химии как реактив для обнаружения некоторых катионов:
1. Fe 3+ : образуется малорастворимый синий осадок «берлинской лазури»:
или, в ионной форме
Получающийся гексацианоферрат(II) калия-железа(III) слабо растворим (с образованием коллоидного раствора), поэтому носит название «растворимая берлинская лазурь».
2. Zn 2+ : образуется белый осадок гексацианоферрата(II) цинка-калия:
или, в ионной форме
3. Cu 2+ : из нейтральных или слабокислых растворов выпадает красно-бурый осадок гексацианоферрата(II) меди(II):
или, в ионной форме
В пищевой промышленности ферроцианид калия зарегистрирован в качестве пищевой добавки E536, препятствующей слёживанию и комкованию. Применяется как добавка к поваренной соли.
Мнемоническое правило
Для того, чтобы запомнить формулу желтой кровяной соли K4[Fe(CN)6] и не спутать её с красной кровяной солью K3[Fe(CN)6], существует мнемоническое правило:
- Число атомов калия соответствует числу букв в английских названиях солей: «gold» — 4 буквы, то есть 4 атома калия — желтая кровяная соль (калий железистосинеродистый) K4[Fe(CN)6]. «Red» — 3 буквы, то есть 3 атома калия — красная кровяная соль (калий железосинеродистый) — K3[Fe(CN)6].
[Fe(CN)6] 4–
аммония • бария • железа(II) • железа(III) • калия • кальция • кобальта • магния • марганца • меди(II) • натрия • никеля • олова • свинца • стронция • таллия • цинка • Железистосинеродистая кислота H4[Fe(CN)6]
[Fe(CN)6] 3–
железа(II) • железа(II,III) • калия • кальция • кобальта • меди(I) • натрия • неодима(III) • олова • свинца • Железосинеродистая кислота H3[Fe(CN)6]
Zncl2 k4 fe cn 6 ионное уравнение
Составьте молекулярные и ионно-молекулярные уравнения реакций, которые надо провести для осуществления следующих превращений:
Fe ⟶ FeCl2 ⟶ Fe(CN)2 ⟶ K4[Fe(CN)6] ⟶ K3[Fe(CN)6]
К окислительно-восстановительным реакциям составьте электронные уравнения.
| Fe + 2HCl ⟶ FeCl2 + H2↑ Fe + 2H + + 2Cl — ⟶ Fe 2+ + 2Cl — + H2↑ Fe + 2H + ⟶ Fe 2+ + H2↑ | ||||
| Fe 0 — 2ē ⟶ Fe +2 | 2 | 2 | 1 | восстановитель (окисление) |
| 2H + + 2ē ⟶ H2 0 | 2 | 1 | окислитель (восстановление) | |
FeCl2 + 2KCN ⟶ Fe(CN)2↓ + 2KCl
Fe 2+ + 2Cl — + 2K + + 2CN — ⟶ Fe(CN)2↓ + 2KCl
Fe 2+ + 2CN — ⟶ Fe(CN)2↓
http://chem.ru/zheltaja-krovjanaja-sol.html
http://gomolog.ru/reshebniki/1-kurs/shimanovich-2014/429.html




